운동이 혈관신생 인자 발현에 미치는 영향
Abstract
PURPOSE
Exercise is one of the strongest stimuli for the induction of angiogenesis that is defined as a formation of new blood vessel. However, underlying mechanism of exercise-induced angiogenesis is not fully uncovered. Therefore, we reviewed the effect of exercise on angiogenic factors such as vascular endothelial growth factor (VEGF), angiopoietin (ANG) and platelet-derived growth factor (PDGF) in heart, skeletal muscle and adipose tissue.
METHODS
In this review, we summarized the function of angiogenic factors and their roles in heart, skeletal muscle and adipose tissue.Also we discussed the alteration of angiogenic gene expression after exercise in three organs mentioned above.
RESULTS
Angiogenic regulators play a critical role in cardiac development, skeletal muscle regeneration and adipose tissue metabolism. Exercise-induced angiogenic factors contributes to the enhancement of vascular remodeling, mobilization of endothelial precursor cell and systemic metabolism. In terms of VEGF, its induction after exercise is regulated mainly by HIF-α and PGC1-α, transcriptional factors of VEGF, whereas the mechanism of exercise-induced ANG and PDGF-B expression is not clear yet.
CONCLUSIONS
Acute exercise, resistance exercise and endurance training increase VEGF, ANG1, ANG2 and PDGF-B expression. Thereby, exercise eventually prevents diseases including cardiovascular impairment, muscle atrophy and metabolic syndrome by increasing or maintaining blood vessel density in heart, skeletal muscle and adipose tissue.
색인어: 운동, 혈관신생, VEGF, Angiopoietin, PDGF
Keywords: Exercise, Angiogenesis, VEGF, Angiopoietin, PDGF
서 론
신체 내 대부분의 장기에 존재하는 혈관은 산소 및 영양소를 장기에 공급하면서 장기의 항상성을 유지시키는 역할을 수행할 뿐만 아니라 장기의 발달, 염증의 발생, 조직 내의 대사 그리고 암의 발생 및 전이 과정에서 조직의 미세 환경을 조절하는 데 있어 중요한 인터페이스를 제공한다. 혈관의 다양한 기능은 혈관의 안쪽 벽면을 구성하고 있는 혈관내피세포(endothelial cell) 및 혈관외벽에 붙어있는 평활근세포(smooth muscle cell) 또는 혈관주위세포(pericyte)에 의해 조절되며, 각 장기의 혈관내피세포는 그 모양과 생물학적 특성에 있어 조직별로 특이성을 보이는 것으로 알려져 있다. 일반적으로 성인에 있어 각 장기의 혈관은 새로이 생겨나거나 증가하지 않으나 운동 또는 염증 및 암과 같은 질환에서는 기존의 혈관에서 새로운 혈관이 생성되는 혈관신생(angiogenesis)이 관찰된다. 특히 저항성 운동 및 장기간의 지구성 운동으로부터 생성된 혈관은 생체 내에 보다 원활한 혈류의 흐름을 제공함으로써 건강을 유지하는 데 유익한 효과를 제공한다. 운동을 통한 혈관신생은 다양한 혈관신생 인자들에 의해 조절되며 대표적인 혈관신생 인자로는 vascular endothelial growth factor (VEGF) 및 angiopoietin (Ang) 그리고 혈관의 안전성(integrity)을 조절하는 데 있어 중요한 역할을 담당하는 platelet-derived growth factor (PDGF) 등이 있다. 운동은 심장 및 근육의 혈관신생 및 지방 크기의 감소를 동반한 체중감소를 유발한다[ 1- 3]. 이에 본 연구에서는 운동과 밀접한 관련이 있는 근육, 심장 그리고 지방의 혈관 특성을 혈관의 구성 및 혈관신생 인자를 중심으로 알아보고 이를 바탕으로 운동이 혈관신생에 미치는 영향을 알아보고자 한다.
1. 혈관신생 인자
1) VEGF
VEGF는 가장 강력한 혈관신생 인자 중 하나이다. VEGF 구성원(family)은 VEGFA, VEGFB, VEGFC, VEGFD 및 placental growth factor (PlGF)를 포함한다. 특히 VEGFA는 선택적 접합(alternative splicing)을 통해 다양한 아형(isoform) (VEGF 121, VEGF 165, VEGF 189, VEGF 206)을 갖는다. VEGFA는 혈관투과성 인자 (vascular permeability factor)로 발견되었으며 혈관투과력은 히스타민(histamine)보다 몇 천 배 이상 높은 것으로 알려졌다[ 4]. 이후의 연구 결과들로부터 VEGFA는 혈관신생을 유도하며 혈관내피세포(endothelial cell)의 분화, 이동, 증식 및 생존 등을 조절하여 새로운 혈관을 생성하는 데 중요한 자극원이라는 것이 알려졌다[ 5]. VEGFA는 타이로신 수용체 키나아제(tyrosine receptor kinase)인 VEGF receptor (VEGFR)1, VEGFR2 그리고 VEGFR3와 결합한다. VEGF는 또한 neurophilin (NRP) 구성원(family)인 NRP1 및 NRP2 그리고 heparan sulfate proteoglycan (HSPGs)과도 결합한다[ 6]. VEGF의 수용체 중 VEGFR2가 혈관내피세포의 신호 전달을 중재하는 주된 수용체이다. VEGFA가 VEGFR2와 결합되면 수용체의 tyrosine이 인산화되며(phosphorylation), 이에 따라 세포 사멸(apoptosis)을 억제하는 기능을 가지고 있는 protein kinase B (PKB)가 활성화되고 또한 세포의 증식을 조절하는 mitogen-activated protein kinase (MAPK)의 활성화가 protein kinase C (PKC)에 의해 조절된다[ 7, 8]. 또한 VEGF는 세포의 이동에 관여하는 Src kinase, focal adhesion kinase, 그리고 p38 MAPK 등을 활성화시킨다[ 9]. VEGF는 발생기 및 출생 후 혈관신생에 중요한 역할을 한다. VEGFA의 대립형질(allele) 중 하나만을 가지고 있는 마우스는 발생기 11일에서 12일(embryonic period day 11-12) 사이에 혈관발달의 결함 및 난황난(york sac)의 혈관 섬(blood islands) 내 적혈구 감소를 동반하며 사망한다[ 10, 11]. 또한 cre-loxP 마우스 시스템을 이용하여 출생 직후 VEGFA의 발현을 억제시킨 마우스는 혈관의 성장을 감소시킴으로써 장기의 발달 결함을 가져온다[ 12]. VEGFR는 마우스의 경우 배아 중배엽(embryonic mesoderm) 7.5-9.5일에 최초로 발현되고 인간의 경우 17주의 태아에서 발현된다[ 13, 14]. 세 개의 VEGF 수용체 중 어느 하나라도 없으면 태아는 사망하며, 특히 VEGFR2를 마우스에서 제거하면 혈관내피세포 및 조혈구세포(hematopoietic cell)의 분화가 억제되어 혈관이 생성되지 않는다[ 15]. 그러나 VEGFR2를 제거한 배아줄기세포로부터 혈관내피세포 또는 조혈구 세포의 전구세포(precursor cell)가 분화되는 것을 보면, VEGFR2가 이들 전구세포의 분화에는 영향을 미치지는 않는 것으로 사료된다[ 16].
2) Ang
Ang 구성원은 Ang1과 Ang2를 포함한다. Ang1은 혈관주변의 동맥평활근세포, 혈관주위세포, 섬유아세포(fibroblast) 그리고 암세포 등에서 발현하며, Ang2는 주로 혈관내피세포에서 발현한다[ 17]. Ang의 수용체는 TEK tyrosine kinase receptor 2 (Tie2)로 Ang가 Tie2에 결합함으로써 배아 중기 또는 혈관의 재형성 과정 및 정상혈관에서의 성숙(maturation) 및 안정화에 기여한다[ 18, 19]. Tie2 수용체는 주로 혈관내피세포에서 발현하나 암의 생성 시 혈관신생을 자극하는 단백질을 분비하는 일부 단핵세포(monocyte) 또는 대식세포(macrophagy)에서도 발현하는 것으로 알려져 있다[ 20, 21]. Tie2는 혈관의 발달, 조혈작용 및 심장 내막(endocardium)의 발달에 중요한 생물학적 역할을 한다[ 22]. Ang1을 제거한 마우스에서는 Tie2를 제거한 마우스에서와 동일하게 배아 단계에서 사망하는 현상이 관찰된다[ 18]. Ang1에 의해 Tie2가 활성화되면 phosphoinositide 3-kinase (PI3K)를 경유한 PKB의 세린(serine) 및 트레오닌(threonine)이 인산화되어 혈관내피세포의 생존을 강화하고 세포괴사를 억제하는 신호전달이 이루어지며 혈관내피세포의 이동(migration)을 자극한다[ 23, 24]. 또한 Tie2의 활성은 VEGF에 의해 유도되는 혈관내피세포의 투과를 억제하는 기능을 가지고 있다[ 25]. Ang1은 α v-integrin 및 integrin α5와 결합하여 심근세포의 생존력을 증가시키고 근세포 및 신경세포의 기능을 강화한다[ 26]. Ang1은 VEGF에 의해 유도되는 혈관 염증성 단백질인 intercellular adhesion molecule-1 (ICAM1) 및 vascular cell adhesion molecule-1 (VCAM1)의 발현을 억제시킴으로써 혈관의 염증을 억제시키고[ 27, 28], VEGF 및 tumor necrosis factor-α (TNFα)에 의해 유도되는 혈액응고를 억제한다[ 29, 30]. 혈관의 안정성은 혈관주변의 평활근세포 및 혈관주위세포의 동원(recruitment)에 의해 유지되며, Ang1을 과발현(overexpression)시키면 이 두 세포의 동원을 증가시켜 혈관의 휴지기(quiescent)가 증가된다[ 31, 32]. 또한 Ang1의 처치 또는 과발현은 심근 허혈을 감소시키고 사지(limb), 심장, 뇌, 관찰 및 신장 등에서 발생한 장애를 복구하는 데 중요한 역할을 하는 것으로 알려져 있다[ 33- 37]. 반면, Ang2는 Ti2에 결합하여 Ang1에 의한 Tie2 수용체의 신호전달을 방해하는 길항작용을 하며[ 18, 38] 또한 integrin에 결합하여 Ang1에 의한 항 염증성 기능을 억제하는 것으로 알려졌다[ 39, 40]. Ang2는 혈관내피세포에서 주로 발현되며 산소결핍, shear stress 그리고 VEGF 등에 의해 그 발현이 증가된다[ 41]. Ang2의 과발현은 혈관생성을 억제하여 발달기에 마우스가 사망하는 현상을 보이며 이런 현상은 Ang1 또는 Tie2의 발현을 억제한 마우스에서 보이는 현상과 동일하다[ 18, 38]. 따라서 혈액 내 Ang2의 농도가 증가하는 것은 생체 내 부정적인 영향을 가져올 수 있다. 더욱이, 염증성 질환 및 제2형 당뇨에서는 혈액 내 Ang2의 농도가 증가한다[ 42, 43].
3) PDGF
PDGF는 PDGF-A, PDGF-B, PDGF-C 그리고 PDGF-D로 구성되어 있으며 이들은 각각 이중 결합(dimerization)하여 PDGF-AA, PDGF-BB, PDGF-AB, PDGF-CC 및 PDGF-DD를 형성한다[ 44]. 이들 PDGF family는 두 개의 수용체인 platelet-derived growth factor receptor (PDGFR)α 및 PDGFRβ에 결합한다[ 45]. 이 중 PDGF-B에 의한 PDGFRβ 활성화는 심혈관 발달에 매우 중요하며 또한 잠재적으로 혈관신생에 중요한 역할을 한다. PDGF-B는 특히 발달 단계 초기에 배아 줄기세포를 혈관내피세포로 분화시키며 분화된 혈관내피세포의 증식, 이동 그리고 관 형성(tube formation)에 중요한 역할을 담당한다[ 46]. PDGFB와 PDGFRβ 는 각각 혈관내피세포 및 혈관주위세포에 발현하며[ 47], 혈관에서 발현되는 PDGF-B의 발현을 억제시키면 혈관의 안정화를 위해 필요한 혈관주위세포를 동원하는 데 결함이 생겨 혈관 자체의 안정성이 저하된다[ 47, 48]. 유전자 조작 마우스를 대상으로 한 실험 결과들은 혈관신생 과정에서 PDGF는 다른 혈관신생 인자들과 협력하여 혈관주위세포를 동원함으로써 혈관신생 및 새로이 형성된 혈관의 안정화에 기여한다는 것을 보여준다. PDGF-B 또는 PDGFRβ의 발현을 제거한 마우스는 태어난 직후 많은 조직에서 혈관 형성의 결함을 보인다[ 49, 50]. 뿐만 아니라 PDGFRα 및 PDGFRβ를 동시에 제거한 마우스는 난황난의 혈관 발달에 결함을 보인다[ 51]. 이는 난환난에서의 PDGF는 세포외 기질(extracellular matrix)을 축적하여 혈관의 재형성을 촉진하는 데 필수적인 단백질이기 때문이다. PDGF-B의 가장 중요한 기능은 혈관주위로 혈관주위세포를 동원하는 것이기에 정맥보다는 동맥에서 그 발현이 보다 강하다[ 52, 53].
2. 조직별 혈관신생 인자의 역할
1) 심장
심장의 모세혈관은 배아 단계 시 외심막을 형성하는 전구세포(proepicardium)에서 기원하는 것으로 알려졌으나 최근의 연구결과들은 심장 모세혈관의 일부만이 외심막을 형성하는 전구세포에서 기원하고 대부분의 모세혈관은 정동맥(sinus venosus) 및 심장내막(endocardium)에서 기원하는 것으로 보고하고 있다. 특히 정동맥에서 제공하는 혈관내피세포의 전구세포는 심실의 측부 자유벽(lateral free wall) 내에 심혈관 바닥(bed)을 형성하며 VEGF에 의해 관상동맥을 형성하는 데 공헌한다[ 54- 56]. 이에 반해, 심근내막 전구세포는 심실 및 배아심장의 복부벽(ventral wall)에서 기인한다[ 56, 57]. 심장에서 혈관이 형성되는 생물학적 기전이 모두 밝혀지지는 않았으나 심근에서 유도된 VEGF가 심장 모세혈관의 전구세포를 자극함으로써 혈관생성에 관여하며[ 57], 심근에서 유도된 Ang1이 심장 내 관상정맥의 형성에 기여하는 것으로 알려져 있다[ 58]. 한편, 심장 내의 혈관주위세포는 평활근세포로 분화하여 관상동맥의 재생 시 관상동맥의 바깥쪽을 둘러싼다[ 59]. 심장에서 혈관이 중요한 이유는 죽상관상동맥 질환이 발생하면 심근의 허혈 및 심한 경우 심근증을 유발하여 생명에 치명적인 결과를 유도하기 때문이다. 죽상관상동맥 질환은 혈관 내 혈액의 흐름에 의해 발생하는 shear stress에 의해 감소될 수 있으며[ 60], 혈류 자극(shear stress)을 강화하는 주된 자극원 중의 하나는 바로 운동이다. 그러나 혈관 내 혈류의 흐름이 난류(turbulence)를 일으키는 혈관에서는 염증성 반응의 증가 및 Hippo signaling의 억제로 죽상관상동맥의 발생이 가속화되기도 한다[ 61]. 또한 혈관내피세포의 대사(metabolism) 역시 관상동맥질환의 발생과 밀접한 관련이 있다[ 62]. PKB 기질(substrate)로 사용되는 forkhead boxO (FOXO)는 세포의 성장, 분화 그리고 대사에 관여하는 전사인자(transcription factor)이다[ 63]. 혈관내피세포의 대사는 생체 내의 대사과정에 의해 직접적인 영향을 받는다. 특히 인슐린 저항성 환자에서는 FOXO1과 FOXO3가 혈관내피세포에서 활성화됨으로써 혈관의 염증성 단백질의 발현을 증가시키고 죽상관상동맥을 안정화시키는 인슐린 신호체계를 억제한다[ 64]. 물론 인슐린 민감성을 혈관내피세포에서 강화시키면 죽상관상동맥을 가속화시키는 모순적인 일이 발생하기도 한다[ 65].
2) 근육
근육에 존재하는 위성세포(satellite cell)는 근세포의 전구세포로써 근육의 발달 및 성장 그리고 재생에 중요한 역할을 한다[ 66]. 근육세포의 분화 및 성장은 hepatocyte growth factor (HGF)에 의해 조절된다. 근육의 혈류량은 운동 중 급격히 증가한다. 안정 시 근육은 심박출량의 약 20%를 받아들이지만 운동 중에는 심박출량의 80%까지를 받아들일 수 있다. 이와 같이 운동 시 근육에서 사용하는 혈액량의 증가는 운동기능과 밀접한 관련이 있다. 특히, 운동 시 요구되는 충분한 혈액을 공급받지 못한 근육은 저산소증으로 인한 근육 피로를 야기하여 운동 수행력의 현저한 저하를 보이게 된다. 따라서 근육 내의 적정수준 이상의 혈관을 유지하는 것은 운동 생리학적 관점에서 중요한 의미를 갖는다. 근육의 혈관 역시 VEGF의 발현과 밀접한 관련을 보인다. 근육에서 VEGF를 발현하는 주된 세포는 근육세포(myocyte)이다[ 67]. VEGF의 발현을 근육에서 제거하기 위해 VEGF에 flox가 삽입된 마우스의 골격근에 아데노바이러스로 cre 단백질을 발현시키고 4주 후 골격근을 분석하면, 근육세포의 괴사를 동반한 모세혈관의 감소(통제군에 비해 약 64% 감소)가 관찰된다[ 68]. 이와 같은 결과는 VEGF가 골격근의 혈관을 유지하는 것뿐만 아니라 혈관의 유지를 통해 근육세포의 생존에도 관여한다는 것을 보여준다. 근육에서의 VEGF의 발현은 근육 내 저산소증에 의한 hypoxia-inducible factor 1 (HIF-1)의 발현이 그 주된 원인으로 알려져 있다[ 69]. 쥐를 12%의 산소에 3주간 노출시키면 횡격막 및 비장근(soleus)과 같은 골격근의 혈관이 증가되며, 6주간 저산소증에 노출시키면 횡격막, 비장근, 앞 정강근(anterior tibialis) 및 긴발가락폄근(extensor digitorum longus) 등에서의 혈관이 모두 증가한다[ 70, 71]. VEGF의 프로모터(promoter)에 존재하는 HIF-1 결합위치인 hypoxia response element (HRE)를 제거한 마우스의 근육은 혈관 감소를 유도하지는 않지만 심각한 근육의 약화 및 근 수축에 관여하는 운동신경(motor neuron)의 퇴화를 보인다[ 72]. 따라서 HIF-1에 의한 VEGF의 변화는 HRE의 기능과는 별개로 혈관신생에 영향을 미치는 것으로 사료된다. Ang1은 손상된 근육의 재생에 관여한다. 근육의 괴사를 유도하기 위해 cardiotoxin을 앞 정강근에 주입한 마우스는 mRNA 수준에서 Ang1의 발현이 급격히 감소하며 이후 2주 동안 증가한다. 근육에서의 Ang1은 주로 위성세포에서 발현되며 아데노바이러스를 이용한 Ang1의 증가는 앞 정강근의 수축력 및 근섬유의 재생 그리고 근육 내 모세혈관의 증가를 가져온다. 더욱이 근육세포에 Ang1을 처치하면 세포의 증식, 생존 및 이동을 향상시킨다[ 73]. 한편, 위성세포에서 발현되는 Ang2의 역할은 잘 알려져 있지 않다. 그러나 위성세포에서의 Ang2 발현은 염증성 싸이토카인(TNFα, IL1β 또는 IL6) 보다는 과산화수소(hydrogen peroxide)에 의해 증가하는 것으로 보아 근세포의 괴사 시 발현되는 것으로 사료된다. 또한 Ang2를 위성세포에 처치하면 Ang1과 같이 세포의 증식, 생존 및 이동을 향상시킨다[ 74]. 따라서 Ang1과 Ang2는 근육이 손상을 입었을 때 발현되어 근 손상에 의한 근육재생에 관여하는 것으로 사료된다. PDGF-B는 근육 내 혈관에서 주로 발현되며 L6J1 근육세포 [ 75] 및 닭의 근아세포(myoblast)[ 76]에 PDGF-B를 처치하면 세포의 증식은 증가되나 분화는 억제된다. 근육에서 PDGF의 흥미로운 역할 중 하나는 글루코스의 흡수이다. PDGF를 과발현시킨 마우스에서는 근육에서의 glucose transporter 1 (GLUT1)의 유전자 발현을 증가시킴과 동시에 글루코스 흡수율이 증가된다[ 77].
3) 지방
백색지방의 팽창(expansion)은 혈관신생과 밀접한 관련을 갖는다. 지방이 팽창하는 부분에는 혈관신생이 활발하여 혈관이 군집을 이루는 부분이 발견되고 이 부분의 형성을 억제하기 위한 항-혈관신생 인자를 마우스에 주입하면 새로운 백색지방 세포의 생성이 억제된다[ 78]. 뿐만 아니라 혈관내피세포의 증식을 억제시키는 TNP-470을 비만 마우스에 처치하면 혈관신생의 억제로 인해 백색지방의 팽창이 억제되어 비만을 감소시킨다[ 79]. VEGFA의 발현을 지방에서만 제거한 마우스는 고지방 식이에도 불구하고 백색지방 내 혈관 감소를 동반한 백색지방의 크기 감소를 보이지만 지방으로 가지 못한 체내 지질(lipid)이 혈액에 축적됨으로써 인슐린 저항성을 발생시킨다. 한편 지방에서만 VEGFA의 발현을 증가시킨 과발현 마우스는 지방 내 저산소증을 감소시킴으로써 인슐린 민감도를 증가시킨다[ 80]. 이와 같은 결과들은 단순히 혈관신생을 백색지방에서 억제하면 백색지방의 크기를 감소시킬 수는 있으나, 백색지방 팽창의 억제 작용으로 백색지방에서 축적하지 못한 지질이 혈액 및 다른 장기에 축적됨으로써(lipotoxicity), 결과적으로 생체 내 지질 대사 및 글루코스 대사에 부정적인 결과를 초래하여 인슐린 저항성을 유도한다는 것을 보여준다. 따라서 백색지방 내의 혈관 밀도를 증가시키는 것이 비만에 의해 발생하는 성인병의 예방에 효과적일 것으로 판단된다. 백색지방 세포의 전구세포인 3T3L1 세포에서는 Ang1이 발현된다. 더욱이, 비만 쥐의 백색지방은 통제군에 비하여 Ang1의 발현이 감소하며, TNP-470을 처치하여 백색지방의 크기를 감소시킨 마우스 역시 백색지방에서의 Ang1의 발현이 감소한다. 또한 저칼로리 식이로 식이 제한을 시행한 마우스 역시 Ang1의 발현감소를 동반한 백색지방 크기의 감소를 보인다[ 81]. 따라서 Ang1은 백색지방의 팽창 시 혈관의 안정성을 조절하며, 혈액 내의 물질들이 지방으로 유입되는 데 유리한 조건을 생성하는 것으로 판단된다. 반면 Ang2는 고지방 식이에 의해 팽창한 백색지방에서 그 발현이 증가하며 지방에서 Ang2를 과발현시킨 마우스는 백색지방의 혈관신생의 증가와 더불어 백색지방의 팽창을 억제시킴으로써 인슐린 민감도를 증가시킨다. 반면, Ang2 항체를 이용하여 Ang2의 발현을 억제한 마우스는 백색지방 내 혈관 감소와 함께 염증성 싸이토카인의 증가 및 간의 지방 축적을 증가시켜 인슐린 저항성을 악화시킨다[ 82]. 지방에서의 PDGF-B의 역할은 최근에 밝혀졌다. 백색지방의 PDGF-B의 발현은 체중 증가와 함께 증가하며 생체 내 PDGF-B의 활성을 모든 장기에서 제거한 마우스는 백색지방 내 혈관의 숫자와 백색지방 세포의 크기 및 염증을 감소시켜 비만을 억제하고 인슐린 민감도를 증가시킨다. 흥미로운 점은 기존의 연구결과들과는 달리 PDGF-B는 백색지방 내 혈관주위세포를 혈관으로부터 분리시킨다는 점이다[ 83]. 그러나 생체 내의 PDGF는 대부분의 장기에서 발현되며, 특히 PDGFRβ+세포는 장기 마다 혈관주위세포를 포함한 또 다른 세포로 분화할 수 있는 세포이기에 PDGFB의 역할을 지방에서 알아보기 위해서는 추후 지방에서 발현되는 PDGF-B만을 제거한 마우스를 대상으로 이와 같은 결과들은 재검증할 필요가 있다.
3. 운동과 혈관신생 인자
1) 운동에 의한 심장 내 혈관신생 인자 변화
운동은 운동에 참여하는 근육의 혈류를 증가시킨다. 특히, 지구성 운동 후 혈관신생을 통하여 증가된 동맥의 크기와 숫자는 심장의 혈류의 증가를 가져오는 중요한 인자이다[ 84]. 인간을 대상으로 운동에 의한 심장의 혈관신생 인자 변화를 연구하는 것은 거의 불가능하기 때문에, 주로 동물실험을 대상으로 그 결과들이 보고되어 왔다. 돼지 및 개를 이용한 1980년대의 동물실험에서 밝혀진 것처럼 장기간의 지구성 운동은 심장의 모세혈관 수를 증가시킨다[ 85, 86]. 뿐만 아니라 15일 동안 수영 운동을 시행한 쥐 역시 심장의 혈관 수를 증가시켰다. 더욱이 VEGF 단백질 주사 및 수영 운동을 병행하면 근육 내 혈관의 수는 차이가 없으나 심장의 혈관 수는 증가한다[ 87]. 이와 같은 결과는 심장의 혈관이 VEGF에 대한 반응에 있어 근육보다 훨씬 민감하다는 것을 보여준다. VEGF는 운동에 의해 증가되는 심장 모세혈관의 증가에 공헌한다. 제1형 당뇨병의 발생을 유도한 쥐를 대상으로 트레드밀 운동을 시행하면 운동군이 통제군에 비해 심장에서의 VEGF 메신저리보핵산(mRNA) 발현이 유의하게 증가한다[ 88]. VEGF는 단순히 심장의 혈관내피세포의 증식을 통해 혈관의 수를 증가시킬 뿐만 아니라, 혈관내피세포 전구세포(endothelial precursor cell, EPC)의 활성화에도 기여한다[ 89]. 혈관내피세포 전구세포는 골수에서 생성되어 각 장기로 이동한 후 혈관내피세포로 분화하는 세포이며[ 90], VEGF는 골수로부터 EPC를 혈액으로 이동시키는(mobilization) 가장 강력한 단백질 중 하나이다[ 91]. 운동부하검사를 시행한 관상동맥질환들은 검사 후 2-6시간에 혈장 VEGF의 농도가 약 4배 이상 증가하며, 검사 후 48시간에 혈장 내 혈관내피세포 전구세포의 수가 최대로 증가하고 이후 144시간이 지나면 안정 시 수치로 감소한다[ 92]. 질환이 없는 건강한 성인에 있어서도 1,500 m를 최대속도로 주파한 후 혈액 내 혈관내피세포 전구세포의 수를 측정하면 CD34+ 및 CD133+ 혈관내피세포 전구세포의 수가 안정 시에 비해 약 2배 이상 증가하지만 VEGF의 혈액 내 농도는 변화가 없었다[ 93]. VEGF에 의한 혈관내피세포 전구세포의 이동은 운동시간 및 운동강도와 관련이 있는 것으로 사료된다. 최대산소섭취량의 82%에 해당하는 강도로 30분간 달리기를 시행하거나 최대산소섭취량의 62% 강도로 30분간 달리기를 시행한 건강한 성인은 운동 후 혈관내피세포 전구세포가 증가하였으나 최대산소섭취량의 62% 강도로 10분간 달리기를 시행한 경우에는 변화가 없었다[ 94]. 저항성 운동을 3년간 시행한 20대 성인이 6개로 구성된 웨이트 트레이닝을 15회씩 반복하는 근지구성 저항운동을 약 12분간 시행하면 운동 후 10분에 혈액 내 VEGF의 농도가 유의하게 증가하고 2시간 후 혈관내피세포 전구세포의 수가 증가한다[ 95]. 따라서 운동은 혈장 내 VEGF를 증가시켜 심장의 혈관내피세포의 증식을 유도하고 동시에 골수로부터 EPC의 이동을 증가시켜 심장의 혈관신생에 공헌한다고 할 수 있다. 관상동맥질 환자는 혈장 내 VEGF 및 Ang2의 농도가 증가하지만 Ang1의 농도는 변화하지 않는다[ 96]. 더욱이, 심실의 심각한 기능상실을 보이는 심근증 환자에 있어서도 혈장 Ang2의 농도는 증가한다. 흥미롭게도 염증성 인자로 알려진 Ang2의 농도는 심질환자에서 운동 시 감소한다. 관상동맥질환자 13명을 대상으로 간헐적 중강도 운동을 시행한 결과 운동 직후 20분부터 72시간까지 혈중 Ang2의 농도가 운동 전에 비하여 유의하게 감소하였으나 그 관련 기전은 알려져 있지 않다[ 97]. 한편, PDGF-A 또는 PDGF-B를 과발현한 마우스는 심장에 섬유증(fibrosis)을 야기하며[ 98], 혈관 평활근세포(vascular smooth muscle cells)에서 PDGF에 의한 신호전달 체계의 활성화는 동맥 내막을 좁아지게 하는 것으로 알려져 있다[ 99]. 그러나 운동에 의해 심장의 PDGF-B의 발현이 조절되는지에 대해서는 아직까지 구체적인 연구결과가 보고되지 않았다.
2) 운동에 의한 근육 내 혈관신생 인자 변화
국부적인 산소 공급의 결핍 또는 이와 관련된 대사기능의 변화가 운동에 의한 혈관신생 인자의 발현을 자극하는 것으로 알려져 있다[ 100]. Annex et al. [ 101]의 연구에서는 쥐의 골격근에 전기자극을 3-56일까지 주었을 때 VEGF 단백질의 생성이 증가하였으며, 근육 염색 기법으로부터 대부분의 VEGF가 근육세포(myocyte)보다는 골격근 사이의 기질(matrix)에서 발견되었음을 보고하였다. 그러나 근육 내 VEGF 발현 세포의 검증 결과는 오래 전에 시행된 실험의 결과로써 항체의 특이성을 보장할 수 없고, 세포질로부터 분비되는 단백질의 경우 면역염색법으로 관찰이 매우 어렵기에 향후 VEGF 리포터 마우스를 통하여 재검증할 필요가 요구된다. 단순히 in situ 상황에서 전기 자극을 부여한 결과뿐만 아니라 1회성 중강도의 트레드밀 운동(1시간, 15 또는 20 m/min, 10°) 역시 VEGF의 메신저리보핵산 발현을 증가시킨다. Breen et al. [ 102]의 연구에서는 증강도의 1회성 트레드밀 운동 후 4시간까지 VEGF 메신저리보핵산이 2-4배 증가되며 운동 후 8시간에서 24시간 후에 안정 시 수준으로 돌아온다는 것을 보여주었다. 쥐를 1일당 4회씩 트레드밀로 훈련시키면 8일까지 가자미근과 비장근에서 VEGF 및 VEGFR1과 VEGFR2의 발현이 모두 증가한다. 그러나 8일 이후부터 24일까지는 그 발현량들이 감소하여 다시 정상 수준으로 돌아간다[ 103]. 인간에 있어 운동에 의한 혈관신생 인자의 역할은 심장 또는 지방보다는 생검(biopsy)이 용이한 근육을 대상으로 그 연구결과들이 축적되어 왔다. VEGF 메신저리보핵산은 인간에 있어서도 운동 후 증가한다. 급성운동은 VEGF의 발현을 증가시킨다. 지구성 운동 선수 및 일반인에게 최대 파워의 50% 강도로 1시간 동안 자전거 운동을 시행하면 두 집단 모두 혈중 내 VEGF 단백질의 농도가 운동 직후부터 증가하기 시작해 4시간이 지나면 정상 수준으로 돌아온다[ 104]. 또한 근력운동 역시 VEGF의 발현을 증가시킨다. 한 다리만으로 무릎 신전 운동을 45분간 시행하면 근육 내 VEGF 메신저리보핵산은 통제군에 비해 178% 증가하고 이와 동시에 HIF-1 β의 메신저리보핵산은 통제군에 비하여 340% 증가한다[ 105]. 단순한 근력 운동뿐만 아니라 저산소증을 유발하기 위해 혈액의 흐름을 억제시킨 상태(blood flow restriction)에서 저강도 근력 운동을 시행하면 VEGF의 발현이 보다 증가된다. 혈류 저항을 유도하기 위해 혈압을 측정할 때 사용되는 커프(pneumatic cuffs)를 다리에 감고 약 220 mmHg의 압력을 가한 후 최대근력의 40%에 해당하는 무게로 120회의 무릎신전 운동을 시행한 20대 성인은 운동 4시간 후 근육에서의 VEGF 메신저리보핵산의 발현이 혈류의 저항 없이 운동을 시행한 군에 비하여 4배 이상 증가하였다[ 106]. 건강한 노인(71±6.5세)을 대상으로 혈류를 억제한 상황에서 보다 낮은 강도의 저항을 운동을 시행하여도 같은 결과를 보였다. 혈압을 측정할 때 사용되는 커프(pneumatic cuffs)를 다리에 감고 약 110 mmHg의 압력을 가한 후 최대근력의 20%에 해당하는 무게로 저강도 근력운동을 5세트 시행한 노인은 운동 직후 30분 후에 혈장 내 VEGF의 농도가 정상적인 혈류를 가진 다리로 운동했을 때보다 약 2배 이상 증가한다[ 107]. 이와 같이 노화는 운동에 의한 근육 내 VEGF의 발현을 억제하지는 않는 것으로 보인다. 최대산소섭취량의 65%로 8주간 유산소성 운동(4일/주, 1시간/회)을 시행한 20대 및 50-70대 여성에 있어 최대하 운동 직후 근육에서의 VEGF 발현량은 나이에 상관없이 증가하였다[ 108]. 따라서 중등도의 저산소증이 동반된 근력운동은 VEGF의 발현을 증가시킨다고 할 수 있다. 한편 고강도의 운동보다는 중강도의 운동이 VEGF의 발현을 더 증가시킨다. 건강한 성인을 대상으로 고강도의 간헐적 운동 트레이닝을(최대산소섭취량의 117-124%, 24회의 1분간 자전거 운동, 3회/주, 4주) 시행한 후 중강도 운동(최대산소섭취량의 약 60%, 60분, 자전거 운동) 및 고강도의 간헐적 운동 시(최대산소섭취량의 117%, 1분간 자전거 운동을 시행한 후 1.5분간 휴식, 24회) 근육의 VEGF 발현을 비교하면 트레이닝 후 중강도 운동 및 고강도의 간헐적 운동 모두 VEGF의 발현을 증가시키나 중강도 운동 후 VEGF의 근육 내 발현량이 고강도의 간헐적 운동보다 약 1/3 정도 더 증가하였다[ 109]. Ang1과 Ang2 역시 트레이닝을 통해 근육에서의 발현이 증가한다. 쥐를 1일당 4회씩 트레드밀로 훈련시키면 8일까지 가자미근에서 Ang1, Ang2 및 Tie2의 발현이 모두 증가한다. 그러나 8일 이후부터는 그 발현량이 감소하여 다시 정상 수준으로 돌아간다[ 103]. 인간을 대상으로 한 실험결과에서도 같은 결과를 보인다. 건강한 성인을 대상으로 45분간의 무릎 신전 운동 트레이닝을 5주간 시행하면 트레이닝 후 Ang1의 변화 없이 Ang2의 발현만이 증가하며, 무릎신전 운동을 혈류저항을 유도한 상태에서 시행하면 혈류저항 없이 트레이닝한 다리보다 Ang2의 발현이 다소 증가된다[ 110]. 말초동맥질환(peripheral arterial disease)을 가진 환자를 대상으로 60분간의 수동적 무릎신전 운동 또는 30분간의 자발적 무릎신전 운동을 시행한 결과 두 운동 모두에서 운동 후 Ang1의 변화 없이 Ang2의 발현만이 근육에서 증가하였다[ 111]. 또한 14명의 건강한 성인을 대상으로 최대산소섭취량의 약 60-68%의 강도로 자전거 운동(주당 3회, 회당 60분, 4주)을 시행한 결과, 외측광근(vastus lateralis)의 Ang1 mRNA는 변화가 없었으나 Ang2 및 Tie2의 발현이 유의하게 증가하였으며[ 112], 고강도의 간헐적 운동시(최대산소섭취량의 117%, 1분간 자전거 운동을 시행한 후 1.5분간 휴식, 24회), 운동 직후 3시간에서의 근육 Ang2 발현량이 증가한다[ 109]. 이처럼 운동 후 발생하는 Ang2는 운동에 의해 증가하는 혈관신생을 위해 기존 혈관의 안정성을 깨뜨리거나 운동 후 일시적으로 생성될 수 있는 염증성 자극을 억제하는 역할을 하는 것으로 사료된다[ 39, 40]. PDGF-B 또한 운동에 의해 증가한다. 트레이닝을 받지 않은 일반인을 대상으로 Cybex를 이용한 무릎 신전 운동을 12주간 시행하면 근육 내 PDGF-B 단백질의 발현이 증가한다[ 113]. 그러나 PDGF-B의 발현 증가가 운동 후 발생하는 기전 및 역할에 대해서는 아직 알려져 있지 않다.
3) 운동에 의한 지방 내 혈관신생 인자 변화
운동은 지방 내 혈관신생 인자의 발현을 조절하여 체내 지방량 감소를 야기한다[ 114]. 정상 식이 및 고지방 식이를 처치한 마우스를 대상으로 6주간 트레드밀을(40분/일, 12 m/분, 12°, 5일/주) 이용한 유산소성 운동을 시행하면 운동을 시행한 고지방 식이군이 운동을 하지 않은 고지방 식이군에 비하여 20% 이상 지방 크기의 감소를 보이며 지방감소에 따른 VEGF의 발현이 유의하게 증가한다[ 115]. 또한 비만 및 당뇨질환 모델인 Zucker 쥐를 이용하여 8주간 트레드밀 운동을(60분/일, 20 m/분, 5일/주) 시행한 결과, 백색지방의 VEGF 발현은 운동에 의해 유의하게 증가하였다[ 116]. 흥미로운 점은 이 두 연구에서 정상 식이를 시행한 정상 체중의 마우스는 운동에 의해 지방에서의 VEGF의 발현이 변화하지 않았다. 또한 정상체중의 마우스에 비해 고지방 식이 마우스 및 zucker 쥐의 백색지방은 VEGF 발현량이 증가한다. 이와 같은 결과는 비만에 의한 지방의 팽창은 VEGF의 발현을 증가시키고 이는 지방의 팽창에 따른 국부적인 지방 내 저산소증으로 인해 혈관신생이 필요하기 때문으로 사료된다. 지방의 VEGF는 지구성 운동능력의 손상과 관련이 있음이 보고되기도 하였다. 지방에서의 VEGF 발현을 제거하기 위해 Fabp4-cre 마우스와 VEGF floxed 마우스를 교배시킨 마우스는 지방 내 혈관의 함량이 감소하고 이와 더불어 나이가 들어감에 따라 체내 지방의 함량 감소를 동반한 체중 감소를 보인다. 지방의 VEGF를 제거한 마우스를 대상으로 2분간 10 m/분 그리고 다시 2분간 15 m/분의 속도로 유지하다가 이후 20 m/분 (10°) 속도로 최대하 운동검사를 시행하면 VEGF 제거 마우스는 통제군에 비해 운동지속 능력이 약 30% 정도 낮으나 최대 런닝 속도는 차이가 없었다[ 117]. 그러나 이 연구의 제한점은 Fabp4가 지방에서 발현되는 단백질이기는 하나 대식세포 및 혈관내피세포에서도 발현된다는 점이다. 생체 내에서 혈관신생뿐만 아니라 다양한 역할을 수행하는 대식세포에서의 VEGF의 발현 감소가 가지는 생리학적 의미를 규명하지 않으면, 위의 결과가 지방의 VEGF에 의해서만 유도되었다고 보기 어렵기 때문에 향후 adiponectin-cre 마우스를 이용하여 재검증할 필요가 있다. 최근 인간을 대상으로 운동에 의한 지방 내 혈관신생 인자의 변화를 연구한 결과가 보고되었다. 비만환자 79명을 대상으로 12주간 운동처치(3회/주, 60-75분/회, 에너지 소모량 500-600 kcal/회) 또는 초저열량 식이 및 운동처치를 병행하였을 때 두 집단에서 모두 유의한 체중감소와 더불어 복부 지방이 유의하게 감소하였다. 그러나 혈장 내 VEGF의 농도는 트레이닝 전과 후 차이가 없었으며 지방 생체검사(biopsy)를 통해 유전자의 발현을 조사한 결과 지방 내 VEGF의 발현에도 차이가 없었다. 또한 운동 전과 비교하여 운동 후 혈장 Ang1의 농도는 유의하게 감소하였으나 지방조직에서의 Ang1의 유전자 발현은 역시 차이가 없었다[ 118]. 이와 같이 운동에 의한 지방에서의 혈관신생 인자의 변화는 동물실험과 인간을 대상으로한 실험결과에서 일치하지 않는 결과들을 보이고 있다. 이는 아마도 인간을 대상으로 한 연구가 극히 제한적이고 동물과 달리 생물학적 조건이 같은 대상자를 상대로 운동처치를 하는 것이 어렵기 때문으로 사료된다. 따라서 향후 보다 많은 참여자를 대상으로 다양한 운동조건에서 혈관신생 인자의 변화를 관찰할 필요가 있다.
4) 운동에 의한 혈관신생 인자 발현 기전
운동에 의한 혈관신생 기전은 2가지 요소에 의해 조절되는 것으로 알려져 있다. 운동 중 발행하는 폐의 가스 교환의 기능저하로 체내에 저산소증이 발생하면[ 119], 생체 내 hypoxia-inducible factor (HIF-1α) 전사인자의 발현이 증가하고, 증가된 HIF-1α는 VEGF의 발현을 증가시킨다[ 120]. 중강도 신체활동에 주당 3.5시간 참여하는 건강한 성인 24명의 근육에서도 HIF-1의 증가는 VEGF의 발현량과 유의한 상관관계를 보였다[ 121]. 따라서 운동에 의해 직접적으로 VEGF를 발현하는 기전은 저산소증으로 간주되어 왔으나, VEGF를 유도할 수준의 저산소증이 발생할 경우 운동을 지속하기 어렵고 또한 근육에서만 HIF-1α를 제거한 마우스는 예상과 달리 근육 내 모세혈관의 수가 월등히 증가하고 또한 6주간 트레드밀을 이용한 트레이닝(30분/회, 5일/주, 18 m/min) 후 지구성 운동 검사를 시행하였을 때 정상 마우스와 비교하여 운동기능에는 전혀 결합을 보이지 않았다[ 122]. 따라서 운동에 의한 혈관신생은 저산소증에 의한 HIF-1α만으로 모두 설명하기는 어려웠다. PPAR coactivator (PGC)-1α (PGC-1 α)는 산화적 대사에 관여하는 전사 공활성화 인자(transcriptional coactivator)이다. 수영운동을 3시간 수행한 쥐 또는 무릎신전 운동을 시행한 인간의 근육 모두에서 PGC-1 α의 발현이 증가한다[ 123, 124]. 흥미로운 점은 근육에서 PGC-1 α를 제거한 마우스는 정상적인 마우스와 근육 내 혈관 수의 차이를 보이지 않으나 자발적 휠 런닝 운동 후 정상 마우스와 비교하면 혈관 수의 증가를 보이지 않는다. 이는 운동 중 증가되는 혈장 노르에피네프린이 β-adrenergic receptors를 활성화시켜 PGC-1 α의 발현이 증가되고[ 125], 증가된 PGC-1 α가 근육 내 VEGF, PDGF-B 및 Ang2의 발현을 증가시키기 때문이다[ 126] ( Fig. 1). 전력으로 자전거운동(체중의 75% 부하)을 30초간 시행한 후 3분간 휴식을 취하는 인터벌 운동을 6회 시행하거나 또는 최대심박수의 80%의 강도로 334 kJ의 자전거 운동 후 3분간 휴식을 취하고 다시 전력으로 자전거운동(최대심박수의 78.9%)을 6회 시행하며, 운동 후 2-3시간에 근육 내 PGC-1 α 및 VEGF의 발현량이 증가한다. 그러나 최대산소섭취량의 60%로 60분간 자전거를 시행한 피험자의 근육에서는 이와 같은 현상이 발견되지 않았다[ 127]. 또 다른 연구에서는 최대산소섭취량의 약 70%의 강도로 30분간 자전거운동을 시행한 건강한 성인은 운동 후 PGC-1 α 및 VEGF의 발현량이 증가하였다[ 128]. 이처럼 운동에 의해 생성되는 혈관신생인자의 발현은 적어도 근육에서는 PGC-1 α에 의해 중재되는 VEGF, Ang2 그리고 PDGF-B에 의해 조절되나, 심장 및 지방에서의 기전은 아직 잘 알려져 있지 않다.
결 론
생체조직의 항상성 및 조직의 생존에 밀접한 관련을 갖는 혈관은 혈관신생 인자의 발현에 의해 정교하게 그 기능이 조절된다. 혈관기능의 이상은 관상동맥질환의 주된 원인이며 또한 혈관의 감소는 근육에서 근육세포의 괴사를 초래하고 지방 내 저산소증을 유발하여 지방의 염증발현을 가속화시킨다. 이와 동시에 지방의 혈관 감소는 지방 내 지질 축적을 억제하여 근육 또는 간과 같은 다른 조직으로 지질의 축적이 재분배되는 현상을 야기하여 결과적으로 당뇨병을 비롯한 지질대사 이상을 초래한다. 혈관신생에 관여하는 대표적인 인자인 VEGF, Ang 그리고 PDGF 등은 단순히 각각의 인자들이 조직 내에서 독립적으로 혈관신생을 조절한다기보다는 서로가 서로의 발현에 영향을 미치면서 혈관의 생성 및 성숙을 효율적으로 조절한다. 운동은 이와 같은 혈관신생 인자의 발현에 가장 완벽한 생리적 자극원이다 ( Table 1). 운동을 통해 그 발현이 증가되는 VEGF, Ang 그리고 PDGF 등은 건강한 혈관의 신생을 통해 심장질환의 발생, 근위축 그리고 성인병의 가장 중요한 위험인자인 비만을 억제함으로써 건강 증진에 이바지한다. 또한 운동은 혈관의 신생과 성숙에 필수적인 유전자의 발현을 모두 증가시키기 때문에 환자에 있어 특정 단백질만으로 혈관신생을 유도하였을 때 생길 수 있는 혈관의 누수(leakage) 또는 그 기능을 수행할 수 없는 불안정한 혈관신생 등의 문제를 극복할 수 있는 가장 좋은 치료 수단이다. 현재까지의 운동과 관련된 혈관신생 인자들의 발현 변화는 동물실험을 통해 연구들이 진행되어 왔으나, 그 관련 기전들에 대해서는 극히 일부만이 알려져 있다. 또한 VEGF를 제외한 Ang2와 PDGF-B 및 그 수용체들의 변화에 운동이 미치는 영향에 대해서는 인간을 대상으로 한 보다 많은 연구가 필요하다. 따라서, 향후 운동과 관련된 혈관신생 인자들의 연구는 생물학적 그리고 병리생리학적 관점에서 관련 유전자를 발현시키는 전사인자의 규명 및 일반인과 혈관 질환자를 대상으로 1회성 운동, 간헐적 운동, 웨이트 트레이닝 및 장기간의 유산소성 운동 등에 의한 치료적 효과에 있어 Ang2 및 PDGF-B의 역할을 규명함으로써 운동에 의한 혈관신생 과정의 관련기전을 이해하는 데 도움이 되는 연구들이 진행되어야 할 것으로 사료된다.
Fig. 1.
Fig. 1.Exercise induces angiogenesis by PGC-1a and HIF1 mediated VEGF, ANG2 and PDGF-B. 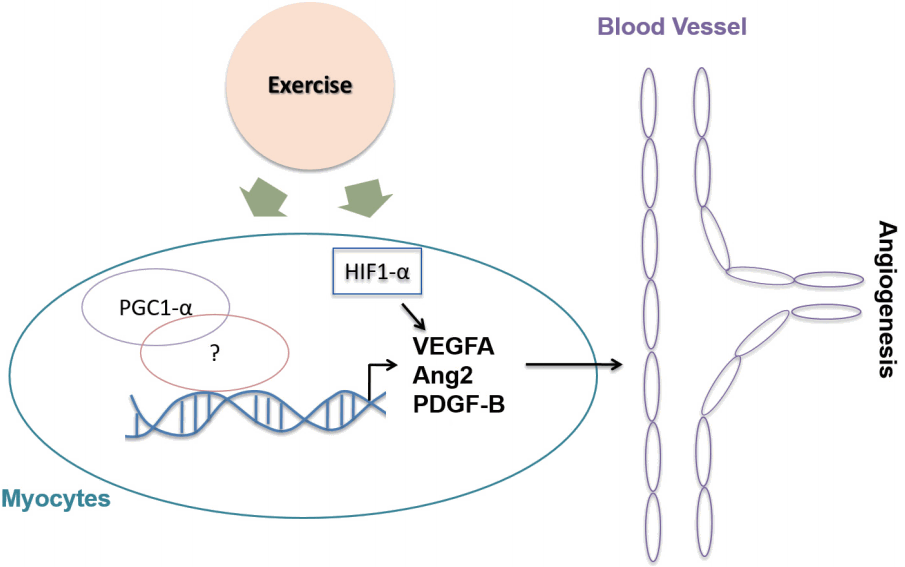
Table 1.
Exercise alters the expression of VEGF, Ang and PDGF-B in heart, skeletal muscle and adipose tissue
|
Animal or Subject |
Exercise Protocol |
Target Tissue |
Results |
Reference |
|
Pig |
Endurance exercise |
Heart |
Capillary vessel↑ |
[85] |
|
Dog |
Endurance exercise |
Heart |
Capillary vessel↑ |
[86] |
|
Rat |
Swimming Exercise for 15 days |
Heart |
Capillary vessel↑ |
[87] |
|
Rat treated with streptozotocin |
Treadmill exercise |
Heart |
VEGF mRNA↑ |
[88] |
|
Coronary artery disease patients |
Exercise test |
Plasma |
VEGF concentration↑ |
[92] |
|
EPC number↑ |
|
Healthy adults |
1,500 m running exercise |
Plasma |
EPC number↑ |
[93] |
|
VEGF concentration↔ |
|
Healthy adults |
30 min Running (82% VO2max) |
Plasma |
EPC number↑ |
[94] |
|
30 min Running (62% VO2max) |
EPC number↑ |
|
10 min Running (62% VO2max) |
EPC number↔ |
|
Trained healthy adults |
Muscle endurance exercise with weight training |
Plasma |
VEGF concentration↑ |
[95] |
|
EPC number↑ |
|
Coronary artery disease patients |
Intermittent mild exercise |
Plasma |
Ang2 concentration↑ |
[97] |
|
Rat |
Electrical Stimulus/3-56 days |
Muscle |
VEGF expression↑ |
[101] |
|
Healthy adults |
Single bout of treadmill running (1 hr/session, 15-20 m/min, 10°) |
Gastrocnemius |
VEGF expression↑ |
[102] |
|
Rat |
Treadmill running (4 sets/day, 20-25 m/min, 24 days) |
Gastrocnemius |
Up to day 8: mRNA of VEGF, VEGFR1, VEGFR2↑ |
[103] |
|
Soleus |
Day 8-24: mRNA of VEGF, VEGFR1, VEGFR2↓ |
|
Trained & untrained healthy adults |
Cycle ergometer (50% of maximum power, 1 hr) |
Plasma |
VEGF concentration↑ |
[104] |
|
Healthy adults |
One-leg knee extension exercise (45 min) |
Skeletal muscle |
VEGF mRNA↑ |
[105] |
|
Healthy adults |
Leg knee extension exercise with blood flow restriction (BFR) (40% of 1 RM, 120 repetition with 1 min rest) |
Skeletal muscle |
VEGF mRNA↑ |
[106] |
|
Healthy elderly person |
Leg knee extension exercise with BFR (20% of 1 RM with 30 sex rest, 5 sets) |
Plasma |
VEGF concentration↑ |
[107] |
|
Age of twenties & sixties women |
Cycle ergometer (65% VO2max, 4 d/wk, 1 hr/day, 8 wk) |
Vastus lateralis |
VEGF mRNA after submaximal exercise↑ |
[108] |
|
Healthy adults |
24 repetition of 1min cycle ergometer training (117-124% VO2max, 3 d/wk, 4 wk) then |
Vastus lateralis |
|
[109] |
|
60 min of cycle ergometer (60% VO2max) or 24 repetition of 1 min cycle ergometer |
VEGF mRNA↑ |
|
VEGF mRNA↑ |
|
Rat |
Treadmill running (4 sets/day, 20-25 m/min, 24 days) |
Gastrocnemius |
Up to day 8: mRNA of Ang1, Ang2, Tie2↑ |
[103] |
|
Soleus |
Day 8-24: mRNA of Ang1, Ang2, Tie2↓ |
|
Healthy adults |
One-leg knee extension exercise with BFR (45 min, highest tolerable workload) |
Vastus lateralis |
Ang2 mRNA↑ |
[110] |
|
Tie2 mRNA↑ |
|
Peripheral artery disease patients |
Passive knee extension exercise with BFR |
Vastus lateralis |
Ang2 mRNA↑ |
[111] |
|
Healthy adults |
Cycle ergometer (60-68% VO2max, 3d/wk, 60 m/session, 4 wk) |
Vastus lateralis |
Ang2 mRNA↑ |
[112] |
|
Tie2 mRNA↑ |
|
Healthy adults |
24 repetition of 1 min cycle ergometer training (117-124% VO2max, 3 d/wk, 4 wk) then |
Vastus lateralis |
Ang2 mRNA↑ |
[109] |
|
60 min of cycle ergometer (60% VO2max) or 24 repetition of 1 min cycle ergometer |
|
Healthy adults |
Knee extension exercise with Cybex for 12 wk |
Skeletal muscle |
PDGF-B protein↑ |
[113] |
|
Mouse |
HFD & treadmill exercise training (12 m/min, 40 m/session, 12°, 5 d/wk) |
White adipose tissue (WAT) |
VEGF mRNA↑ |
[115] |
|
Obese patient |
Aerobic exercise training (500-600 kcal/session, 60-75 m/session, 3 d/wk) |
WAT |
VEGF mRNA & Ang1 mRNA↔ |
[118] |
|
Plasma |
Concentration of VEGF↔& Ang1↓ |
REFERENCES
1. Bernardo BC, McMullen JR. Molecular aspects of exercise-induced cardiac remodeling. Cardiol clin. 2016;34(4):515-30.   2. Haas TL, Nwadozi E. Regulation of skeletal muscle capillary growth in exercise and disease. Appl Physiol Nutr Metab. 2015;40(12):1221-32.   3. Thompson D, Karpe F, Lafontan M, Frayn K. Physical activity and exercise in the regulation of human adipose tissue physiology. Physiol Rev. 2012;92(1):157-91.   4. Senger DR, Galli SJ, Dvorak AM, Perruzzi CA, Harvey VS, et al. Tumor cells secrete a vascular permeability factor that promotes accumulation of ascites fluid. Science. 1983;219(4587):983-5.   5. Leung DW, Cachianes G, Kuang WJ, Goeddel DV, Ferrara N. Vascular endothelial growth factor is a secreted angiogenic mitogen. Science. 1989;246(4935):1306-9.   6. Saharinen P, Eklund L, Pulkki K, Bono P, Alitalo K. VEGF and angiopoietin signaling in tumor angiogenesis and metastasis. Trends Mol Med. 2011;17(7):347-62.   7. Kroll J, Waltenberger J. The vascular endothelial growth factor receptor KDR activates multiple signal transduction pathways in porcine aortic endothelial cells. J Biol Chem. 1997;272(51):32521-7.   12. Gerber HP, Hillan KJ, Ryan AM, Kowalski J, Keller GA, et al. VEGF is required for growth and survival in neonatal mice. Development. 1999;126(6):1149-59.  13. Dumont DJ, Fong GH, Puri MC, Gradwohl G, Alitalo K, et al. Vascularization of the mouse embryo: a study of flk-1, tek, tie, and vascular endothelial growth factor expression during development. Dev Dyn. 1995;203(1):80-92.   17. Davis S, Aldrich TH, Jones PF, Acheson A, Compton DL, et al. Isolation of angiopoietin-1, a ligand for the TIE2 receptor, by secretiontrap expression cloning. Cell. 1996;87(7):1161-9.   18. Suri C, Jones PF, Patan S, Bartunkova S, Maisonpierre PC, et al. Requisite role of angiopoietin-1, a ligand for the TIE2 receptor, during embryonic angiogenesis. Cell. 1996;87(7):1171-80.   20. De Palma M, Venneri MA, Galli R, Sergi Sergi L, Politi LS, et al. Tie2 identifies a hematopoietic lineage of proangiogenic monocytes required for tumor vessel formation and a mesenchymal population of pericyte progenitors. Cancer Cell. 2005;8(3):211-26.   22. Takakura N, Huang XL, Naruse T, Hamaguchi I, Dumont DJ, et al. Critical role of the TIE2 endothelial cell receptor in the development of definitive hematopoiesis. Immunity. 1998;9(5):677-86.   23. Papapetropoulos A, Fulton D, Mahboubi K, Kalb RG, O’Connor DS, et al. Angiopoietin-1 inhibits endothelial cell apoptosis via the Akt/survivin pathway. J Biol Chem. 2000;275(13):9102-5.   24. DeBusk LM, Hallahan D, ELin PC. Akt is a major angiogenic mediator downstream of the Ang1/Tie2 signaling pathway. Exp Cell Res. 2004;298(1):167-77.   25. Gavard J, Patel V, Gutkind JS. Angiopoietin-1 prevents VEGF-induced endothelial permeability by sequestering Src through mDia. Dev Cell. 2008;14(1):25-36.   26. Dallabrida SM, Ismail N, Oberle JR, Himes BE, Rupnick MA. Angiopoietin-1 promotes cardiac and skeletal myocyte survival through integrins. Circ Res. 2005;96(4):e8-24.   27. Hughes DP, Marron MB, Brindle NP. The antiinflammatory endothelial tyrosine kinase Tie2 interacts with a novel nuclear factorkappaB inhibitor ABIN-2. Circ Res. 2003;92(6):630-6.   28. Kim I, Moon SO, Park SK, Chae SW, Koh GY. Angiopoietin-1 reduces VEGF-stimulated leukocyte adhesion to endothelial cells by reducing ICAM-1, VCAM-1, and E-selectin expression. Circ Res. 2001;89(6):477-9.   29. Kim I, Ryu YS, Kwak HJ, Ahn SY, Oh JL, et al. EphB ligand, ephrinB2, suppresses the VEGF- and angiopoietin 1-induced Ras/mitogen-activated protein kinase pathway in venous endothelial cells. FASEB J. 2002;16(9):1126-8.   31. Cho CH, Kim KE, Byun J, Jang HS, Kim DK, et al. Long-term and sustained COMP-Ang1 induces long-lasting vascular enlargement and enhanced blood flow. Circ Res. 2005;97(1):86-94.   32. Suri C, McClain J, Thurston G, McDonald DM, Zhou H, et al. Increased vascularization in mice overexpressing angiopoietin-1. Science. 1998;282(5388):468-71.   33. Chae JK, Kim I, Lim ST, Chung MJ, Kim WH, et al. Coadministration of angiopoietin-1 and vascular endothelial growth factor enhances collateral vascularization. Arterioscler Thromb Vasc Biol. 2000;20(12):2573-8.   34. Smith AH, Kuliszewski MA, Liao C, Rudenko D, Stewart DJ, et al. Sustained improvement in perfusion and flow reserve after temporally separated delivery of vascular endothelial growth factor and angiopoietin-1 plasmid deoxyribonucleic acid. J Am Coll Cardiol. 2012;59(14):1320-8.   35. Shin HY, Lee YJ, Kim HJ, Park CK, Kim JH, et al. Protective role of COMP-Ang1 in ischemic rat brain. J Neurosci Res. 2010;88(5):1052-63.   36. Park BH, Jang KY, Kim KH, Song KH, Lee SY, et al. COMP-Angiopoietin-1 ameliorates surgery-induced ischemic necrosis of the femoral head in rats. Bone. 2009;44(5):886-92.   37. Jung YJ, Kim DH, Lee AS, Lee S, Kang KP, et al. Peritubular capillary preservation with COMP-angiopoietin-1 decreases ischemiareperfusion-induced acute kidney injury. American journal of physiology. AM J Physiol Renal Physiol. 2009;297(4):F952-60.   38. Maisonpierre PC, Suri C, Jones PF, Bartunkova S, Wiegand SJ, et al. Angiopoietin-2, a natural antagonist for Tie2 that disrupts in vivo angiogenesis. Science. 1997;277(5322):55-60.   40. Gale NW, Thurston G, Hackett SF, Renard R, Wang Q, et al. Angiopoietin-2 is required for postnatal angiogenesis and lymphatic patterning, and only the latter role is rescued by Angiopoietin-1. Dev Cell. 2002;3(3):411-23.   41. Oh H, Takagi H, Suzuma K, Otani A, Matsumura M, et al. Hypoxia and vascular endothelial growth factor selectively up-regulate angiopoietin-2 in bovine microvascular endothelial cells. J Biol Chem. 1999;274(22):15732-9.   43. Li L, Qian L, Yu ZQ. Serum angiopoietin-2 is associated with angiopathy in type 2 diabetes mellitus. J Diabetes Complications. 2015;29(4):568-71.   45. Magnusson PU, Looman C, Ahgren A, Wu Y, Claesson-Welsh L, et al. Platelet-derived growth factor receptor-beta constitutive activity promotes angiogenesis in vivo and in vitro. Arterioscler Thromb Vasc Biol. 2007;27(10):2142-9.   47. Uutela M, Lauren J, Bergsten E, Li X, Horelli-Kuitunen N, et al. Chromosomal location, exon structure, and vascular expression patterns of the human PDGFC and PDGFD genes. Circulation. 2001;103(18):2242-7.   48. Shih AH, Holland EC. Platelet-derived growth factor (PDGF) and glial tumorigenesis. Cancer Lett. 2006;232(2):139-47.   49. Leveen P, Pekny M, Gebre-Medhin S, Swolin B, Larsson E, et al. Mice deficient for PDGF B show renal, cardiovascular, and hematological abnormalities. Genes Dev. 1994;8(16):1875-87.   50. Soriano P. Abnormal kidney development and hematological disorders in PDGF beta-receptor mutant mice. Genes Dev. 1994;8(16):1888-96.   52. Hellstrom M, Kalen M, Lindahl P, Abramsson A, Betsholtz C. Role of PDGF-B and PDGFR-beta in recruitment of vascular smooth muscle cells and pericytes during embryonic blood vessel formation in the mouse. Development. 1999;126(14):3047-55.  53. Lindahl P, Bostrom H, Karlsson L, Hellstrom M, Kalen M, et al. Role of platelet-derived growth factors in angiogenesis and alveogenesis. Curr Top Pathol. 1999;93:27-33.   59. Volz KS, Jacobs AH, Chen HI, Poduri A, McKay AS, et al. Pericytes are progenitors for coronary artery smooth muscle. Elife. 2015;4.   60. Boon RA, Leyen TA, Fontijn RD, Fledderus JO, Baggen JM, et al. KLF2-induced actin shear fibers control both alignment to flow and JNK signaling in vascular endothelium. Blood. 2010;115(12):2533-42.   61. Wang L, Luo JY, Li B, Tian XY, Chen LJ, et al. Integrin-YAP/TAZJNK cascade mediates atheroprotective effect of unidirectional shear flow. Nature. 2016.
62. Pircher A, Treps L, Bodrug N, Carmeliet P. Endothelial cell metabolism: A novel player in atherosclerosis? Basic principles and therapeutic opportunities. Atherosclerosis. 2016;253:247-57.   65. Viswambharan H, Yuldasheva NY, Sengupta A, Imrie H, Gage MC, et al. Selective enhancement of insulin sensitivity in the endothelium in vivo reveals a novel proatherosclerotic signaling loop. Circ Res. 2017;120(5):784-98.   66. Anderson JE. The satellite cell as a companion in skeletal muscle plasticity: currency, conveyance, clue, connector and colander. J Exp Biol. 2006;209(Pt 12):2276-92.   68. Tang K, Breen EC, Gerber HP, Ferrara NM, Wagner PD. Capillary regression in vascular endothelial growth factor-deficient skeletal muscle. Physiol Genomics. 2004;18(1):63-9.   69. Ameln H, Gustafsson T, Sundberg CJ, Okamoto K, Jansson E, et al. Physiological activation of hypoxia inducible factor-1 in human skeletal muscle. FASEB J. 2005;19(8):1009-11.   70. Deveci D, Marshall JM, Egginton S. Relationship between capillary angiogenesis, fiber type, and fiber size in chronic systemic hypoxia. Am J Physiol Heart Circ Physiol. 2001;281(1):H241-52.   71. Deveci D, Marshall JM, Egginton S. Chronic hypoxia induces prolonged angiogenesis in skeletal muscles of rat. Exp Physiol. 2002;87(3):287-91.   75. Pinol-Jurado P, Gallardo E, de Luna N, Suarez-Calvet X, Sanchez-Riera C, et al. Platelet-Derived Growth Factor BB Influences Muscle Regeneration in Duchenne Muscle Dystrophy. Am J Pathol. 2017;187(8):1814-27.   76. Yablonka-Reuveni Z, Seifert RA. Proliferation of chicken myoblasts is regulated by specific isoforms of platelet-derived growth factor: evidence for differences between myoblasts from mid and late stages of embryogenesis. Dev Biol. 1993;156(2):307-18.   77. Yuasa T, Kakuhata R, Kishi K, Obata T, Shinohara Y, et al. Plateletderived growth factor stimulates glucose transport in skeletal muscles of transgenic mice specifically expressing platelet-derived growth factor receptor in the muscle, but it does not affect blood glucose levels. Diabetes. 2004;53(11):2776-86.   78. Cho CH, Koh YJ, Han J, Sung HK, Lee HJ, et al. Angiogenic role of LYVE-1-positive macrophages in adipose tissue. Circ Res. 2007;100(4):e47-57.   80. Sung HK, Doh KO, Son JE, Park JG, Bae Y, et al. Adipose vascular endothelial growth factor regulates metabolic homeostasis through angiogenesis. Cell Metab. 2013;17(1):61-72.   81. Dallabrida SM, Zurakowski D, Shih SC, Smith LE, Folkman J, et al. Adipose tissue growth and regression are regulated by angiopoietin-1. Biochem Biophys Res Commun. 2003;311(3):563-71.   82. An YA, Sun K, Joffin N, Zhang F, Deng Y, et al. Angiopoietin-2 in white adipose tissue improves metabolic homeostasis through enhanced angiogenesis. Elife. 2017;6.   83. Onogi Y, Wada T, Kamiya C, Inata K, Matsuzawa T, et al. PDGFRbeta Regulates Adipose Tissue Expansion and Glucose Metabolism via Vascular Remodeling in Diet-Induced Obesity. Diabetes. 2017;66(4):1008-21.   84. White FC, Bloor CM, McKirnan MDCarroll SM. Exercise training in swine promotes growth of arteriolar bed and capillary angiogenesis in heart. J Appl Physiol. 1998;85(3):1160-8.   85. Laughlin MH, Tomanek RJ. Myocardial capillarity and maximal capillary diffusion capacity in exercise-trained dogs. J Appl Physiol. 1987;63(4):1481-6.   86. Laughlin MH, Overholser KA, Bhatte MJ. Exercise training increases coronary transport reserve in miniature swine. J Appl Physiol. 1989;67(3):1140-9.   87. Efthimiadou A, Asimakopoulos B, Nikolettos N, Giatromanolaki A, Sivridis E, et al. The angiogenetic effect of intramuscular administration of VEGF on muscle. In Vivo. 2004;18(6):825-9.  89. Sarto P, Balducci E, Balconi G, Fiordaliso F, Merlo L, et al. Effects of exercise training on endothelial progenitor cells in patients with chronic heart failure. J Card Fail. 2007;13(9):701-8.   91. Shirreffs JH. A lesson on stress. Health Educ. 1977;8(3):41-2.
92. Adams V, Lenk K, Linke A, Lenz D, Erbs S, et al. Increase of circulating endothelial progenitor cells in patients with coronary artery disease after exercise-induced ischemia. Arterioscler Thromb Vasc Biol. 2004;24(4):684-90.   93. Bonsignore MR, Morici G, Riccioni R, Huertas A, Petrucci E, et al. Hemopoietic and angiogenetic progenitors in healthy athletes: different responses to endurance and maximal exercise. J Appl Physiol. 2010;109(1):60-7.   94. Laufs U, Urhausen A, Werner N, Scharhag J, Heitz A, et al. Running exercise of different duration and intensity: effect on endothelial progenitor cells in healthy subjects. Eur J Cardiovasc Prev Rehabil. 2005;12(4):407-14.   95. Ross MD, Wekesa AL, Phelan JP, Harrison M. Resistance exercise increases endothelial progenitor cells and angiogenic factors. Med Sci Sports Exerc. 2014;46(1):16-23.   96. Lee KW, Lip GYBlann AD. Plasma angiopoietin-1, angiopoietin-2, angiopoietin receptor tie-2, and vascular endothelial growth factor levels in acute coronary syndromes. Circulation. 2004;110(16):2355-60.   97. Larouche JF, Yu C, Luo X, Farhat N, Guiraud T, et al. Acute High-Intensity Intermittent Aerobic Exercise Reduces Plasma Angiopoietin-Like 2 in Patients With Coronary Artery Disease. Can J Cardiol. 2015;31(10):1232-9.   98. Gallini R, Lindblom P, Bondjers C, Betsholtz C, Andrae J. PDGF-A and PDGF-B induces cardiac fibrosis in transgenic mice. Exp Cell Res. 2016;349(2):282-90.   99. Nurminskaya M, Beazley KE, Smith EP, Belkin AM. Transglutaminase 2 promotes PDGF-mediated activation of PDGFR/Akt1 and beta-catenin signaling in vascular smooth muscle cells and supports neointima formation. J Vasc Res. 2014;51(6):418-28.   100. Adair TH, Gay WJ, Montani JP. Growth regulation of the vascular system: evidence for a metabolic hypothesis. Am J Physiol. 1990;259(3 Pt 2):R393-404.   101. Annex BH, Torgan CE, Lin P, Taylor DA, Thompson MA, et al. Induction and maintenance of increased VEGF protein by chronic motor nerve stimulation in skeletal muscle. Am J Physiol. 1998;274(3 Pt 2):H860-7.   102. Breen EC, Johnson EC, Wagner H, Tseng HM, Sung LA, et al. Angiogenic growth factor mRNA responses in muscle to a single bout of exercise. J Appl Physiol. 1996;81(1):355-61.   103. Lloyd PG, Prior BM, Yang HT, Terjung RL. Angiogenic growth factor expression in rat skeletal muscle in response to exercise training. Am J Physiol Heart Circ Physiol. 2003;284(5):H1668-78.   104. Kraus RM, Stallings HW, Yeager RC, Gavin TP. Circulating plasma VEGF response to exercise in sedentary and endurancetrained men. J Appl Physiol. 2004;96(4):1445-50.   105. Gustafsson T, Puntschart A, Kaijser L, Jansson E, Sundberg CJ. Exercise-induced expression of angiogenesis-related transcription and growth factors in human skeletal muscle. Am J Physiol. 1999;276(2 Pt 2):H679-85.   107. Patterson SD, Leggate M, Nimmo MA, Ferguson RA. Circulating hormone and cytokine response to low-load resistance training with blood flow restriction in older men. Eur J Appl Physiol. 2013;113(3):713-9.   109. Hoier B, Passos M, Bangsbo J, Hellsten Y. Intense intermittent exercise provides weak stimulus for vascular endothelial growth factor secretion and capillary growth in skeletal muscle. Exp Physiol. 2013;98(2):585-97.   110. Gustafsson T, Rundqvist H, Norrbom J, Rullman E, Jansson E, et al. The influence of physical training on the angiopoietin and VEGF-A systems in human skeletal muscle. J Appl Physiol. 2007;103(3):1012-20.   112. Hoier B, Nordsborg N, Andersen S, Jensen L, Nybo L, et al. Proand anti-angiogenic factors in human skeletal muscle in response to acute exercise and training. J Physiol. 2012;590(3):595-606.   113. Trenerry MK, Della Gatta PA, Larsen AE, Garnham AP, Cameron-Smith D. Impact of resistance exercise training on interleukin-6 and JAK/STAT in young men. Muscle Nerve. 2011;43(3):385-92.   114. Hansen D, Dendale P, Berger J, van Loon LJ, Meeusen R. The effects of exercise training on fat-mass loss in obese patients during energy intake restriction. Sports Med. 2007;37(1):31-46.   116. Disanzo BL, You T. Effects of exercise training on indicators of adipose tissue angiogenesis and hypoxia in obese rats. Metabolism. 2014;63(4):452-5.   118. Cullberg KB, Christiansen T, Paulsen SK, Bruun JM, Pedersen SB, et al. Effect of weight loss and exercise on angiogenic factors in the circulation and in adipose tissue in obese subjects. Obesity. 2013;21(3):454-60.   119. Hopkins SR. Exercise induced arterial hypoxemia: the role of ventilation-perfusion inequality and pulmonary diffusion limitation. Adv Exp Med Biol. 2006;588:17-30.   121. Gustafsson T, Puntschart A, Sundberg CJ, Jansson E. Related expression of vascular endothelial growth factor and hypoxia-inducible factor-1 mRNAs in human skeletal muscle. Acta Physiol Scand. 1999;165(3):335-6.   122. Mason SD, Rundqvist H, Papandreou I, Duh R, McNulty WJ, et al. HIF-1alpha in endurance training: suppression of oxidative metabolism. Am J Physiol Regul Integr Comp Physiol. 2007;293(5):R2059-69.   123. Baar K, Wende AR, Jones TE, Marison M, Nolte LA, et al. Adaptations of skeletal muscle to exercise: rapid increase in the transcriptional coactivator PGC-1. FASEB J. 2002;16(14):1879-86.   124. Norrbom J, Sundberg CJ, Ameln H, Kraus WE, Jansson E, et al. PGC-1alpha mRNA expression is influenced by metabolic perturbation in exercising human skeletal muscle. J Appl Physiol. 2004;96(1):189-94.   125. Zouhal H, Jacob C, Delamarche P, Gratas-Delamarche A. Catecholamines and the effects of exercise, training and gender. Sports Med. 2008;38(5):401-23.   127. Skovgaard C, Brandt N, Pilegaard H, Bangsbo J. Combined speed endurance and endurance exercise amplify the exercise-induced PGC-1alpha and PDK4 mRNA response in trained human muscle. Physiol Rep. 2016;4(14).  128. Conceicao MS, Chacon-Mikahil MP, Telles GD, Libardi CA, Junior EM, et al. Attenuated PGC-1alpha Isoforms following Endurance Exercise with Blood Flow Restriction. Med Sci Sports Exerc. 2016;48(9):1699-707.  
|
|






