AbstractPURPOSEImpaired autophagy, a conserved process for the cellular energy homeostasis by degrading damaged cytosolic constituents, is an important contributor to the pathogenesis of atherosclerosis. The purpose of this study was to determine whether regular aerobic exercise can improve obesity-induced dysregulation of autophagy in mice arterial endothelial cells.
METHODSHigh-fat diet-induced obese mice were subjected to the treadmill running for 10 weeks (15 m/min, 1 hour/day, 6 days/week). Endothelial cells were isolated from aorta by perfusing with QIAzol reagent. The mRNA and protein expressions of autophagy-related genes were investigated by qRT-PCR and western-blot respectively. Statistical analysis was performed by one-way ANOVA.
RESULTSAutophagy-related gene expressions in both levels of mRNA and protein were significantly decreased in vascular endothelial cells and arterial vessels of obese mice. However, these phenomena have been partly reversed by the regular treatment of treadmill exercise for 10 weeks. Furthermore, eNOS downregulation induced by the obesity was also improved by the regular aerobic exercise, representing enhanced endothelial function.
서 론인슐린 저항성, 제2형 당뇨와 같은 대사성 질환은 에너지 섭취의 과도한 증가와 에너지 소비의 감소로 인한 체내 에너지 불균형 상태, 즉 비만에 의해 그 발병률이 증가하는 것으로 알려져 있다[1,2]. 혈관 내피세포(vascular endothelial cells)에서 발생하는 산화질소(nitric oxide, NO)는 유산소성 운동에 의해 생성이 증가하는 강력한 혈관 확장 물질로서, 동맥을 이완하여 혈압을 정상적으로 유지하고, 주요 장기 및 기관으로 향하는 혈액 흐름의 항상성을 유지하는 등, 혈관 건강의 유지와 개선을 위한 필수적인 역할을 담당한다[3]. 따라서 산화질소 합성효소(endothelial nitric oxide synthase, eNOS)의 활동성 저하와 그로 인한 NO 생체이용률 저하는 혈관 기능의 손상과 각종 심혈관 질환을 유발하는 직접적인 원인이 된다[4,5]. 서구화된 식습관과 고열량, 고지방 식이 및 운동 부족으로 인한 비만과 혈중 콜레스테롤의 증가는 이러한 혈관 내피세포의 NO 생산 기능을 저하시키고, 산화 스트레스와 염증반응을 증가시킴으로써 혈관 기능의 감소를 유발하고 동맥 경화와 같은 각종 심혈관 질환의 유병을 증가시킨다는 사실은 수없이 많은 선행연구들에 의해 밝혀져 왔다[6-9]. 그럼에도 불구하고, 비만으로 인해 유발되는 혈관기능 저하에 대한 명확한 분자생물학적 기전에 대한 연구는 여전히 진행 중에 있으며, 비만에 의한 심혈관 질환 발병에 대한 고민 또한 여전히 해결되지 않은 현대인의 건강 문제로 그 중요성이 강조되고 있다.
오토파지(autophagy)란 ‘세포 내 자가소화작용’을 의미하는 용어로써, 세포 외부 환경 또는 세포 내부로부터 발생한 스트레스에 의해 손상이 일어난 세포 내 소기관(organelle)들을 분해하여[10], 차후과정에서 이를 소멸 또는 재활용함으로써 세포 내 에너지대사 반응의 항상성을 유지하는 과정을 의미한다[11,12]. Atg5, Atg6, Atg12와 같은 오토파지 관련 유전자들은 세포 내 소기관들의 손상이 발생할 경우, 자가포식소포체(autophagosome)라 하는 소낭을 형성하여 손상된 소기관들을 에워싸도록 한다[13]. 용해성의 ubiquitin-like 단백질인 LC3 (microtubule-associated protein 1A/1B-light chain 3)은 단백질 분해효소인 Atg4에 의해 변형되어 LC3I을 형성하게 되고, LC3I은 다시 Atg3과 Atg7 신호에 따라 포스파티딜에탄올라민(phosphatidylethanolamine)에 의해 LC3II로 전환된다. LC3II 단백질은 자가포식소포체가 정상적으로 성장하여 손상된 소기관들을 소낭 내부에 가두고, 차후 과정에서 자가포식소포체가 리소좀(lysosome)과 결합하여 자가포식용해소체(autophagolysosome)를 형성함으로써 손상된 세포 소기관이 소멸되도록 하는데 핵심적인 조절 기능을 담당한다[14]. 이 과정에서 p62 단백질은 LC3I의 LC3II 전환에 관여함으로써 자가포식소포체의 성숙과 손상된 소기관의 자가포식소포체 유입을 유도한다. 자가포식소포체와 리소좀이 결합하여 자가포식용해소체가 형성된 후, 손상된 세포 소기관이 소낭 내에서 최종적으로 소멸될 때 p62는 자가포식소포체와 함께 분해된다[15]. 따라서, 오토파지의 시작에 관여하는 Atg3, Atg4, Atg5, Atg6, Atg7, Atg12 등 오토파지 관련 유전자들의 발현량 증가와 오토파지의 진행에 따른 p62 소멸과 발현량 감소, LC3I의 LC3II 전환에 따른 LC3II 단백질의 축적과 상대적인 LC3I의 감소는 오토파지가 정상적으로 수행되고 있음을 의미하는 바이오 마커가 된다[16,17].
혈관 내피세포 배양 실험을 실시한 선행연구들에서는 혈관 내 오토파지 기능을 억제할 경우, 혈관 내피세포의 기능 저하와 함께 혈관 염증반응의 증가가 나타나고, NO 생성 능력의 저하를 통한 혈관 이완 기능 감소와 혈관 긴장 증가가 유발되는 등 혈관기능의 전반적인 항상성 저하가 나타나는 것으로 보고되었다[18,19]. 이러한 오토파지 기능의 손상은 세포 신호 조절 단백질의 발현 저하와 미토콘드리아의 기능 장애에도 관여하여, 세포 내 산화 스트레스의 생성을 촉진하는 것으로도 알려져 있다[20,21]. 또한 유산소 운동을 통한 혈관 전단응력의 향상은 혈관 내피세포의 eNOS 활성과 NO 생성 증가를 유발하는데, 오토파지는 이러한 운동유발 혈관 기능 항상성 향상에도 관여하는 것으로 보고되고 있어[22], 유산소 운동에 의한 혈관 오토파지 관련 단백질 발현에 대한 연구는 지속적으로 필요성이 제기되고 있다.
이상에서 살펴본 바와 같이, 비만이라는 생리적 현상은 필연적으로 혈관기능의 저하와 심혈관 질환을 유발하게 되는데, 이를 억제하고 혈관 기능의 항상성을 유지하기 위해서는 오토파지가 필수적인 기전으로 작용할 가능성이 매우 높다. 그러나 비만이 혈관 세포에서의 오토파지 기능 저하를 유발하는지에 대해서는 알려진 바가 적으며, 유산소성 운동 훈련을 통한 비만인 혈관기능 개선에 있어서 오토파지가 어떠한 역할을 담당하는지에 대한 기전연구 역시 잘 알려지지 않았다. 특히, 오토파지의 기능 변화가 혈관 내피세포가 존재하는 내막(intimal layer)과 혈관의 평활근 세포가 존재하는 중막(media) 및 외막(adventitia)층 중, 어느 조직에서 특이적으로 나타나는지에 대한 정보는 거의 전무한 실정이다.
따라서 본 연구에서는 혈관 오토파지에 대한 비만의 영향을 파악하고, 유산소 운동을 통한 비만 혈관 기능의 개선에 오토파지가 관여하는지를 규명함으로써 비만인의 심혈관 질환 예방과 개선을 위한 기초자료를 제공하는 데 그 목적이 있다.
연구 방법1. 실험동물본 연구의 실험동물은 5주령의 수컷 C57BL/6 마우스 40마리를 사용하였다. 12주간 10마리에는 일반 식이(normal chow diet: 10% 지방, 20% 단백질, 70% 탄수화물)를 처치하였고, 30마리에는 고지방 식이(high-fat chow diet: 45% 지방, 20% 단백질, 35% 탄수화물)를 처치하여 고지방 식이를 실시한 30마리에게 비만을 유발하였다[23,24]. 동물의 사육환경은 평균온도 21±2°C, 습도 50 ±5%, 주간 및 야간의 순환은 각각 12시간(주간시간 07:00-19:00)으로 유지되었으며, 물과 사료는 제한 없이 섭취하도록 공급되었다. 실험동물 40마리 중, 일반 식이를 섭취한 10마리는 통제군(Con)으로, 고지방 식이를 섭취한 30마리 중 15마리는 비만 비운동군(Ob)으로, 비만 유도 후 트레드밀 운동을 실시한 15마리는 비만 운동군(ObEx)으로 무작위 그룹 배정하였다. 본 연구를 위한 실험동물은 국제 AAALAC (association for assessment and accreditation of laboratory animal care) 인증기관인 S대학교의 동물실험윤리위원회(IACUC)의 승인(Protocol# SNU-180813-9)을 거쳐, 실험동물 관리 지침에 따라 사육되었다.
2. 트레드밀 운동 프로토콜본 연구의 전동용 트레드밀 운동에 적용된 실험동물은 C57BL6 마우스로서, 5-10 m/min의 강도로 하루 30분씩 3일간의 적응기(acclimation) 과정을 거친 후, 1-2주차에는 10 m/min 속도와 경사도 5%에서 1일 30분씩 실시하고, 3-4주차에는 12 m/min 속도와 경사도 5%에서 1일 45분씩 실시하고, 5-6주차에는 14 m/min 속도와 경사도 10%에서 1일 45분씩 실시하고, 7-10주차에는 15 m/min의 속도와 경사도 15%에서 1일 60분씩 실시하였다. 주 6회의 빈도로 총 10주간의 트레드밀 러닝 유산소 운동을 실시하였다[25,26].
3. 조직처리모든 쥐는 비만 및 10주간의 트레드밀 운동 유무에 따라 Con, Ob, ObEx 그룹으로 분류되어 그룹별 처치 후 희생되었다. 100% 산소와 혼합된 2-4%의 Isoflurane 흡입을 통해 마취된 쥐의 흉강을 열고 대동맥(aorta)을 샘플링하였다. 대동맥의 약 1/5은 mRNA 측정에 사용되었으며, 혈관의 내막층을 형성하는 내피세포와 중막 및 외막층을 형성하는 평활근세포의 분리를 위해 QIAzol lysis reagent (Qiagen) 300 μL를 인슐린 주사기를 이용하여 혈관 내부로 주입해 내피세포를 용해·분리하였다. 내피세포 용해액과 용해되지 않은 남은 부분 즉, 평활근 세포는 별도로 구분하여 각각 액화질소에 급속 냉동 후 -80°C에 저장하였다. 대동맥의 나머지는 단백질 발현량을 측정하기 위해 액화질소에 급속 냉동 후, -80°C에 저장되었다.
4. Immunoblot-80°C에 저장된 대동맥 샘플은 4°C로 냉장 보관된 RIPA 용액(10 mM Tris-HCl, 5 mM EDTA, 150 mM에 NaCl, 1% triton X-100, 0.1% SDS, 1% deoxycholate, pH 7.5)에서 균질화(homogenization)하여 용해하였다. RIPA 용액에 용해된 샘플들은 4°C에서 16,000 g로 15분간 원심분리 후, 상층액을 수집하였다. 브래드포드 단백질 에세이(bradford protein assay)를 통해 단백질의 농도를 측정 후, SDS (sodium dedocyl sulfate)를 혼합하고, PAGE (polyacrylamide gel electrophoresis) 전기영동을 실시하였다. 젤 상의 SDS-단백질 혼합물은 Immobilon-P 멤브레인으로 이동시킨 후, 화학발광(chemiluminescence) 기법을 이용하여 단백질 발현량을 관찰하였다. Atg3 (cell signaling, product no. 3415, Danvers, MA, USA), Atg5 (cell signaling, product no. 12994, Danvers, MA, USA), Atg7 (cell signaling, product no. 8558, Danvers, MA, USA), LC3II (sigma, product no. L7543, Burlington, MA, USA), p62 (novus, product no. H00008878-M01, Centennial, CO, USA) 등과 같은 오토파지 관련 유전자의 1차 항체(primary Antibody)를 이용하여 오토파지 발현량을 측정하였고, GAPDH (cell signaling, product no. 2118, Burlington, MA, USA)를 내부 대조 유전자로 활용하였다. 각각의 단백질 발현량의 수치화된 객관적 측정을 위해 Image J (NIH) 소프트웨어를 활용하였다.
5. Real-time PCR mRNA quantificationmRNA는 QIAzol 용해제를 이용하여 추출하였고, cDNA 합성은 QuantiTect 역전사 키트(QIAGEN, Germantown, MD, USA)를 이용하여 합성하였다. mRNA 발현량은 SYBR green 형광법에 의한 real-time RT-PCR 기법에 의해 측정되었다. 주기 임계값(Ct)은 하우스키핑 유전자인 18S에 의해 표준화 분석되었다. 본 연구에 사용된 프라이머 시퀀스는 Table 1과 같다.
연구결과1. 고지방 식이에 따른 마우스 체중 변화5주령의 수컷 C57BL/6 마우스를 무작위로 그룹 분류하여, Con 그룹은 일반 식이(normal chow diet: 10% 지방, 20% 단백질, 70% 탄수화물)를 처치하였고, Ob 및 ObEx 그룹은 12주간 고지방 식이(high-fat chow diet: 45% 지방, 20% 단백질, 35% 탄수화물)를 처치하여 비만을 유도하였다. 식이 처치 전 체중은 세 그룹에서 통계적 유의차가 나타나지 않았으나, 12주간의 그룹별 식이 처치 후 Ob와 ObEx 그룹의 평균 체중은 Con 그룹에 비해 유의한 증가(Ob: p =.023, ObEx: p =.030)를 나타냈다. 실험동물의 그룹별 12주간 식이 섭취에 따른 체중 변화는 Fig. 1과 같다.
2. 트레드밀 운동에 따른 비만 쥐 대동맥 오토파지 단백질 변화Ob 그룹과 ObEx 그룹의 비만유발 후, ObEx 그룹은 10주간 트레드밀 러닝을 실시하였다. Ob그룹에서는 Atg3 (p =.011), Atg5 (p =.025), Atg7 (p =.045), LC3II (p =.032)의 발현량 감소와 p62 (p =.037)의 발현량 증가가 나타나는 등 비만에 의한 오토파지 기능 저하가 나타난 반면, 10주간 트레드밀 운동을 실시한 ObEx 그룹에서는 비만에 의한 오토파지 기능 저하가 반감되는 결과(Atg3: 2.46-fold increase, Atg5: 1.89-fold increase, Atg7: 2.18-fold increase, LC3II: 4.08-fold increase, P62: 0.63-fold increase compared to Ob)가 나타났다. 오토파지 관련 단백질 발현량의 변화는 Fig. 2와 같다.
3. 동맥 내피세포 분리비만 및 유산소운동에 따른 오토파지의 기능 변화가 혈관의 내피세포에서 특이적으로 나타나는지를 조사하기 위해 대동맥의 내막층(내피세포층)과 중막+외막층(평활근세포층)을 분리하였다. 혈관 내피세포가 정확히 분리되었는지를 검증하기 위해 혈관의 평활근세포에는 존재하지 않고 내피세포에서만 식별되는 Platelet endothelial cell adhesion molecule (PECAM)의 mRNA 발현량을 측정한 결과, 내피세포에서만 관측되었다. 혈관 내피세포 분리 결과는 Fig. 3과 같다.
4. 트레드밀 운동에 따른 대동맥 오토파지 mRNA 변화고지방 식이를 통해 비만이 유발된 Ob와 ObEx 그룹 가운데, ObEx 그룹은 10주간 트레드밀 러닝을 실시하였다. Ob그룹에서는 Atg5 (p =.048), LC3II (p =.025) mRNA 발현량 감소와 p62 (p =.050) 발현량 증가가 나타나는 등 비만에 의한 오토파지 기능 저하가 나타났다. 그러나 비만유발 후 10주간의 트레드밀 운동을 실시한 ObEx 그룹에서는 비만에 의한 저하된 오토파지 기능이 회복되는 결과(Atg3: 1.67-fold increase, Atg5: 1.71-fold increase, Atg7: 1.48-fold increase, LC3B: 1.61-fold increase, P62: 0.79-fold increase compared to Ob)가 나타났다. 또한 혈관기능의 주요 바이오 마커인 eNOS mRNA 발현량이 Ob 그룹에서 유의한 감소(p =.031)가 나타난 반면 ObEx 그룹에서는 부분적인 회복(1.55-fold increase compared to Ob)이 나타났다. 오토파지 관련 유전자의 mRNA 발현량 변화는 Fig. 4와 같다.
논 의수많은 선행연구들의 결과에도 불구하고 비만에 의한 심혈관 손상과 기능 이상 문제는 여전히 해결되지 못한 문제로 남아있으며, 이를 개선하기 위한 노력과 기전연구는 여전히 계속되고 있다. 혈관 기능 항상성에 대한 오토파지의 역할에 대한 연구도 이어지고 있으나[18,22], 비만에 의한 혈관 손상 과정에 오토파지의 기능 저하가 관여하는지에 대해서는 알려진 바가 많지 않으며, 유산소성 운동을 통한 비만인 혈관기능 개선에 있어서의 오토파지 역할에 대한 기전 역시 명확하지 않다. 특히, 오토파지의 기능 변화가 혈관의 내피세포와 평활근세포층 중 어느 조직에서 특이적으로 나타나는지에 대한 정보는 거의 전무한 실정이다. 이에 본 연구에서는 비만에 의해 유발되는 혈관 기능의 저하와 유산소 운동을 통한 개선에 있어 혈관 내 오토파지의 역할을 규명하고자 하였다.
이를 검증하기 위해 본 연구에서는 C57BL6 쥐에게 고지방 식이를 처치하여 비만을 유도하고, 오토파지 관련 유전자들의 발현량을 mRNA와 단백질 수준에서 조사하였다. 본 연구에서 실시한 고지방 식이 처치는 식이 전에 비해 100% 이상의 체중 증가율을 나타내며 일반 식이 처치 그룹의 체중 증가율 25%에 비해 약 4배 이상의 체중 증가율을 나타냈다. 식이 처치 전 모든 그룹의 체중 평균에서 유의차가 나타나지 않았으나, 12주간의 그룹별 식이 처치 후 Ob와 ObEx에서 일반식이 처치 그룹 Con에 비해 4배 이상의 증가율을 나타낸 것으로(Fig. 1), 본 연구에서 실시한 고지방 식이 처치가 실험동물의 비만을 효과적으로 유발하였음을 보여주었다.
오토파지의 시작에 관여하는 Atg3, Atg4, Atg5, Atg6, Atg7, Atg12 등 오토파지 관련 유전자들의 발현량 증가와 오토파지의 진행에 따라 자가포식소포체와 함께 소멸되어 그 발현량이 저하되는 p62 단백질의 감소, 오토파지 과정에서 LC3I의 LC3II로의 전환에 의해 LC3II 단백질의 발현량 증가는 오토파지 기능의 증거가 되는데, Ob 그룹의 비만 쥐에서는 Atg3, Atg5, Atg7, LC3II 발현량 감소와 p62의 발현량 증가가 나타나는 등 오토파지 기능의 저하가 나타났다(Fig. 2). 그러나 10주간 트레드밀 운동을 실시한 ObEx 그룹의 비만 쥐에서는 오토파지 기능 저하가 둔화되었는데, 이는 규칙적이고 지속적인 유산소성 운동이 비만에 의한 혈관 오토파지 기능의 손상을 막아준 결과라고 할 수 있겠으며, 이는 유산소 운동이 노화에 따른 오토파지 기능 저하의 개선을 가져왔다는 선행연구 결과와 더불어[27,28], 운동을 통한 비만인 혈관 기능 개선에 있어서도 오토파지가 관여한다는 것을 추정해 볼 수 있겠다.
비만 쥐의 대동맥 혈관조직에서 나타난 이러한 결과와 더불어, 본 연구에서는 혈관 조직의 내피세포와 평활근세포 중 어느 곳에서 오토파지가 실질적으로 나타나는지를 탐구하고자 하였다. 이를 검증하기 위해 우선 대동맥의 내막층(내피세포층)과 중막+외막층(평활근세포층)을 분리하였는데, QIAzol lysis reagent를 인슐린 주사기를 이용하여 혈관 내부로 주입해 내막층을 용해·분리함으로써 내피세포를 획득할 수 있었고, 중막과 외막은 QIAzol에 용해되지 않으므로 평활근세포 역시 조직 상태로 샘플링할 수 있었다. 이러한 혈관 조직의 분리가 완전하게 이루어졌는지를 검증하기 위해 혈관 내피세포에서만 식별되는 PECAM mRNA 발현량을 qRT-PCR로 측정한 결과[29], 혈관 내막층 세포에서만 PECAM 발현이 관측되어 내피세포의 분리가 깨끗이 이루어졌음을 보여주었다(Fig. 3).
끝으로, Fig. 2에서 나타난 오토파지 관련 단백질 발현의 결과가 혈관 내피세포층에서 실제적으로 일어난 것인지를 확인하기 위해 용해·분리된 혈관 내막층, 즉 내피세포에서의 오토파지 관련 유전자들의 mRNA 발현량을 측정하였다. 그 결과, 비만 쥐의 내피세포에서는 오토파지 관련 유전자들의 mRNA 발현량에서 유의한 감소가 나타났으며, 10주간의 유산소 운동을 수행한 비만 쥐에서는 오토파지 관련 유전자 발현 감소가 완화된 것을 볼 수 있었다(Fig. 4). 이는 Fig. 2의 결과에서 보여주는 비만으로 인한 혈관 조직의 오토파지 기능 감소와 운동을 통한 예방이 구체적으로 혈관 내피세포에서 일어난 현상이라는 사실을 보여준 결과라 할 수 있겠다. 또한 운동을 처치한 비만 쥐는 비운동 비만 쥐에 비해 eNOS mRNA 발현량의 유의한 증가가 나타났는데, 이는 eNOS의 발현 증가를 통한 NO의 생성이 혈관 기능 향상의 대표적인 증거라는 점을 감안하였을 때[22,23], 본 연구에서는 비록 오토파지와 혈관장애의 직접적인 연관성을 보여주지는 못하였지만, 10주 운동을 통해 증가된 오토파지가 혈관장애를 개선시키는 데 부분적으로 기여할 수 있었을 것으로 추정된다.
결 론고지방 섭취를 통해 유발되는 비만은 혈관 조직의 오토파지 기능 저하를 유발하며, 이는 혈관 내피세포에서 특이적으로 일어나는 현상으로써 지속적인 유산소성 운동을 통해 부분적으로 예방될 수 있는 것으로 나타났다. 아울러, 이러한 혈관 내피세포 오토파지의 저하와 개선은 혈관 조직의 기능에도 직접적으로 관여됨을 알 수 있었다.
이러한 결과를 통해 본 연구는 비만인의 심혈관 질환 예방과 개선을 위한 약물처치의 대안으로서 유산소 운동이 효과적일 수 있음을 다시 한번 검증하였으며, 본 연구에서는 비록 운동에 의한 오토파지의 증가가 혈관장애를 개선시켜 준다는 정확한 기전이나 직접적인 인과관계를 조사하지는 못하였으나, 그 가능성을 보여준 연구로서 의미를 가질 수 있겠다.
Fig. 1.Fig. 1.High-fat diet-induced obesity in C57BL6 mice. Con group was treated with normal chow diet, while Ob and ObEx groups were treated with high-fat chow diet for 12 weeks. Con, control; Ob, obesity; ObEx, obesity-exercise. *Denotes significant difference in p<.05 compared to each group of pre-diet; † Denotes the significant difference in p<.05 compared to Con. 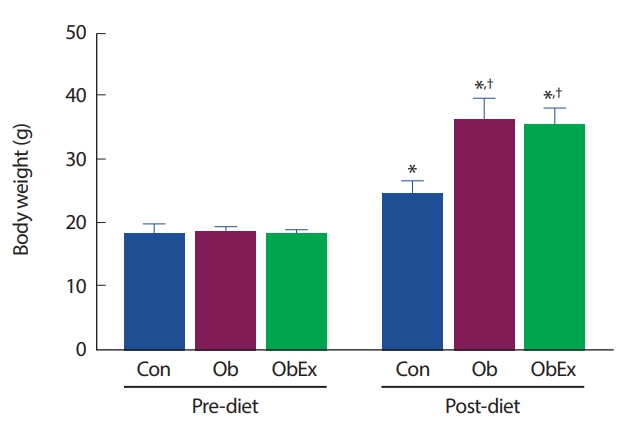
Fig. 2.Fig. 2.Effects of treadmill-running exercise on vascular autophagy-related protein expressions in C57BL6 obese mice. (A) Western blotting results from the expression levels of Atg3, Atg5, Atg7, LC3II, and p62. Protein expressions were normalized to the GAPDH expression, the internal control. Con, control; Ob, obesity; ObEx, obesity-exercise. *Denotes the significant difference in p<.05 compared to Con; †Denotes the significant difference in p<.05 compared to Ob. 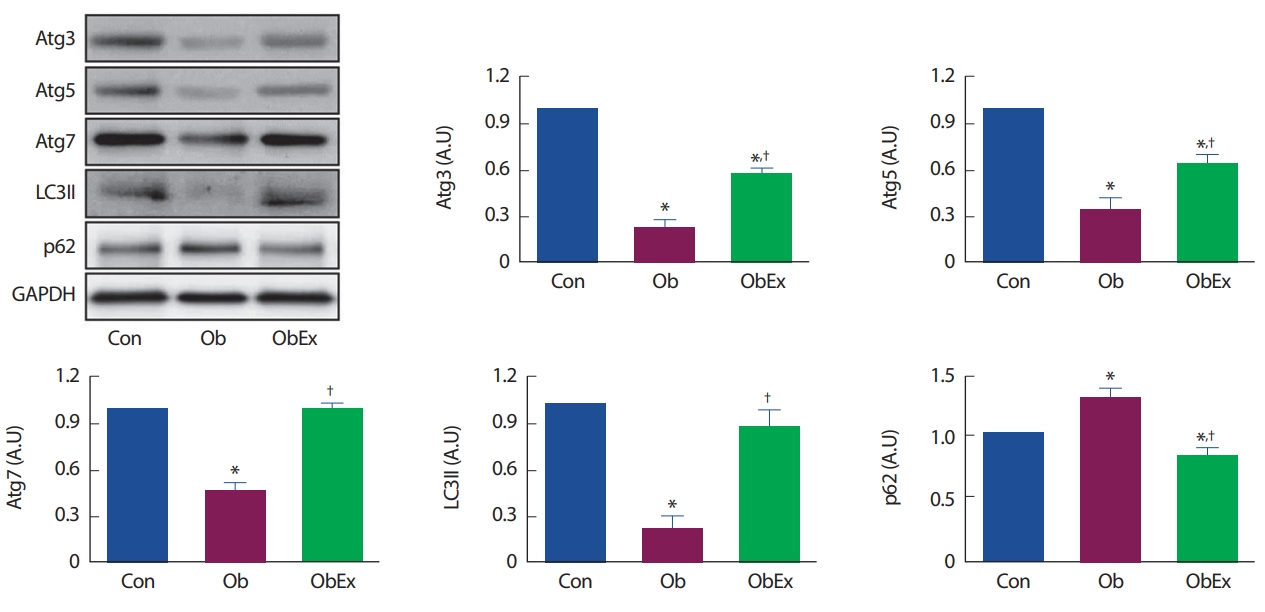
Fig. 3.Fig. 3.Relative mRNA expression of PECAM in intimal layer and media/adventitia fraction. 18S was used for the internal control. Int, intima; Med, media; Adv, adventitia. **Denotes the significant difference from Int in p<.01. 
Fig. 4.Fig. 4.Effects of treadmill-running exercise on vascular autophagy-related gene mRNA expressions in C57BL6 obese mice. mRNA expressions were normalized to the GAPDH, the internal control. Con, control; Ob, obesity; ObEx, obesity-exercise. *Denotes the significant difference in p<.05 compared to Con; †Denotes the significant difference in p<.05 compared to Ob. 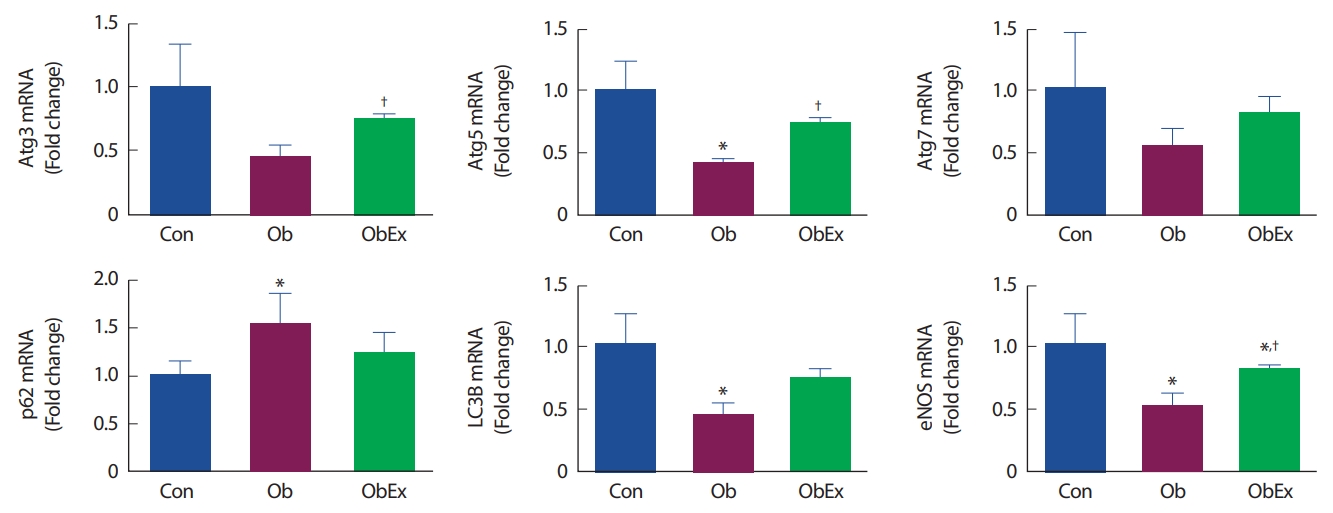
Table 1.Mouse primer sequence REFERENCES1. Fink RI, Kolterman OG, Griffin J, Olefsky JM. Mechanisms of insulin resistance in aging. J Clin Invest. 1983;71(6):1523-35.
2. Barzilai N, Huffman DM, Muzumdar RH, Bartke A. The critical role of metabolic pathways in aging. Diabetes. 2012;61(6):1315-22.
3. Donato AJ, Morgan RG, Walker AE, Lesniewski LA. Cellular and molecular biology of aging endothelial cells. J Mol Cell Cardiol. 2015;89(Pt B):122-35.
4. Marzetti E, Csiszar A, Dutta D, Balagopal G, Calvani R, et al. Role of mitochondrial dysfunction and altered autophagy in cardiovascular aging and disease: from mechanisms to therapeutics. Am J Physiol Heart Circ Physiol. 2013;305(4):H459-76.
5. Stampfli SF, Akhmedov A, Gebhard C, Lohmann C, Holy EW, et al. Aging induces endothelial dysfunction while sparing arterial thrombosis. Arterioscler Thromb Vasc Biol. 2010;30(10):1960-7.
6. Frisbee JC. Vascular dysfunction in obesity and insulin resistance. Microcirculation. 2007;14(4-5):269-71.
7. Bhatta A, Yao L, Xu Z, Toque HA, Chen J, et al. Obesity-induced vascular dysfunction and arterial stiffening requires endothelial cell arginase 1. Cardiovasc Res. 2017;113(13):1664-76.
8. Stapleton PA, James ME, Goodwill AG, Frisbee JC. Obesity and vascular dysfunction. Pathophysiology. 2008;15(2):79-89.
9. Vanhoutte PM. Obesity and vascular dysfunction: the fat-e of rich and poor. Br J Pharmacol. 2012;165(3):541-3.
11. Pallauf K, Rimbach G. Autophagy, polyphenols and healthy ageing. Ageing Res Rev. 2013;12(1):237-52.
12. Russell RC, Yuan HX, Guan KL. Autophagy regulation by nutrient signaling. Cell Res. 2014;24(1):42-57.
13. Chen Y, Klionsky DJ. The regulation of autophagy - unanswered questions. J Cell Sci. 2011;124(Pt 2):161-70.
14. Kabeya Y, Mizushima N, Ueno T, Yamamoto A, Kirisako T, et al. LC3, a mammalian homologue of yeast Apg8p, is localized in autophagosome membranes after processing. EMBO J. 2000;19(21):5720-8.
15. Bjorkoy G, Lamark T, Brech A, Outzen H, Perander M, et al. p62/SQSTM1 forms protein aggregates degraded by autophagy and has a protective effect on huntingtin-induced cell death. J Cell Biol. 2005;171(4):603-14.
16. Salabei JK, Conklin DJ. Cardiovascular autophagy: crossroads of pathology, pharmacology and toxicology. Cardiovasc Toxicol. 2013;13(3):220-9.
17. Nussenzweig SC, Verma S, Finkel T. The role of autophagy in vascular biology. Circ Res. 2015;116(3):480-8.
18. Bharath LP, Mueller R, Li Y, Ruan T, Kunz D, et al. Impairment of autophagy in endothelial cells prevents shear-stress-induced increases in nitric oxide bioavailability. Can J Physiol Pharmacol. 2014;92(7):605-12.
19. Zhou B, Li H, Liu J, Xu L, Zang W, et al. Intermittent injections of osteocalcin reverse autophagic dysfunction and endoplasmic reticulum stress resulting from diet-induced obesity in the vascular tissue via the NFkappaB-p65-dependent mechanism. Cell Cycle. 2013;12(12):1901-13.
20. Gottlieb RA, Carreira RS. Autophagy in health and disease. 5. Mitophagy as a way of life. Am J Physiol Cell Physiol. 2010;299(2):C203-10.
21. Chen F, Chen B, Xiao FQ, Wu YT, Wang RH, et al. Autophagy protects against senescence and apoptosis via the RAS-mitochondria in high-glucose-induced endothelial cells. Cell Physiol Biochem. 2014;33(4):1058-74.
22. Bharath LP, Cho JM, Park SK, Ruan T, Li Y, et al. Endothelial cell autophagy maintains shear stress-induced nitric oxide generation via glycolysis-dependent purinergic signaling to endothelial nitric oxide synthase. Arterioscler Thromb Vasc Biol. 2017;37(9):1646-56.
23. Symons JD, McMillin SL, Riehle C, Tanner J, Palionyte M, et al. Contribution of insulin and Akt1 signaling to endothelial nitric oxide synthase in the regulation of endothelial function and blood pressure. Circ Res. 2009;104(9):1085-94.
24. Zhang QJ, Holland WL, Wilson L, Tanner JM, Kearns D, et al. Ceramide mediates vascular dysfunction in diet-induced obesity by PP2A-mediated dephosphorylation of the eNOS-Akt complex. Diabetes. 2012;61(7):1848-59.
25. Sano K, Kawashima M, Ito A, Inaba T, Morimoto K, et al. Aerobic exercise increases tear secretion in type 2 diabetic mice. Invest Ophthalmol Vis Sci. 2014;55(7):4287-94.
26. Schefer V, Talan MI. Oxygen consumption in adult and AGED C57BL/6J mice during acute treadmill exercise of different intensity. Exp Gerontol. 1996;31(3):387-92.
27. He C, Sumpter R Jr, Levine B. Exercise induces autophagy in peripheral tissues and in the brain. Autophagy. 2012;8(10):1548-51.
|
|
|||||||||||||||||||||||||||||||||||||