일회성 운동이 골감소증 고령여성의 골대사성 사이토카인 생성에 미치는 영향
The Effects of a Bout Exercise on Production of Bone Metabolic Cytokines in Osteopenia Elederly Women
Article information
Trans Abstract
PURPOSE
Although overproduction of cytokines from peripheral blood mononuclear cell (PBMC) was associated with the reduction of bone mass, bone metabolic cytokines production according to exercise is still not clear. We aimed to test whether changes in production of bone metabolic cytokines after a bout exercise in osteopenia elderly women.
METHOD
Nine osteopenia elderly women (T-score -2.61±0.46; aged 67.67±3.24 years) underwent a bout exercise of 60 %VO2max (EX group) with a cycle ergometer. To clarify the changes during exercise, we designed repeated measure ANOVA as the sedentary control (CON group) to perform blood sampling without exercise. The concentrations and the mRNA expressions of cytokines were measured before, immediately after and then recovery 60 minutes after exercise. Serum Ca, Pi, Mg, and ALP were also measured at same times.
RESULTS
There were no significant changes in the concentrations of serum TNF-alpha, IL-6, IL-1beta, and INF-gamma (NS). Although the mRNA expression of most cytokines also show no significant changes (NS), only TNF-alpha mRNA expression showed significant difference between groups (p=.008). On the other hand, serum Ca showed significant difference between times (p=.002), that of EX group was significantly increased at immediately after exercise compared to baseline (p<.05), and it was decreased at recovery period (p<.01).
CONCLUSIONS
These results suggest that a bout exercise of moderate intensity might not be effect on production of bone metabolic cytokines both level of serum and mRNA from PBMC, and induced temporal hypercalcemia.
서 론
뼈는 운동기능 수행 및 칼슘 등의 무기질 저장, 조혈작용 등 다양한 기능을 한다[1]. 뼈는 체내의 대사적 변화뿐만 아니라 외부의 기계적인 자극에 민감하게 반응하여 활성 변화가 일어난다. 골량의 증가 및 감소를 일으키는 골대사의 변화에는 유전인자[2]뿐만 아니라 영양[3] 및 운동[4] 등의 환경인자가 큰 영향을 미친다. 우주비행[5] 또는 무중력상태[6]와 같은 비운동(inactivity) 환경은 골량감소를 촉진하지만, 규칙적인 적당한 운동은 골량을 유지 또는 증가시키는 것으로 알려져 있다[7]. Nuti et al. [8]의 연구에서도 성장기와 청소년기, 고령기 모두 운동양식에는 차이가 있었으나 운동에 의한 골밀도의 증가가 나타났다. 그러나 대부분의 연구가 운동의 효과로 나타나는 골밀도의 변화 정도를 보고하는 ‘현상연구’로, 그러한 변화가 어떠한 기전에 의하여 이루어지고 있는지를 밝히는 ‘기전연구’는 부족한 실정이다. 예를 들어, 운동에 의한 골량증가가 골형성 촉진으로 인하여 골밀도를 증가시키는 것인지 아니면 골흡수를 억제함으로써 골밀도가 증가하는 것인지에 대해서는 아직까지 명확하지 않으며 논란의 여지가 있다.
한편, 운동은 골세포를 직·간접적으로 자극하여 골량의 변화를 일으키며, 특히 골수에서는 골 관련세포뿐만 아니라 생체방어를 담당하는 면역계세포를 함께 생성한다. 따라서 뼈는 골대사뿐만 아니라 면역 대사를 공유하며, 내분비계 역시도 함께 네트워크를 형성하여 뼈의 골량 변화에 영향을 미친다. 세포간전달물질인 사이토카인은 각 세포의 분화와 기능을 조절하는 생리활성물질로서 다양한 세포로부터 생성되어 면역 및 조혈작용을 조절하는 것으로 알려져 있다[9]. 대부분의 사이토카인은 표적세포의 세포표면 수용체를 통하여 작용하며, 그 작용기전은 호르몬과 유사하지만 세포 수준에서 국소적으로 작용하여 부위-특이적이라 할 수 있다. 일부 사이토카인은 뼈의 경우, 조골세포 및 골수세포, 마크로파지계세포, 말초혈액 단핵세포(peripheral blood mononuclear cell, PBMC) 등으로 부터 생성되며, PBMC로부터 생성되는 사이토카인의 발현은 골수 환경을 반영하는 것으로 밝혀져 있다[10]. 이들 사이토카인은 골 관련 세포 사이에 복잡한 네트워크를 형성하여 골대사를 조절하고 있어 골대사성 사이토카인이라 불린다[11,12]. 이들 중 인터루킨(interleukin; IL)-1 [13] 및 IL-6 [14], 종양 괴사 인자(tumor necrosis factor, TNF)-α [15]는 파골세포의 분화, 증식, 활성화를 촉진하고, 강력하게 골흡수를 촉진시키는 것으로 알려져 골흡수성 사이토카인으로 보고되고 있다. 한편 바이러스 감염에 대하여 세포저항을 유도하는 다기능 사이토카인으로 알려진 인터페론(interferon, IFN)은 임파구와 단핵구로부터 유리되는 당단백질로[16], 최근의 연구에 의하면, 골형성과 골흡수에도 직간접적으로 영향을 미치는 것으로 밝혀지고 있다[17]. 인간의 T세포로부터 생산된 IFN는 파골세포의 형성을 억제하고[17], 파골세포의 분화를 저해[18]하는 것으로 알려져 있다. 즉, IL-1과 IL-6, TNF-α 등의 골흡수성 사이토카인과는 달리 IFN-γ는 골형성성 작용을 하고 있을 가능성이 시사된다. 따라서 이러한 골흡수성 사이토카인과 골형성성 사이토카인의 생성량과 유전자 발현 정도를 검토하여 골대사의 동태를 명확하게 밝히는 것은 운동의 효과를 규명하기 위해 반드시 필요한 것으로 판단된다.
따라서 본 연구에서는 골흡수 촉진 상태인 골량감소증 고령여성을 대상으로 일회성 중강도 운동을 처치하여 골대사성 사이토카인의 생성을 검토하였다. 즉, 일회성의 운동 전, 처치직후, 회복 60분 후의 혈액을 채취하여 혈청 중의 골대사성 사이토카인 및 칼슘대사 표지자(Ca metabolic markers)의 농도를 비교하였으며, 혈액으로부터 단핵세포(PBMC)를 분리 배양하여 단핵세포로부터 발현되는 골대사성 사이토카인의 mRNA를 분자생물학적으로 검토하였다.
연구 방법
1. 연구대상 및 절차
자율적으로 실험에 참여를 희망하는 대상자 중, 골다공증 관련 약물이나, 흡연, 심한 알코올 섭취를 하지 않은 65세 이상의 고령 여성 30명을 모집한 후 골밀도를 측정하여 골감소증 대상자 9명을 선정하였다. 대상자들의 평균 연령은 67.67±3.24세로, 평균 체중(kg) 53.24 ± 4.79, 평균 신장(cm) 151.10±3.14, 평균 BMI (kg/m2)는 23.33±1.99였으며, BMD T-score (score)는 -2.61±0.46이었다. 이들 대상자들에게는 실험규정에 따라 실험내용 및 불편함, 실험중지의 자유 등에 대하여 자세히 설명하고, 각 피험자로부터 동의를 얻었다. 본 실험은 동일집단에 의한 반복측정으로, 운동 1주일 전 피험자들은 실험실 도착 후 아무 활동 없이 의자에 앉아 안정을 취하며 채혈만 하는 비운동 통제 실험(CON 집단)을 하였고, 다시 1주일 후에 60 %VO2max 운동(EX 집단)하는 반복측정을 실시하였다. 본 실험에서 통제집단을 설정한 이유는 측정 변인의 일내변동을 측정함으로써 60 %VO2max 운동에 의한 변화를 알아보기 위하여 실시되었다.
2. 분석 항목 및 분석 방법
1) 골밀도 측정 및 골감소증 평가
최초 65세 이상의 고령 여성 30명은 본 실험의 대상자 선정을 위하여 이중에너지 X레이 흡수법(Dual energy X-ray apsorptionmetry, DEXA)의 골밀도 측정장비(DPX-L, LUNAR, USA)를 이용하여 전신골밀도를 측정하였다. 골감소증의 판정은 세계보건기구(WHO)에서 제시하는 T-Score를 기준으로, 정상(T-score > -1 SD), 골감소증(-1 SD < T score > -2.5 SD), 골다공증(T-score < -2.5 SD)으로 분류하였다[19]. 그 결과 골다공증 5명을 포함한 골감소증으로 판명된 9명을 최종 대상자로 하였다.
2) 운동 강도와 시간 설정
60 %VO2max 운동 강도 결정을 위하여 자전거 에르고미터(Helmass, Combi 75XL Ⅱ, Japan)를 이용하여 VO2max를 추정하였다. 대상자들이 고령이고 골다공증을 지닌 연약한 여성인 점을 고려하여 안전성이 검증된 최대하 운동부하법으로 VO2max를 추정하였다. 참여자들은 측정에 앞서 1분에 50바퀴의 회전수를 유지하는 속도로 준비운동을 실시한 후 최대심박수의 70%에 도달하게 하였고, 이때의 심박수 반응 과 부하의 관계를 토대로 회귀직선식을 구하여 VO2max를 추정하였다[20]. 본 연구에 참여한 대상자들의 VO2max (mL/kg/min)는 23.49±2.81, 안정시 심박수(beat/min)는 70.56±6.58, 최대심박수(beat/min)는 152.33±3.24였다. 이러한 검사 결과를 토대로 60 %VO2max에 해당하는 운동강도를 구하였고, 이때의 심박수(bpm)를 이용하여 운동 시 60 %VO2max의 강도를 유지하는지를 모니터링하는 기준으로 이용하였다. 또한 산소 1 L 당 5 kcal를 소비하는 것으로 가정하여 200 kcal의 열량소비에 필요한 운동소요시간을 계산하여 대상자 모두가 동일한 운동량을 소비하도록 하였다.
3) 안정 시 및 60 %VO2max 운동 부하 실험
9명의 대상들은 VO2max 측정 1주 후에 비운동 안정 시를 측정(CON 집단)하였으며, 다시 1주일 후에 60 %VO2max 자전거 에르고미터 운동실험을 실시(EX 집단)하였다. 대상자들에게 각각의 60 %VO2max에 상응하는 목표심박수(bpm; within ±5%)를 설정하고, 페달링 속도는 50 rpm으로 고정하여 동일하게 200 kcal의 운동을 수행하도록 시간을 조정하였다. 60 %VO2max 강도에서의 200 kcal 소비를 위한 대상자들의 평균 목표 심박수(beat/min) 및 운동시간(min)은 121.2±3.6과 45.7±6.5였다.
4) 채혈 및 혈액 분석
채혈 전 모든 대상자에게 일정한 식사패턴을 유지하게 하고, 신체활동을 제한하도록 권유하였다. 안정시 채혈은 모든 대상자들이 12시간 이상의 공복상태로 실험실에 도착하여 30분간 안정을 취한 후(Baseline, B) 수집되었다. 이후 각각의 지정된 시간동안 60 %VO2max 운동을 수행하고, 운동 종료 직후(Post, P), 60분 후(recovery, R)에 각각 10 mL의 혈액이 수집되었다. CON 집단의 채혈은 운동을 하지 않고 안정된 상태에서 동일시간대에 수집되었다. 채혈된 혈액으로부터 4 mL는 골흡수성 사이토카인의 mRNA 발현을 검토하기 위하여, PBMC를 분리 추출하여 총 RNA를 분리했다. 나머지 6 mL는 3,000 rpm으로 15분 간 원심분리하여 혈청을 분리한 후 골흡수성 사이토카인의 농도 및 칼슘대사 마커를 분석하였다.
5) 혈청 골흡수성 사이토카인의 농도 및 칼슘대사 마커 분석
원심분리된 혈청은 분석 시까지 -80℃ 냉동고에 보관하였다. 골흡수성 사이토카인인 TNF-α, IL-6, IL-1β와 INF-gamma의 혈청 농도를 측정하기 위하여 각각의 측정용 ELISA 킷(Human TNF-α ELISA kit, Fine Test, China; Human IL-6 ELISA kit, Fine Test, China; Human IL-1β ELISA kit, Fine Test, China; Human INF-γ ELISA kit, Fine Test, China)을 사용하여 분석하였다. 혈청 Ca과 Alkaline Phosphatase, P, Mg은 전문 혈액 분석회사인 C 재단(검사기관기호 NO: 11370319)에 의뢰하여 분석하였다.
6) 말초혈액의 PBMC로부터의 사이토카인 mRNA 발현량 분석
(1) PBMC 분리
채혈한 혈액의 약 4 mL는 PBMC 추출을 위하여 헤파린 튜브(BD Franklin Lakes NJ, USA)에 채취한 후 동량의 phosphate-buffered saline (PBS)에 희석하여, 4 mL의 Ficoll-Paque (Pharmacia, Sweden)에 중층하고, 상온에서 400×g로 20분간 원심분리하였다. Ficoll-Paque과 혈액 사이의 경계에 분리된 PBMC들을 얻은 후, 2차례 phosphate-buffered saline을 첨가한 후 세척과정을 거쳐 순수 PBMC를 분리하였다.
(2) 총 RNA 추출
PBMC의 분리 및 총 RNA의 추출은 Pacifici 등[10]의 방법을 개량하여 실시하였으며, 전 과정은 멸균상태에서 조작하였다. 분리된 PBMC를 modified acid guanidinium-thiocyanate-phenol-chloroform 추출 방법[21]을 이용한 RNAzol Kit (Guadine thiocyanate 4M, 2-metrcaptoethanol 0.1M, Phenol; TEL TEST INC., USA)을 사용하여 총 RNA를 분리하였다. 즉, PBMC에 0.5 mL의 RNAzol을 넣어 세포를 용해시킨 후, 0.05 mL의 클로로포름 용액을 첨가하여 혼합하고, 얼음 위에서 5분간 처리 후, 4℃에서 12,000×g로 15분간 원심 분리하였다. 원심 후 상청액에 이소프로필 알코올 0.5 mL을 첨가하여 총 RNA를 추출하고, RNA가 추출되었는지를 마이크로분광광도계 (ASP-2680, CellTA Gen, Korea)를 이용하여 260 nm/280 nm의 비율로 흡광도를 측정하여 확인하였다. 최종적으로 추출되어진 RNA는 -80℃에 측정 시까지 75% 에탄올에 넣어 보관하였다.
(3) 역전사 반응법에 의한 Complementary DNA (cDNA) 합성
각 RNA로부터 cDNA의 합성은 AccuPower RocketScript™ Cycle RT PreMix (Bioneer. Korea)를 사용하였다. 75% 알코올로 보존(-80℃)하고 있던 각 RNA를 실온에서 15분간 건조시킨 후, 10 μL의 DNase/RNase free의 2차 증류수로 용해하여 사용하였다. 제조사의 설명서에 따라서 RNA 용해액에 Reverse Transcriptase, Oligo (dT) 20, dNTPs, reaction buffer 및 primer 등 순환 온도 역전사 반응(Cyclic Reverse Transcription, CTRT)에 필요한 구성 성분을 포함하는 pre Mix를 넣고, DW로 총량을 20 μL로 하여 cDNA를 합성하였다. 반응조건은 primer annealing을 위한 37°C에서 30초, cDNA 합성을 위한 50°C에서 4분, RNA template의 secondary structure 해소를 위한 55°C에서 30초 과정의 역전사반응을 12회 반복하였다. DNA는 측정 시까지 -20℃에 보관하였다.
(4) 실시간 중합효소 연쇄반응(Real-time PCR)
각 사이토카인 mRNA의 분석은 실시간 중합효소 연쇄반응(Real-time quantitative polymerase chain reaction)을 이용하여 측정하였으며, CFX96 Real-Time PCR Detection System (BIO-RAD, USA)을 사용하여 cDNA를 증폭시켜 측정하였다. 본 실험에서 측정한 사이토카인 mRNA는 TNF-α 및 IL-6, IL-1β, INF-γ 이며, 정량을 위하여 하우스키핑 유전자인 glyceraldehyde 3-phosphate dehydrogenase (GAPDH) mRNA에 대한 상대량을 분석하였다. 역전사반응을 통하여 합성된 cDNA와 반응하는 forward primer 및 reverse primer는 Primer ExpressTM (Applied Biosystems, Foster, CA, USA)을 이용하여 설계하였다(Table 1). PCR의 조건은 각 well에 SsoAdvanced SYBR Green supermix (BIO-RAD, USA) 10 μL와 각각 5 pMol의 forward primer와 reverse primer 1 μL와 cDNA를 1 μL 넣고, 최종적으로 Diethylpyrocarbonate (DEPC) 처리수와 혼합하여 총 용량인 20 μL의 반응액을 만들어 PCR을 수행하였다. 95℃에서 5분간 전 처리(pre-denaturation)한 후, 각 주기(cycle)마다 95℃에서 15초간 변성(denaturation), 59-60℃에서 60초 동안의 결합(annealing) 과정을 40회 반복하고, 그 후 최종적으로 Melt curve를 위하여 65-95℃에서 각 step당 1-5초간 반응시켰다. SYBR Green 분석은 C1000 Thermal Cycler (CFX96 real-time system, Bio-Rad, US)를 사용하였다. 각각의 target mRNA 발현량은 GAPDH mRNA양으로 보정하였으며, 각 집단의 안정 시 발현량을 기준으로 하여 변화율로 나타냈다.
3. 자료처리방법
본 연구의 통계처리는 SPSS for Windows (ver. 21.0) 통계 프로그램을 사용하였다. 모든 측정치에 대한 평균 및 표준오차를 산출하였다. 통계처리는 이원변량 반복측정 분산분석(2-way repeated measure ANOVA)을 실시하여 2집단(CON 집단 및 EX 집단)에 따른 3시기(운동 개시 전 안정 시, 운동 종류 직후 및 회복 60분 후) 간의 차이(2 by 3)를 분석하였다. ANOVA 검사 후 유의한 차이가 있을 경우 Adjusted Bonferroni를 통해 사후검사를 실시하였다. 모든 통계치의 유의수준(α)은 5% 미만(p< .05)으로 설정하였다.
연구 결과
1. 혈청 TNF-α, IL-6, IL-1β, and INF-γ 농도 비교
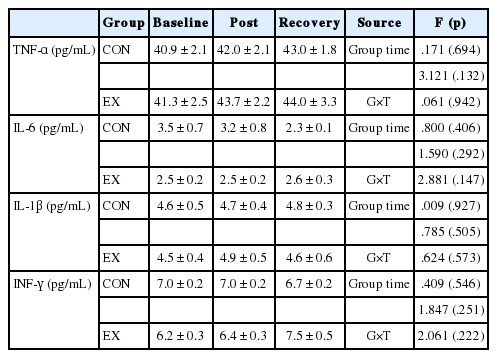
Table 2에는 두 집단 간의 운동 개시 전 안정시(baseline, B) 및 처치 직후(post, P), 회복 60분 후(recovery, R)의 TNF-α 및 IL-6, IL-1β, INF-γ의 혈청 농도 변화를 나타냈다. 모든 혈청 사이토카인 농도 변화에 있어서 두 집단에 따른 상호작용 효과 및 각각의 집단, 시기에 따른 주효과 모두 유의한 변화는 없었다.
2. TNF-α, IL-6, IL-1β, and INF-γ mRNA 발현 변화
Table 3에는 두 집단 간의 운동 전 안정 시 및 처치 직후, 회복 60분 후의 PBMC로부터의 TNF-α 및 IL-6, IL-1β, INF-γ mRNA 발현 변화를 나타냈다. 이원변량 반복측정 분산분석 결과, 대부분의 mRNA 발현 변화에 있어서 상호작용 효과 및 각각의 집단, 시기에 따른 주 효과 모두 유의한 차이는 없었지만, TNF-α mRNA 발현에서만 집단 간에 유의한 차이가 나타났다(p=.008).
3. 혈청 골대사 마커 및 칼슘대사 마커
두 집단 간의 운동 전 안정 시 및 처치 직후, 회복 60분 후의 Serum Ca 및 P, Mg, ALP 농도를 Table 4에 나타냈다. Serum Ca은 이원변량 반복측정 분산분석 결과 시기의 주효과가 나타났다. 즉, EX 집단의 처치 직후에 유의하게 증가하였다가(p < .05) 회복 시에 유의하게 감소하였다(p< .01). Serum ALP도 시기의 주효과에서 유의한 것으로 나타났고, 이는 두 집단 모두 처치 직후에 비해 회복 시의 감소로 나타난 것이었다(p< .01). Serum P와 Mg는 상호작용 및 주 효과 모두 유의한 차이를 보이지 않았다.
논 의
일회성의 중강도 운동이 골대사에 미치는 영향을 검토하기 위하여, 본 연구에서는 골흡수가 진행되고 있는 골량감소 고령여성을 대상으로, 60 %VO2max 운동을 부하하여 운동 전과 처치 직후, 회복 60분 후의 혈액을 채취하여, 혈청 골대사 관련 사이토카인과 칼슘대사 마커의 농도를 검토하였다. 또한 PBMC로부터 발현되는 골대사 관련 사이토카인의 mRNA 발현을 비운동 시와 비교 검토하였다. 그 결과, 두 집단 간의 운동 전 안정 시 및 처치 직후, 회복 60분 후의 혈청 TNF-α 및 IL-6, IL-1β 농도 변화를 검토한 결과 모든 항목에서 유의미한 결과를 발견할 수 없었다. 같은 시기의 PBMC로부터의 이들 사이토카인의 mRNA 발현 변화를 검토한 결과에서도 통계적인 유의차는 나타나지 않았지만, TNF-α mRNA 발현에서만 시기 간이 아닌 집단 간에 유의한 차이가 나타났다(p =.008). 즉, 골감소증 고령 여성에게 있어 일회성 중강도 운동은 골흡수성 사이토카인의 생성에 큰 영향을 미치지 않을 가능성이 시사된 것이다. TNF-α와 IL-6 등은 뼈에서는 골수세포 및 마크로파지계 세포, 말초혈액 단핵세포(peripheral blood mononuclear cell, PBMC) 등으로부터 생성되며, 특히 파골세포의 증식과 활성화를 촉진하고, 강력하게 골흡수를 촉진시키는 골흡수성 사이토카인으로 알려져 있다[13,15,22]. Suda et al. [23]의 전구파골세포와 조골세포를 사용한 실험에서 TNF-α와 IL-6 등이 비례하여 파골세포의 형성을 촉진하는 것을 보고하고 있으며, Ishimi et al. [24]은 갓 태어난 생쥐 뼈를 사용한 실험에서 IL-6가 IL-1과 협조하여 골흡수를 촉진하는 것을 보고하는 바와 같이 TNF-α 및 IL-6뿐만 아니라 IL-1β도 골흡수성 사이토카인으로 알려져 있으며, 이들 골흡수성 사이토카인의 공조에 의하여 파골세포를 자극하여 골흡수를 촉진하는 것이 알려져 있다. 또한, 장기간의 절대안정상태(bed rest)에 의하여 일어나는 부동성 골위축에 있어서도 이들 골흡수성 사이토카인이 골대사를 조절하고 있음이 보고되고 있으며[25], 흰쥐의 뒷다리 부유 골조직에서도 골량감소와 함께 사이토카인 mRNA의 발현이 증가됨을 밝히고 있다[26].
한편, 운동 시의 TNF-α와 IL-6 mRNA의 발현증가 요인에 대해서는 단순히 골격근 손상에 따른 염증반응의 증가가 직접적인 원인이 될 수 있으나, De Rijk et al. [27]이 밝히는 바와 같은 아드레날린의 증가에 의하여 일어날 수 있으며, 혈장 IL-6은 혈장 젖산 농도에 비례한다는 Ostrowski et al. [28]의 연구와 같이 운동 강도와 관련이 깊을 가능성도 알려져 있다. 또한, 자전거 에르고미터를 사용한 1회성의 무산소성 고강도 운동을 부하한 결과, 운동 15분 후 젖산증가와 함께 골흡수성 사이토카인인 IL-6와 TNF-α의 mRNA가 유의하게 증가하는 것을 밝혀 내고, 고강도 운동에 따른 혈액의 산성화가 골흡수성 사이토카인의 발현을 증가시키고 있음을 밝히고 있다[29]. 그러나 최근의 연구에 있어서 무산소성 역치점 이하 강도에서 실시한 1회성 운동 후에는 TNF-α와 IL-6 mRNA 발현이 증가하지 않았다는 보고도 있다[30]. 이러한 결과들로부터 TNF-α와 IL-6 등의 골흡수성 사이토카인의 발현은 운동강도에 반응하며, 적어도 역치점 이하의 운동 강도는 세포레벨에서의 사이토카인의 발현에 큰 영향을 미치지 않을 가능성이 시사된다. 본 연구에서도 혈청과 mRNA에서 모두 TNF-α 및 IL-6, IL-1β의 생성이 변화하지 않았던 이유는 본 연구에서 실시한 60 %VO2max 강도가 골대사를 자극하기에는 불충분했던 것으로 판단된다. 최근 Park et al. [31]의 연구에서는 우리나라 현실을 감안하여 운동 강도를 표준화하면서 VO2max의 45-64%를 중강도로 정의하고 있으며, 이러한 점들을 고려할 때 고령 여성의 경우 본 연구에서 처치한 200 kcal를 소모하는 조건에서의 60 %VO2max의 중강도 운동은 골흡수성 사이토카인을 자극할 정도의 운동 강도로는 부족한 것으로 사료됐다. 특히, 같은 강도라도 칼로리 소모를 증가(200 kcal vs. 300 kcal)시키는 조건에서는 생리적으로도 운동강도가 더 커지기 때문이다. 또한, 본 연구에서 TNF-α mRNA 발현에서 집단 간에 유의한 차이가 나타났던 것은 운동에 의한 효과라기보다는 기초선(baseline)에서의 발현량 차이에 기인한 것이라고 판단되었다.
또한, 주로 T세포로부터 생산되는 INF-γ는 TNF-α와 IL-6과 상반되게 파골세포의 형성을 억제하고[17], 파골세포의 분화를 저해함으로써[18] 골형성 작용을 한다. 본 연구 결과에서 혈청 INF-γ 농도와 PBMC로부터의 INF-γ mRNA 발현에 있어서 두 집단 간의 통계적인 유의차는 발견할 수 없었다. 이는 본 연구에서 실시한 1회성의 60 %VO2max 운동이 골형성 사이토카인 생성에도 영향을 미치지 못하는 강도였다는 것을 보여주는 것이라 판단된다. 한편, 장기간의 운동 부하에 따른 사이토카인의 변화는 일회성 운동과는 다르게 나타날 수 있다. 최근의 Marques et al. [32]의 주 2회 저항성 운동과 주 1회의 유산소 운동의 복합 운동을 32주간 실시한 연구에서 골밀도와 함께 혈청 사이토카인의 농도 변화를 검토한 결과, 근력과 함께 골밀도의 증가를 관찰하였으나, TNF-γ에서는 변화가 없었고, IL-6에서는 감소하는 경향을 나타냈다고 보고하고 있다. 즉 1회성 운동 후에는 일시적으로 증가하지만, 운동이 장기간 지속된 후에는 생성량이 변화될 가능성이 있는 것이다. 장기간의 운동 부하에 따른 INF-γ 변화에 있어서도 TNF-α와 IL-6와 마찬가지로 다르게 나타나서, 8주간의 복합운동 후에 INF-γ가 감소한다는 보고[33]도 있지만, 8주간의 운동 후에 변화하지 않는 다는 보고[34]도 있어 아직까지 명확한 결론을 내리지 못한 상태이다. 추후 운동 강도 또는 운동량에 따른 추가적인 실험이 이루어져야 할 것으로 판단된다.
혈청 ALP는 시기에 있어 통계적 유의차가 있었으나 두 집단 모두 유사하게 회복 60분 후에 유의하게 감소하고 있어 집단 간의 차이를 발견할 수 없었다. 혈청 Ca 대사 마커에 있어서 유의미한 변화를 나타낸 것은 혈중 Ca농도로, 대조집단에서는 변화가 없었음에도 불구하고, 운동 집단에 있어서는 운동 종료 직후에 유의하게 증가하였다가(p< .05) 회복 60분 후에 다시 유의하게 감소하였다(p< .01). 즉 60 %VO2max 운동에 의하여 운동 종료 직후에 일시적인 고칼슘혈증(Hypercalcemia)이 발생하고 있을 가능성이 시사되었다. 임상적으로 고칼슘혈중은 혈중 칼슘농도가 12 mg/dL 이상인 상태를 말하며, 본 실험에서 나타난 고칼슘혈증은 신체적 이상을 초래할 정도의 높은 수준은 아니라고 판단된다. 고칼슘혈증은 부갑상선호르몬 관련 단백질(parathyroid hormone-related protein, PTH-rP) 등의 체액성 매개체에 의하여 발생되는 것으로 알려져 있으며, PTH-rP는 PTH와 유사한 구조를 가지고 있어 골흡수를 촉진시켜 혈청 칼슘 농도를 상승시키는 것으로 알려져 있다[35]. 본 연구에서 밝혀진 고칼슘혈중은 일회성 운동에 의한 일시적인 생체 반응으로 장기간의 운동에 대한 생체 적응 결과와는 차이가 있을 수 있다. 예를 들어 일시적인 운동은 심박수를 증가시키지만, 장기간의 운동의 경우 안정 시 심박수를 감소시키는 것처럼, 일시적인 반응과 장기적인 적응은 서로 다르게 결과가 나타날 수 있다. 따라서 장기간의 운동 부하에 따른 칼슘 대사와의 관계에 대한 추가 연구가 필요할 것으로 판단된다.
결 론
200 kcal를 소모하는 조건에서의 일회성 60 %VO2max 중강도 운동은 골감소증 고령여성의 골대사성 사이토카인의 혈청 수준 및 PBMC로부터의 mRNA생성에는 영향을 미치지 못하지만, 경도의 고칼슘혈증을 발생시킬 가능성이 시사되었다.