여성 노인의 대퇴 골밀도 감소에 따른 대사증후군과 체력 비교
Comparison of Metabolic Risk Factors and Physical Fitness according to Femur Osteoporotic Status in Elderly Women
Article information
Trans Abstract
PURPOSE
This study was to compare metabolic risk factors and physical fitness according to femur bone mineral density (BMD) status in elderly women.
METHODS
A total of 300 female participants aged 73.5±6.8 years were voluntarily recruited from local community centers. Whole body composition including body weight, body mass index (BMI), waist circumference, percent body fat, and bone mineral density, was determined using dual-energy X-ray absorptiometry. Metabolic risk factors, such as resting blood pressures, fasting glucose, and lipids, were assessed in fasting blood. Analysis of covariance (ANCOVA) followed by LSD post-hoc test, if necessary, was applied to determine significant differences in dependent variables among normal, osteopenia, and osteoporosis groups. Multivariate linear regression was used to determine significant determinants of osteoporotic status.
RESULTS
ANCOVA showed significant differences in upper body strength (p<.001), upper and lower body flexibility (p=.024 & .048, respectively), and appendicular skeletal muscle mass (ASM) (p<.001) among the osteoporotic status-based subgroups; the normal and osteopenia groups had significantly higher means in upper strength (p<.05) upper and lower strength (p<.05), and ASM (p<.05) than the osteoporosis group. Multivariate linear regression analyses revealed that age (p<.001), upper body strength (p=.035), and BMI (p=.012) were independent predictors of osteoporotic status.
CONCLUSIONS
Findings of this study suggest that muscular strength and BMI in conjunction with age were important factors in determining individual variability of bone health status in this study population, implying the importance of strength exercise and a healthy body weight against loss of bone density associated with aging.
서 론
골다공증(osteoporosis)은 뼈의 양(bone mass) 감소와 미세구조 변화로 골절 위험성을 증가시키는 대표적인 노인성 근골격계 질환이며, 특히 여성의 경우 폐경 이후 호르몬의 변화로 인해 골 소실이 더욱 급격히 일어나 남성보다 여성에게 더 많은 유병률을 보인다[1,2]. 국내의 골다공증 유병률을 살펴보면 여성의 경우 37.3%, 남성의 경우 7.5%에서 골다공증이 관찰되었고 여성의 경우 48.9%, 남성의 경우 46.8%에서 골감소증이 관찰되었으며 노화가 진행됨에 따라 골감소증에서 골다공증으로 진행된다는 점을 고려할 때 노년기에 매우 흔한 질환으로 이를 예방 및 관리하기 위한 사회적인 관심이 필요할 것으로 보인다[3]. 한편, 골다공증은 인종, 가족력, 조기폐경과 같은 유전적인 요인뿐만 아니라 류마티스 관절염, 당뇨병과 같은 만성 질환과 저체중, 비활동성(inactivity), 낮은 수준의 체력과 같은 생활습관 등 다양한 위험요인이 원인이 된다. 최근 선행연구는 노인의 대사증후군이 골다공증 혹은 골절과 관련있는 것으로 보고하였다[4-8].
노인의 대사증후군은 노화 진행에 따라 복부비만 증가와 신체활동 감소로 이어지고 이는 혈압 상승, 혈중 인슐린 증가 및 이상지질혈증 등으로 인해 만성질환이 유발되는데 궁극적으로 심혈관계질환 발생 및 사망위험에 크게 영향을 미치는 것으로 보고된다[9]. 또한 대사증후군은 전신의 낮은 염증성 상태(systemic inflammation)와 관련 있는데 최근 연구에 의하면 이는 골 흡수 과정(bone resorption process)을 활성화시켜 결과적으로 골밀도의 감소를 초래하는 것으로 보고하였다[10]. 또 다른 연구에 의하면 혈중 지질 수준은 폐경 후 여성의 골밀도 수준과 연관성이 있는 것으로 보고되었다[11]. 그러나 이와 다르게 대사증후군 위험 요인이 골다공증과 연관성이 없다는 연구결과들도 보고되고 있다. 예를 들어, 폐경 여성을 대상으로 한 횡단적 연구에서 대사증후군을 가진 집단과 그렇지 않은 집단의 골밀도의 통계학적 유의한 차이가 없었으며 대사증후군 위험요소인 혈중지질과 허리둘레 등에서도 골밀도와 상관관계가 없는 것으로 나타났으며[12] 대사증후군 위험인자인 비만 혹은 높은 수준의 BMI가 골다공증을 예방하는 효과가 있다는 연구결과 보고도 있어[13] 대사증후군과 골다공증의 관계는 명확하게 정의되지 않은 상태이다.
한편, 규칙적인 근력강화 운동은 50세 이상 노인의 골다공증을 예방 혹은 치료 수단으로 이용될 뿐만 아니라 낙상 혹은 골절의 위험률을 낮추는 것으로 알려진다[14]. 선행연구에 의하면 근력 운동은 폐경 후 여성의 골 손실을 완화시킨다고 하였으며 유산소성 운동 또한 골밀도를 증가시키는 데 효과가 있는 것으로 알려진다[15]. 또한, 폐경 여성의 높은 심폐체력 수준은 골 손실 위험률과 부적 상관관계를 갖는 것으로 나타났다[16]. 그러나 국내 노인을 대상으로 노인 체력과 대사증후군 위험 요소가 골다공증에 미치는 영향에 대한 연구는 제한적으로 진행되어왔다.
따라서 본 연구에서는 여성 노인을 대상으로 골밀도 수준에 따른 집단 간 대사증후군 위험요소와 체력지표를 비교하고, 골밀도의 개인 차이에 대한 독립예측인자를 결정하는 것을 연구의 목적으로 하였다.
연구 방법
1. 연구 대상자
본 연구의 대상자는 특별한 의학적 질환이 없고 정상적인 일상생활 수행이 가능한 경기도 S시 지역의 65세 이상 여성 노인 300명을 연구 대상자로 하였다. 모든 피험자는 연구의 목적 및 진행방법에 대한 사항을 문서와 구두로 자세히 설명 들었으며 실험 참여 동의서를 작성한 후 실험에 참여하였다. 본 연구는 S 대학교 생명윤리위원회의 승인(SKKU-IRB-2014-01-002)을 받아 진행되었다.
2. 신체구성 지표와 골밀도 측정
피험자의 신장은 자동측정기(DS-102, Jenix, Korea)를 이용하여 측정하였다. 체중, 근육량 및 골밀도는 이중 에너지 X-ray 방사선 흡수 계측(Dual-energy X-ray Abosorptiometry, DXA) 원리를 사용하는 Lunar DPX Pro (GE medical systems Lunar, USA)를 이용하여 측정하였으며 대퇴 부위(Femur total) 골밀도를 g/cm2 단위로 측정하였다. 사지근육 비율(appendicular skeletal muscle mass index, ASM index)은 사지근육량(kg)/신장(m2) 공식을 이용하여 산출하였다. 체질량지수(body mass index, BMI)는 측정된 체중과 신장을 이용하여 체중(kg)/신장(m2) 공식으로 산출하였다. 허리둘레(WC)는 일정교육을 받은 조사자들이 인체측정줄자를 이용하여 늑골 하단부(lower border of rip cage)와 장골능 상부(top of iliac crest)의 중간 지점에서 측정을 실시하였다. 피험자의 혈압은 자동혈압계(Jawon Medical, Korea)로 측정하였으며 혈압 측정 전 5분간 앉은 상태에서 휴식을 취한 후 3분 간격으로 2회 측정하여 평균값을 이용하였다.
피험자의 골밀도 수준에 따른 분류는 대퇴 골밀도의 T-score에 근거하였으며 T-score≥-1.0의 경우 정상(normal)집단으로 -2.5<T-score<-1.0의 경우 골감소증(osteopenia)집단으로 T-score≤-2.5인 경우 골다공증(osteoporosis)으로 구분하였다.
3. 노인체력검사
건강관련체력은 피로를 느끼지 않고 일상생활을 수행할 수 있는가에 대한 체력 요인으로써 Rikli & Jones [17]에 의해 개발된 노인체력검사(senior fitness test, SFT)를 바탕으로 실시하였으며, 그 중 건강관련체력 요인인 상체 근력(30초간 덤벨 들기), 하체 근력(30초간 의자에 앉았다 일어서기), 유연성(등 뒤로 손잡기, 앉아 윗몸 앞으로 굽히기), 심폐지구력(2분 제자리 걷기), 균형감(외발서기)을 측정하였다.
4. 대사증후군 위험인자 측정
모든 피험자는 12시간 공복 후 정맥혈액을 채혈한 다음 원심분리기(원심분리기: MF 300, Hanil, Korea)를 이용하여 3,000 rpm에서 20분간 원심 분리한 후 혈청(serum)만 분리하여 -70℃ 초저온 냉동고에 분석 전까지 보관하였다. 혈중 glucose, triglyceride (TG), high-density lipoprotein cholesterol (HDL-C)는 N의료원에 혈액분석실에서 colormetric assay 방법을 이용하여 분석하였다.
5. 자료처리 방법
본 연구의 모든 자료는 평균과 표준편차(mean±SD)로 표기하였다. 골밀도에 따른 신체구성은 일원변량분석(One-Way ANOVA)을 사용하였으며 유의한 결과에 대한 사후검증으로 LSD를 사용하였다. 골밀도에 근거한 정상집단, 골감소증, 골다공증 집단 간 대사증후군 위험인자 및 노인체력 차이는 집단 간 연령차이를 통계적으로 보정한 공분산분석(Analysis of covariance, ANCOVA)를 이용하여 검증하였다. 또한, 다중선회귀분석을 이용하여 골밀도의 개인차이에 대한 독립예측인자를 결정하였다. 모든 통계분석은 SPSS-PC (version 18.0)을 이용하고 가설 검정을 위한 유의수준은 α=.05로 설정하였다.
연구 결과
1. 여성노인의 대퇴골밀도에 따른 신체구성과 폐경나이 비교
Table 1은 대퇴골밀도의 T-score를 바탕으로 정상, 골감소증, 골다공증 집단으로 분류하여 각 집단에 따른 신체구성과 폐경나이를 비교한 것이다. 신체구성 중 나이(p<.001)와 체중(p<.001)에서 집단 간 유의한 차이가 있는 것으로 나타났으며, 사후 검증 결과 정상집단과 골감소 집단, 골감소 집단과 골다공증 집단, 정상집단과 골다공증 집단에 유의한 차이가 있는 것으로 나타났다. 신체구성 중 BMI (p<.001)와 체지방량(p<.001)에서 집단 간 유의한 차이가 있는 것으로 나타났으며 사후 검증 결과 정상집단과 골다공증 집단에서 유의한 차이가 있는 것으로 나타났다. 폐경나이의 경우(p=.022) 집단 간 유의한 차이가 있는 것으로 나타났으며 사후검증 결과 정상집단과 골다공증 집단에 유의한 차이가 있는 것으로 나타났다.
2. 여성노인의 대퇴골밀도에 따른 대사증후군 위험인자 비교
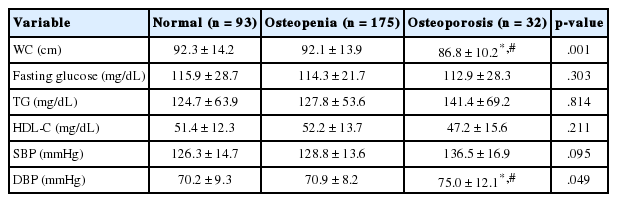
Table 2는 대퇴골밀도 정도에 따라 나이를 보정한 후 대사질환 위험 요소를 비교한 것이다. 대사질환 위험요소 중 허리둘레(p=.001)와 이완기(p=.049)에서 집단 간 유의한 차이가 있는 것으로 나타났다. 사후 검증 결과, 허리둘레는 정상집단에 비해 골다공증집단(p=.001) 그리고 골감소 집단에 비해 골다공증 집단(p=.017)에서 유의하게 감소된 것으로 나타났고, 정상집단과 골감소 집단 간에는 통계학적으로 유의한 차이가 없었다. 이완기 혈압은 정상집단에 비해 골다공증집단(p=.033) 그리고 골감소 집단에 비해 골다공증 집단(p=.038)에서 유의하게 더 높은 것으로 나타났고, 정상집단과 골감소 집단 간에는 통계적으로 유의한 차이가 없었다. 그 외 혈당, 중성지방, 고밀도 지단백 콜레스테롤, 수축기 혈압은 집단 간에 통계적으로 유의한 차이가 없는 것으로 나타났다.
3. 여성노인의 대퇴골밀도에 따른 체력 비교
Table 3은 대퇴골밀도 정도에 따라 나이를 보정한 후 체력을 비교한 것이다. 체력 요소 중 상체근력(p<.001), 상체 유연성(p=.024), 하체 유연성(p=.048), 사지근육량(p<.001)이 집단 간 유의한 차이가 있는 것으로 나타났다. 사후검증 결과, 상체근력(p<.001 & p<.001, respectively), 하체(p=.035 & p=.022, respectively) 유연성, 사지근육량(p=.007 & p=.004, respectively)은 정상집단에 비해 골감소증 및 골다공증집단에서 유의하게 더 낮은 것으로 나타났다. 상체(p=.001)유연성의 경우 정상집단에 비해 골감소 집단에서 유의하게 낮은 것으로 나타났다. 상체 근력, 상체 및 하체 유연성, 사지근육량은 골감소증과 골다공증 집단 간에는 통계적으로 유의한 차이가 없는 것으로 나타났고, 하체근력, 심폐지구력, 균형감은 정상집단, 골감소증, 골다공증 집단 간에 통계적으로 유의한 차이가 없는 것으로 나타났다.
4. 여성노인의 대퇴골밀도 저하에 대한 독립예측인자결정을 위한 회귀분석
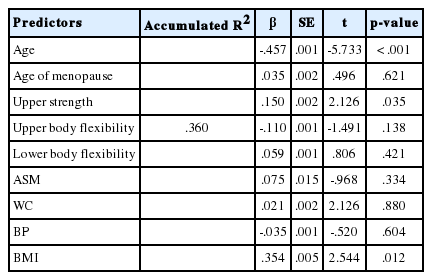
Table 4는 다중선회귀분석을 이용하여 노인체력과 대사성 위험인자가 대퇴골밀도에 대한 독립예측인자로서의 역할을 분석하였다. 그 결과 상체근력(β=.150, p=.035), 나이(β=-.457, p<.001), 체질량지수(β=.354, p=.012)가 독립예측인자인 것으로 나타났고, 구체적으로 대퇴골밀도는 상체근력과 체질량지수와는 양적 상관관계 그리고 연령과는 부적 상관관계를 갖는 것으로 나타났다.
논 의
본 연구는 여성 노인 300명을 대상으로 골밀도에 따른 대사증후군 위험요소와 노인 체력을 비교하고, 두 가지 변인이 여성 노인의 골감소에 위험요소로 작용하는지 검증하는 것을 주요 목적으로 하였다. 총 300명을 대상으로 대퇴골밀도의 T-score를 근거로 하여 집단을 구분한 결과, 정상 집단 93명(31%), 골감소증 집단 175명(58.3%), 골다공증 집단 32명(10.7%)으로 나타났다. 국내 대규모 통계자료인 2008년도부터 2011년까지 조사한 국민건강영양조사서에 따르면 50세 이상 여성에게서 37.3%가 골다공증이었고 48.9%에서 골감소를 보였으며 정상적인 골밀도를 가진 여성은 13.8%에 불구하였다[3]. 본 연구의 대상자가 65세 이상의 노인이었음에도 불구하고 대규모 국내 조사서의 골다공증 비율보다 낮게 나타난 이유는 특별한 의학적 질환이 없고 정상적인 일상 생활 수행이 가능한 지역주민 여성 노인을 대상으로 했기 때문인 것으로 사료된다.
골항상성은 낡은 뼈를 제거하는 골흡수와 새로운 뼈를 만드는 골형성이 평형을 이룰 때를 뜻하며 골항상성은 30-50세까지 대체로 유지되다 연령 증가에 따라 골소실이 급격히 진행된다[20,21]. 특히 여성은 폐경 이후 에스트로겐의 결핍으로 인해 급격한 골흡수가 진행된다[21]. 본 연구 결과는 선행연구 결과와 일치하게 골밀도가 낮을수록 연령이 유의하게 높아지는 것으로 나타났고 폐경 나이의 경우 골밀도가 낮을수록 폐경나이의 평균이 통계학적으로 유의하게 감소하는 것으로 나타났다.
대사증후군 위험인자는 전신에 산화성 스트레스와 염증 수준을 올려 골격근 대사와 뼈 건강에 부정적인 영향을 미친다는 연구 결과가 있지만[22], 또 한편으로는 대사증후군 유무와 대사증후군의 위험인자가 골감소와 상관관계가 없다는 연구 보고도 있어 논란의 여지가 있는 것으로 보인다. 본 연구결과에 의하면 총 300명의 여성 노인을 대상으로 대퇴골밀도에 따른 대사증후군 위험인자를 나이를 보정하여 비교한 결과 허리둘레와 이완기 혈압이 유의한 차이가 나는 것으로 나타났고 이완기 혈압의 경우 골밀도가 낮아질수록 증가되는 경향을 보였으며 허리둘레의 경우 골밀도가 낮아질수록 감소되는 선경향을 보였다. Zhou et al. [23]은 중국인을 대상으로 한 후향적 연구에서(retrospective cross-sectional study) 제2형 당뇨를 가진 폐경 후 여성의 높은 수축기혈압(SBP)이 척추 골밀도 T-score 감소와 관련 있는 것으로 나타났다. Cakmak et al. [24]의 터키여성을 대상으로 한 횡단적 연구에 의하면 폐경 후 여성의 골감소에 있어 당뇨와 고혈압은 통계학적으로 의미 있는 독립적인 위험인자로 나타났다. 한편, 대사증후군 위험인자 중 비만과 관련된 체질량 지수, 체지방률 및 체중은 골밀도가 낮을수록 통계학적으로 유의하게 낮아지는 선 경향이 있는 것으로 나타났다. 특히, 체질량 지수의 경우 골밀도의 독립예측인자인 것으로 나타났다. De Laet et al. [4]의 메타 연구에 의하면 체질량 지수가 25 kg/m2인 그룹과 비교했을 때 체질량 지수가 20 kg/m2인 그룹에서 골절 위험률이 2배 증가하는 것으로 나타났고 체질량 지수가 25 kg/m2인 그룹과 비교했을 때 30 kg/m2인 그룹에서 골절 위험률이 17% 감소하는 것을 확인하였다. 즉 낮은 수준의 체질량 지수는 골절에 위험요소인 것으로 나타났다. 이와 유사하게 Nguyen et al. [13]의 연구에 의하면 마르고 체중 감소가 있었던 여성 노인에서 체중이 비교적 일정했던 집단에 비해 골소실이 더 급격하게 일어나는 것으로 확인되었다. 이에 Moran et al. [25]은 BMI가 높은 폐경 후 여성의 경우 BMI가 낮은 여성에 비해 성호르몬과 결합하는 글로불린(globulin)의 양이 감소함에 따라 자유 에스트로겐이 증가하고 이는 조골세포의 에스트로겐 수용체와 결합하여 파골세포형성 억제인자(osteoprotegerin)를 감소시켜 골 흡수를 억제한다고 하였다. 또 다른 최근 연구에 따르면 BMI가 높은 경우 고인슐린혈증(hyperinsulinemia)에 걸릴 위험이 크고 고인슐린혈증은 혈중 IGF-1의 증가를 야기시켜 골아세포의 분화를 통해 골형성을 촉진시킨다는 결과를 발표하였다[26]. 즉, 적당한 허리둘레 및 체질량 지수는 노인의 골감소를 억제하는 데 긍정적인 효과를 거둔다는 선행연구는 본 연구결과를 뒷받침하고 있다[27].
여성노인의 체력과 골다공증에 관한 본 연구 결과는 나이를 보정하고도 상체근력, 상·하체유연성 그리고 사지 근육량에서 대퇴 골밀도에 따라 유의한 선 경향이 있는 것으로 나타났다. 이와 일치하는 선행연구로 Iki et al. [28]에 의하면 일본 폐경 여성 중 상체 근력이 낮은 집단에서 골 소실이 일어날 위험이 상체 근력이 좋은 집단에 비해 10배 이상 높은 것으로 나타났다. Iki et al. [29]의 또 다른 연구에 의하면 높은 상체 근력은 나이와 신체 사이즈 및 비타민 D의 유전형을 보정하고도 독립적으로 뼈 소실을 감소시키는 것으로 나타나 상체 근력이 골밀도 감소와 상관관계가 있는 것으로 나타났다. Lu et al. [30]의 중재 연구에 의하면 유연성과 균형감에 긍정적인 영향을 미치는 요가운동 10동작을 인터넷을 기반으로 하여 훈련시킨 결과 요가운동이 척추와 대퇴의 골밀도를 향상시키는 데 기여하는 것으로 나타났다. 또한 DeFina et al. [16]의 연구에 의하면 1,720명의 백인 폐경 후 여성을 대상으로 체력과 골밀도에 관한 코호트 스터디를 실시한 결과 골감소 집단에서 체력이 높은 사람(OR=.32)이 체력이 낮은 사람(OR=.50)에 비해 골감소에 걸릴 위험률이 적은 것으로 나타났고 골다공증 집단에서도 체력이 높은 사람(OR=.29)이 체력이 낮은 사람(OR=.30)에 비해 골다공증에 걸릴 위험률이 적게 나타났다.
본 연구결과와 선행연구를 종합하여 볼 때, 노화로 인한 골손실은 대사증후군 위험노출증가 및 체력감소를 유도할 수 있으며, 특히 체력, BMI, 나이는 여성 노인의 골밀도를 결정하는 데 중요한 결정인자인 것으로 나타났다. 따라서 이러한 결과는 규칙적인 신체활동을 통한 근력 증진과 건강 체중 유지가 노화로 인한 골 소실을 예방하는 데 긍정적으로 작용한다는 사실을 의미하는 것으로 판단된다.
결 론
본 연구에서 여성 노인의 골감소는 대사증후군 및 체력저하와 밀접한 연관성이 있으며, 상체근력과 체질량지수는 나이와 더불어 골밀도를 결정하는 데 중요한 요인으로 나타났다. 따라서 본 연구의 결과는 여성 노인의 골다공증 예방 차원에서 규칙적인 신체활동을 통한 체력 증진과 건강한 식습관 실천을 통한 건강체중유지의 중요성을 의미하는 것으로 판단된다. 다만, 본 연구는 여성 노인만을 대상자로 하는 횡적 연구라는 사실로 인해 연구결과에 대한 명확한 인과관계를 파악하기가 어렵기 때문에 추후 운동과 식습관을 포함한 건강생활실천을 통한 체력증진과 대사성 위험인자 개선이 노년기 골밀도에 미치는 영향을 검증하는 후속 연구가 필요할 것으로 판단된다.