비만 여대생의 저항성운동이 생리주기에 따른 아디포카인에 미치는 영향
Effects of Resistance Exercise on Adipokines According to Menstrual Cycle in Obese College Women
Article information
Trans Abstract
PURPOSE
The purpose of this study was to investigate the level of lipids and adipokines according to the menstrual cycle (follicular and luteal phase) and to investigate the effect of resistance exercise on the change of lipids and adipokines according to menstrual cycle.
METHODS
The subjects were living in C city and body fat of over 30% in the obesity college women students (n=30). These were divided into the follicular phase group (n=15) and the luteal phase group (n=15) by random sampling. All the contents of the study were approved by Kangwon National University IRB and applied to the guidelines for personal safety.
RESULTS
There was no interaction effect between group and time on body composition, lipid profiles and adipokines. Body composition showed a significant decrease in body percent fat in both groups. After the exercise program, there was a significant difference between groups in body percent fat. Also, TC was significantly decreased after 16 weeks compared with 0 week. Leptin concentration was significantly higher in the luteal group than in the follicular group and was significantly decreased after 16 weeks of exercise program in the luteal group. Adiponectin concentration was also significantly higher in the luteal group than in the follicular group, but in the luteal group, there was a significantly increase after 16 weeks of exercise program compared 0 week.
CONCLUSIONS
This study suggests that the concentration of aidpokine in the luteal phase is higher than that of the follicular phase and that the timing of blood collection is very important for women. Resistance exercise seems to have an effect on adipokine concentration.
서 론
우리나라의 출산율은 지속적으로 감소하고 있는데, 그 이유 중 하나로 여성들의 과도한 체중조절에 의한 마른 비만의 증가와 정신적 스트레스[1]가 있으며, 비정상적인 신체구성으로 인하여 질병과 관련된 다양한 문제가 제기되고 있다. 일반적으로 비만은 다양한 질병과 관련이 있으며, 특히 젊은 여성들의 비만은 불임, 다낭성난소증후군, 그리고 무월경과 같은 생식기 질환을 유발하여 고통받게 한다[1,2]. 한편, 월경이란 주기적으로 분비되는 호르몬에 의해 자궁내막이 증식하여 배아의 착상 준비를 유발하며, 착상이 발생하지 못하면 자연적으로 자궁내막이 탈락되는 현상이다. 이는 자궁에서 단독으로 일어나는 것이 아니라 시상하부의 신경물질에 의해 뇌하수체에서 생식샘자극호르몬이 분비되고 난소에서 배란이 되어 에스트라디올과 프로게스테론이 생성되어 자궁내막에 작용하여 주기적인 변화를 일으키게 된다. 스트레스와 비만은 월경주기에 부정적인 영향을 주게 되는데, 특히 시상하부에 부정적으로 작용하여 불안, 우울, 영양장애는 물론 무월경에 영향을 주는 것으로 알려져 있다[3]. 이처럼 여성의 월경주기 조절은 외부환경 및 정신적인 요인에 의해 영향을 받을 수 있다[4-6]. 그리고 영양부족으로 인한 체중 및 체질량지수의 감소는 월경이상과 신경내분비 이상의 원인이 되지만[7], 반대로 비만으로 인한 생식기 이상의 관계는 대부분 월경이상으로 나타난다[8]. 비만으로 인한 인슐린의 부정적 효과는 근육, 지방조직, 그리고 간과 같은 말초조직들의 생리학적 대사에 이상이 나타난다.
한편, 비만과 관련이 높은 leptin, adiponectin, 그리고 RBP-4와 같은 adipokine 인자들의 수준은 남성보다 여성에서 더욱 높은 수치를 보이고 있으며[9-14], 이는 estrogens에 의해 분비가 촉진되는 것으로 보고되고 있다[9,10,14]. 또한 몇몇 adipokine 인자들은 생식 기능을 중재하고, pituitatry-ovary-axis에 간접적인 영향과 난소 수용기 활동에 직접적인 영향을 주는 것으로 알려져 있다[15]. 뇌하수체에서 leptin과 adiponectin 수용기의 활성은 성선자극호르몬에 영향을 준다[14,16]. 반면 높은 leptin 농도는 난소 스테로이드 합성에 악 영향을 준다[15]. 선행연구와 같이 성선자극호르몬 그리고 난소 호르몬에 대한 adipokine의 분비는 긍정적이거나 부정적인 피드백이 작용한다. 즉, 월경주기 중에 adipokine 분비 변화의 평가는 상반될 수 있다.
운동대사와 관련된 연구들은 대상자들에게 에스트라디올과 프로게스테론이 연구결과에 미칠 수 있는 영향을 최소화하기 위해 생리주기 중 호르몬 수준이 가장 낮은 난포기에 테스트를 받게 한다[17]. 또한 여성들의 운동에 대한 생리적 반응에 있어 난소 호르몬에 영향을 받는 것에 대한 이해의 부족과 추가 연구의 필요성을 강조하였다. 최근 연구에 의하면 운동 여성의 41.7%는 생리주기가 운동 훈련과 수행에 부정적인 영향을 미친다고 보고하고 있다[18]. 일반적으로 대사증후군 또는 비만과 관련하여 adipokine 수치와 상관관계가 있음이 증명되었으며[19], 신체활동 또는 운동은 항염증 인자를 향상시키고 염증 유발인자를 감소시킴으로써 adipokine profile을 긍정적으로 변화시킨다고 보고하고 있다[20-22]. 따라서 본 연구는 여대생들을 대상으로 생리주기(여포기, 황체기)에 따른 혈청 adipokine의 수준을 알아보고, 규칙적인 운동이 생리주기에 따른 adipokine의 변화에 어떠한 영향을 주는지 알아보고자 실시하였다.
연구 방법
1. 연구 대상
본 연구의 대상자는 C시에 거주하고 있는 여대생(n=30)으로 최근 6개월간 운동경험이 없고, 본 연구의 목적에 대한 설명을 이해하고 동의한 여대생으로 실시하였다. 연구대상자들의 포함기준은 체지방률이 30% 이상이면서 BMI는 평균 24.0±3.99이었으며, 다른 의학적 질병이 없는 대상자들로 분석하였다. 선정된 대상자들은 여포기 그룹(n=15)과 황체기 그룹(n=15)으로 각각 분류하였으며, K대학 생명연구윤리위원회(IRB: 2017-05-003-003)의 승인을 얻어 개인의 안전보장은 물론 권리 등에 대한 지침을 적용하여 실시하였다. 대상자들의 신체적 특성은 Table 1과 같다.
2. 실험방법
1) 신체구성
신체조성 검사는 체성분분석기(Inbody 720, bio space, Korea)를 이용하여 신장(cm), 체중(kg), 체질량지수, %fat, WHR을 측정하였다.
2) 혈액검사
모든 대상자들은 10시간 이상 공복 상태를 유지하여 안정 시 주정맥을 통해 약 5 mL tube에 채혈하였다. 채혈 전 설문지를 통해 개개인의 월경주기를 확인하여 여포기 채혈그룹과 황체기 채혈그룹으로 구분하여 약 10일 간격을 두고 각각 채혈하였으며, 분석 전까지 -80℃에 보관하였다. 혈액분석은 혈장과 혈청에서 지질성분(TC, TG, HDL-c, LDL-c)과 adipokine (leptin, adiponectin) 인자들을 분석하였다. 총 콜레스테롤(TC), 중성지방(TG), 고밀도지단백콜레스테롤(HDL-c), 저밀도지단백콜레스테롤(LDL-c)은 일본 Hitachi Electronics사의 Hitachi 7600-110/7170 측정장비와 일본 Eiken Chemical사의 SICDIA L TCHO Reagent 시약과 스위스 Roche사의 시약을 사용하여 Enzymatic colorimetry 원리를 사용한 자동분석법을 이용하여 분석하였다. Adiponectin과 leptin 분석은 ELISA 방식을 이용하여 각각(R & D system DY1065, R & D system DY398) 분석하였다.
3) 운동 프로그램
본 연구의 운동프로그램은 저항성운동으로 저항성운동에 가장 적합한 130 BPM 박자에 해당하는 음악과 함께 실시하였다. 1 RM의 50-65%에 해당되는 운동강도로 polar (M400)를 이용하여 총 운동시간 동안 하루 250-300 kcal를 소비할 수 있는 운동량으로 주 3회, 16주 동안(여성의 생리주기를 고려하여) 실시하였으며, 2주마다 운동강도를 재처방하였다. 구체적인 운동프로그램은 Table 2와 같다.
4) 자료처리방법
본 연구에서 얻은 자료는 SPSS PC Windows version 23.0 통계 package를 이용하여 모든 측정항목에 대한 평균과 표준편차를 산출하였다. 모든 변인들은 그룹 간(2)×시기 간(2) 2 way ANOVA를 실시하였으며, 그룹과 시기 간에서 각각 유의성이 나타날 경우 독립검증과 대응검증으로 사후검증을 실시하였다. 모든 통계적 유의수준은 α=.05로 설정하였다.
연구 결과
1. 신체구성의 변화
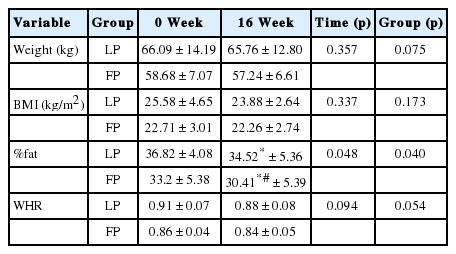
연구대상자들의 신체구성 변화에 대한 결과는 Table 3과 같다. 신체조성에 대한 그룹과 시기 간에 상호작용효과는 나타나지 않았다. 하지만, 황체기와 여포기 그룹 모두 %fat에서 규칙적인 저항성운동으로 0주에 비해 16주 후 유의하게 감소하였다(p<.05). 그리고 운동프로그램 이후 %fat에서 그룹 간 유의한 차이가 나타났다(p<.05).
2. 혈중 지질의 변화
연구대상자들의 혈중 지질성분에 대한 결과는 Table 4와 같다. 혈중지질성분에 대한 그룹과 시기 간에 상호작용효과는 나타나지 않았다. 하지만 TC에서 규칙적인 저항성운동프로그램으로 두 그룹 모두 0주에 비해 16주 후 유의하게 감소하였다(p <.05). 하지만 다른 모든 인자는 통계적으로 유의한 차이가 나타나지 않았다.
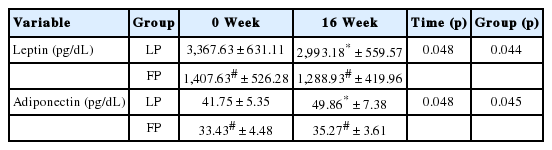
3. Adipokine 인자들의 변화
연구대상자들의 adipokine 인자들에 대한 변화는 Table 5와 같다. Adipokine 인자들에 대한 그룹과 시기 간에 상호작용효과는 나타나지 않았다. 하지만, leptin 농도의 경우 그룹 간 비교에서 여포기에 비해 황체기 그룹이 유의하게 높게 나타났으며(p <.05), 황체기 그룹에서는 0주에 비해 16주 운동프로그램 이후 유의하게 감소하였다(p<.05). Adiponectin 농도 역시 여포기에 비해 황체기 그룹이 유의하게 높게 나타났다(p<.05). 황체기 그룹에서 0주에 비해 16주 운동프로그램 이후 유의하게 증가하였다(p<.05).
논 의
본 연구는 비만 여대생들을 대상으로 저항성운동이 생리주기에 따른 지질성분과 아디포카인의 변화에 어떠한 영향을 미치는지 알아보기 위해 실시하였다. 그 결과 생리주기에 따라 지질성분의 차이는 없었으나, 아디포카인의 수치는 유의한 차이가 나타났다.
지질성분과 지단백 인자에 대한 생리주기에 따른 성호르몬과 관련하여 1980년대 연구에서는 상관이 높게 영향을 미치는 것으로 알려져 왔으나[23-25], 이후 장비 및 실험기술의 발달에 따라 1990년대 연구에서는 생리주기에 따른 지질과 지단백 농도에 영향을 미치지 않는 것으로 나타났다[26-30]. 본 연구 결과 역시 여포기와 황체기 지질성분 농도 수준은 두 그룹 간에 유의한 차이가 나타나지 않았다. 즉, 지질 또는 지단백의 농도 수준은 생리주기에 따른 성호르몬 농도와 직접적이든 간접적이든 관련이 없는 것으로 사료된다. 그리고 저항성운동은 총 콜레스테롤 수치에서 두 그룹 모두 유의한 감소가 나타나 저항성운동의 효과는 두 그룹 모두 동일하게 나타났다. 이는 저항성운동으로 인한 지질성분의 긍정적 효과는 동일하게 나타나는 것으로 사료된다.
한편, 여성의 생리주기 동안 호르몬 분비의 효과는 배란에 의한 효과뿐만 아니라 음식섭취와 식욕에도 유의한 영향이 있으며[31], 증가된 에너지 소비와 섭취는 황체기에서 마른 여성의 호르몬 분비를 균형적으로 잘 유지하는 것으로 보고되고 있다[32]. 일반적으로 순환 leptin의 수준은 남성보다 여성에서 약 2-3배 정도 높게 나타난다[33]. 이는 leptin의 수준이 hypothalamic-pituitary-gonadal axis에 대한 효과로 인하여 여성 생식기에 중요한 역할을 수행하기 때문이다[34]. 황체형성호르몬 농도는 순환 leptin 수준과 비례하며, 생식 기능의 조절에서 leptin의 역할을 제공한다[35]. 게다가 혈장 leptin은 estradiol과 progesterone 농도 중 어느 것에도 영향을 받지 않는다는 연구[36]와 그렇지 않은 연구로 상반된다[37]. 그러나 여포기와 황체기 사이 leptin 농도의 변화는 testosteron과 17-OH progesterone 농도뿐만 아니라 다른 인자들과의 관련이 제기되고 있다. 즉, leptin은 월경 중에 호르몬 변화뿐만 아니라 성활동 조절에 역할을 하는 것으로 여겨지고 있다. 다시 말해 Wyskida et al. [38]의 연구에 의하면 생리주기 단계에 따라 대부분의 adipokine 인자들이 안정적인 수준으로 나타나지만, leptin과 vaspin의 경우 다른 주기에서보다 황체기에서 높게 나타나는 것으로 보고하고 있다. 본 연구결과 선행연구와 같이 여포기보다 황체기에서 leptin의 수준이 높게 나타났으며, 저항성운동은 생리주기와 관계없이 긍정적인 효과가 나타났다. 인체 혈장 총 단백질의 약 0.01%로 설명되는 adiponectin은 지방에 의해 광범위하게 분비되며, 혈중에서 순환하는 것으로 알려져 있다[39]. 비만과 인슐린 저항성은 낮은 adiponectin 농도와 관련이 있으며, 남성보다 여성에서 더 높은 농도를 나타내는데, 이러한 이유는 adiponectin은 생식선 스테로이드에 의해 분비되기 때문으로 알려져 있다[39-42]. 많은 연구에 따르면 황체기에서 혈장 adiponectin 농도는 순환 estradiol 수준과 17-OH progesterone 농도와 반비례 관계를 나타내고 있다[43-46]. 다시 말해 여성의 월경주기 동안 adiponectin의 수준은 성호르몬 활동과 반대적인 효과를 보고하고 있으며, 또한 순환하는 adiponectin 농도와 허리둘레는 반비례적 관계를 나타낸다[47].
운동과 adipokine 인자들의 선행연구를 살펴보면, 유산소성 운동은 letpin과 adiponectin 농도에 긍정적인 영향을 주는 것으로 알려져 있으며[48], 특히 최근에는 저항성운동에 대한 연구가 활발히 진행되고 있다[49]. 또한 저항성운동은 선행연구들에 의해 adipokine 인자들의 긍정적 변화를 보고하고 있으며[50,51], 최근 연구에 의하면 저항성운동으로 뇌기능 및 뇌신경가소성에 긍정적인 효과를 보고하고 있다[52].
본 연구에서 생리주기에 따른 황체기와 여포기의 adiponectin 농도에서 유의한 차이가 나타났으며, 저항성 운동은 두 그룹 모두 유의하게 adiponectin 농도를 증가시켰다. 이는 생리주기 중 황체기에서 높은 농도가 나타나는 선행연구와 동일하며, 저항성운동으로 인한 효과는 생리주기와 관계없이 긍정적으로 나타남을 보여준다.
결 론
본 연구는 비만 여대생들을 대상으로 생리주기에 따라 저항성운동이 지질성분과 아디포카인에 미치는 영향을 조사한 결과 다음과 같은 결론을 얻었다. 여포기와 황체기 모두 체지방률의 유의한 감소가 나타났다. 그리고 아디포카인과 leptin은 황체기에서 유의하게 높게 나타났으며, 규칙적인 저항성운동은 leptin의 수준을 유의하게 감소시켰다. 또한 adiponectin 역시 황체기에서 유의하게 높게 나타났으며, 규칙적인 저항성운동은 adiponectin의 수준을 유의하게 증가시켰다. 따라서 여포기보다 황체기에서 adipokine의 농도가 높게 나타나, 여성들에게 있어 생리주기에 따라 채혈시기를 동일하게 하는 것이 매우 중요함을 시사한다. 또한 규칙적인 저항성운동은 adipokine 농도에 효과적인 영향을 주는 것으로 판단된다.
Notes
논문 작성에 있어서 어떠한 조직으로부터 재정을 포함한 일체의 지원을 받지 않았으며, 논문에 영향을 미칠 수 있는 어떠한 관계도 없음을 밝힌다.