복합운동 및 올리브유 섭취가 비만초등학생의 건강체력, 심혈관질환 위험인자, 골밀도에 미치는 영향
Influence of Extra Virgin Olive Oil Supplement and Combined Exercise on Health-Related Physical Fitness, Cardiovascular Disease Risk Factors, and Bone Density in Obese Elementary Students
Article information
Trans Abstract
PURPOSE
The purpose of this study was to investigate the influence of combined exercise and extra virgin olive oil supplement on health-related physical fitness, cardiovascular disease risk factors, and bone density in obese elementary school students.
METHODS
The participants were 40 obese elementary students over 25 kg/m2 to BMI, 10 combined exercise with high olive oil supplement group (HO+CE), 10 combined exercise with low olive oil supplement group (LO+CE), 10 combined exercise with placebo group (PL+CE), and 10 placebo group (PL). The participants have performed the exercise program for 70 minutes a day and 3 times a week with aerobic and resistance exercise during 12 weeks. Also, high and low olive oil supplement group took in 25 g and 10 g respectively at the same time and place.
RESULTS
There were significant decreases in body fat to HO+CE compared with PL+CE (p<.05) and significant increase in muscle mass and muscular endurance compared with PL+CE (p<.05). However, there were no significant differences in body weight, BMI, muscular strength, and flexibility between groups. For cardiovascular disease risk factors, there is a significant difference to triglyceride, LDL-C, total cholesterol in HO+CE compared with PL+CE (p<.05) and there were significant differences to HDL-C significantly decreased in HO+CE compared with PL+CE (p<.05). There is no significant difference in bone density between groups (p>.05).
CONCLUSIONS
In conclusion, there were positive responses for body composition and cardiovascular disease risk factors for the twofold cases through combined exercise and high extra virgin olive oil supplement, but not for bone density.
서 론
신체활동의 감소와 음식섭취량의 증가를 통하여 나타나는 비만은 전 세계적으로 급격히 증가하여 심각한 보건문제로 대두되어지며, 특히 아동 및 청소년의 비만인구비율은 30%에 육박하고 있는 실정이다[1]. 더욱이 이러한 아동기 비만현상이 장기간 방치되어지면 치료 및 해소방법이 보다 어려워질 뿐만 아니라 심혈관질환이나 당뇨 등의 생활 습관병을 유발시킬 확률이 높아지는 것으로 보고되고 있다[2,3]. 특히 아동기 비만은 소아기부터 시작되어 지방세포 수의 증가를 유발하는 세포증식형 비만과 지방세포의 크기가 커지는 세포비대형 비만이 동시에 나타나 성인이 되어서도 비만이 계속 유지되기 쉬운 것으로 알려져 있기에[4,5] 아동기의 비만을 예방하는 방법이 중요한 것으로 보고 되고 있다[6,7].
비만을 예방하고 치료하는 방법은 다양하게 제시되어 식이요법, 약물요법, 수술요법 및 운동요법이 대중적으로 많이 적용되고 있지만, 특히 신체적 능력의 향상을 가져오는 운동요법이 부적 에너지균형을 가져오는데 탁월한 효과를 나타내는 것으로 알려져 있다[8,9]. 게다가 운동요법을 병행하지 않은 식이요법 또는 약물요법은 체중감량의 효과를 일시적으로 가져올 수 있지만 근육손실에 따른 기초대사량의 저하 및 제지방량의 감소현상을 가져오는 것으로 보고되고 있으며[10], 지속적인 신체활동의 수행 및 유산소성 운동과 저항성 운동은 신체질량지수, 체지방량, 제지방량, 혈압, 그리고 혈중지질 등의 개선효과를 가져오는 것으로 알려져 있다[11-13].
유산소성운동은 체지방 감량을 위해 가장 선호되어지는 운동형태로서 체지방을 직접적으로 연소시켜 지방대사를 활성화시키는 운동방법으로 혈중지질의 구성비율을 긍정적인 방향으로 향상시킴으로써 심혈관계질환의 예방 및 치료에 도움을 줌과 동시에 체중관리를 위한 운동으로 가장 권장되어왔다[13,14]. 이와 더불어 저항성 운동 또한 건강증진, 신체활성도 및 조직의 증대를 위하여 매우 효과적인 운동방법으로 선행연구를 통하여 제시되고 있으며, 근력운동의 경우 근육량 증가가 기초대사를 상승시켜 전체 에너지 소비량을 높이고 지방분해능력, 에너지 소비율, 제지방 조직, 지방질 이용 등의 증가를 통해 혈중지질 및 신체조성에 긍정적인 효과를 미치는 것으로 보고 되고 있다[15,16].
비만은 골밀도와 부적 상관관계를 보이며, 비만청소년의 경우 골밀도의 감소로 인하여 골절률이 정상체중 집단보다 높게 나타난다[17]. 지속적인 운동수행은 골질량과 골근력을 촉진시키기 때문에 골대사의 활발한 변화가 나타나는 아동기의 적극적인 활동은 매우 권장되며[18], 규칙적인 신체활동은 체중부하에 의한 자극을 통하여 골밀도에 긍정적인 효과를 가져오기 때문에 적절한 운동방법의 제시가 필요하다[19]. 따라서 운동효과의 극대화를 위해서는 부상의 방지와 함께 신체활동시 관절부위에 무리가 가지 않도록 하고, 관절의 가동범위와 근력을 증가시킬 수 있는 운동형태와 적절한 운동시간 및 운동강도를 설정하여 진행하는 것은 필요 요소 중의 하나이다. 골밀도를 증가시키기 위해서는 뼈에 중력부하와 함께 근수축의 자극이 이루어져야하며 Kang et al. [20]은 체중부하운동을 통하여 여성들의 요추 및 대퇴골의 골밀도가 향상된 결과를 보고하였고 걷기 및 조깅과 같은 유산소성 운동 또한 골밀도 감소 예방에 효과가 있는 것으로 보고되고 있다[21].
한편 신체활동과 함께 아동기의 정상적인 성장 발달을 꾀하기 위해서는 적절한 영양공급이 매우 중요함에도 불구하고 비만아동의 경우 편식, 패스트푸드, 불규칙적인 식사시간 등과 같은 잘못된 식습관으로 정상체중의 어린이와 비교하여 적절한 영양 공급이 이루어지지 않는 것으로 나타나고 있다[22]. 더욱이 이러한 불균형적인 영양섭취는 인슐린 감수성 저하 및 포도당의 지방전환으로 인한 혈중지질농도의 상승으로[23], 높은 중성지방수치와 저밀도 지단백 콜레스테롤(LDL-C)의 증가 현상과 같은 지질대사의 이상이 발생하여 고혈압, 고혈당과 더불어 대사증후군 발현에 직접적인 연관성을 보이게 된다[24].
올레인산이 풍부한 올리브유는 고밀도 지단백 콜레스테롤(HDL-C)은 증가시키고 LDL-C는 낮춰 고혈압이나 심장질환 등의 성인병 예방의 생리활성 효과가 있는데, 포화지방을 많이 섭취하는 지중해 연안 국가 사람들이 순환기질환이 적은 이유는 올리브유를 섭취하기 때문인 것으로 알려져 있다[25,26]. 또한, 올레인산과 더불어 리놀렌산은 면역기능의 향상과 함께 혈압저하 및 혈전증의 개선을 통하여 동맥경화 예방 및 항콜레스테롤의 효과 등을 가져온다[27,28]. 특히, 항산화 물질인 베타카로틴과 비타민 E가 함유되어 있는 엑스트라 버진 올리브유는 제조과정에서 정제하지 않고, 열을 가하지 않으며 압착하여 생산하기 때문에 동맥경화와 심장병 예방에 좋은 단일불포화지방산을 식물성 기름 중에서 가장 많이 함유하는 것으로 보고되고 있다[29]. 게다가 빠른 속도의 산화과정은 체지방으로 축적되지 않고 혈중중성지방 농도를 감소시키며, 체중과 내장지방량을 감소시킴으로써 비만예방 효과를 가져오게 된다[30]. Engel & Tholstrup [31]은 중년여성을 대상으로 올리브유 섭취를 실시한 결과 HDL-C의 증가와 LDL-C의 감소결과를 도출하였으며, Carnevale et al. [32]은 위약섭취군과 비교하여 올리브유 섭취집단에서 중성지방 및 총콜레스테롤 수치의 감소양상과 혈압의 개선효과를 보고하였다. 하지만 현재까지의 연구들은 올리브유의 유종 또는 섭취기간에 따른 심혈관질환 위험인자의 변화 등이 보고되었으며[33], 올리브유 섭취적정량에 대한 연구는 미흡한 실정으로 비만이 성인기까지 이어질 가능성이 높은 초등학생을 대상으로 올리브유가 건강 증진 및 비만의 예방에 미치는 영향에 관한 연구는 전무한 상황이다. 더욱이 올리브유 섭취와 복합운동의 병행처치가 비만의 미치는 영향에 관해서도 마찬가지로 잘 알려져 있지 않은 실정이다. 따라서 본 연구에서는 올리브유 섭취량의 조건을 달리함으로써 올리브유 섭취에 관한 적합한 지표설정의 제시와 함께 복합운동의 이중적 적용을 통하여 초등학생의 건강증진과 비만예방을 도모하는데 그 목적이 있다.
연구 방법
1. 연구설계 및 대상
본 연구는 서울시 소재 M초등학교에 재학하고 있는 남학생을 대상으로 하였으며 이들은 특별한 병력이나 건강상에 이상 또는 질병이 없고 체질량지수가 25 kg/m2 이상인 초등학생 40명으로, 고올리브유 섭취 및 복합운동군 10명(HO+CE 그룹), 저올리브유 섭취 및 복합운동군 10명(LO+CE 그룹), 위약섭취 및 복합운동군 10명(PL+CE 그룹), 위약섭취군 10명(PL 그룹)으로 구성하여 본 실험을 수행하였다. 연구자는 실험에 앞서 보호자 입회하에 모든 연구대상자에게 본 연구 및 실험 과정에 대하여 구체적으로 충분히 설명한 후 자발적으로 참여동의서 및 검사동의서를 작성한 피험자를 대상으로 본 실험에 착수하였다. 연구대상자의 신체적 특성은 Table 1과 같다.
2. 연구내용
1) 실험설계
본 실험에 앞서 모든 피험자들의 신체적 특성을 측정하였다. 피험자의 신장과 체중은 신장계와 체중계(BSM 330, Biospace, Korea)를 이용하여 측정였으며 체질량지수를 산출하였다. 체지방률과 근육량은 체성분 분석기(VENUS-5.5, Jawon Medical, Korea)를 이용하여 생체전기저항 방식으로 측정하였다. 또한 실험기간 동안 실험변인에 영향을 미칠 수 있는 약물복용 및 무리한 운동은 배제하도록 하였다. 본 실험에서 모든 피험자들은 4가지 그룹으로 나누어 12주간 운동프로그램을 수행시켰다. 모든 피험자는 주당 3회, 총 운동시간은 70분으로, 준비운동과 정리운동 각 10분, 본 운동은 유산소성운동과 저항성운동 복합 형태로 50분간 실시하였다. 준비운동은 구령에 맞춘 맨손체조를 실시하였고 정리운동은 스트레칭으로 마무리하였으며 모든 피험자는 운동프로그램 적용 전후 건강체력, 심혈관질환 위험인자, 골밀도 분석을 실시하였다.
2) 복합운동프로그램
본 연구에서는 유산소성운동과 저항성운동을 통한 복합형태의 운동프로그램을 적용시켰다. 유산소성운동은 자전거타기, 트레드밀, 줄넘기운동을 적절한 시간에 배정하여 지루하지 않게 유지될 수 있도록 진행하였다. 유산소성운동의 강도는 목표심박수 공식을 이용하여 개인별 최대심박수의 40-60%의 저강도에서 중등강도 수준 강도로 설정하였으며 목표심박수는 심박수 측정기(Polar)를 착용하여 유지 및 확인하였다. 저항성운동은 탄성밴드를 이용하여 전신근육을 강화시키는데 초점을 맞춰 진행하였다. 탄성밴드의 탄성력은 1-4주는 노란색, 5-8주는 빨간색, 9-12주는 파란색 밴드를 선택하여 각 동작을 한 세트 당 10-12회 실시하였다[34]. 운동강도는 Borg의 주관적 운동강도(Rating of Perceived exertion, RPE)에 따라 1-4주 기간은 RPE 11-12, 5-8주 기간은 RPE 13-14, 9-12주 기간은 15-16으로 점차적으로 증가시켜 진행하였다. 본 실험에서 이용한 구체적인 운동프로그램은 Table 2에 제시된 바와 같다.
3) 올리브유 섭취방법
모든 피험자들은 매일 일정한 시간에 동일한 장소에 모이게 하여 엑스트라 버진 올리브유와 위약을 거부감이 발생하지 않도록 음료에 희석시켜 섭취시켰다. 미국 FDA기준(2018)에 따른 올리브유 권장량은 하루 23 g이며, 평상시 섭취하는 음식물 속에도 올리브유 성분이 중복 복용되어질 수 있는 부분을 고려하여 본 연구에서는 Tirosh et al. [35]이 사용한 방법에 따라 고올리브유 섭취군과 저올리브유 섭취군은 매일 각각 25 g, 10 g의 올리브유를 섭취시켰다. 음식섭취는 평상시와 다르지 않게 식생활 패턴을 유지하게 하였으며, 모든 피험자에게 올리브유 투여 방법 및 섭취가 인체내 기능에 미치는 영향에 대하여 인지할 수 있도록 자세히 설명하였다.
3. 측정변인 및 방법
1) 건강체력
건강체력의 하위요인으로는 근력, 근지구력, 유연성, 그리고 신체조성을 측정하였다. 근력은 악력을 측정하였으며, 근지구력은 윗몸일으키기, 유연성은 좌전굴을 측정하였다(TKK 5403, Takei, Japan). 피험자의 신장과 체중은 신장계와 체중계(BSM 330, Biospace, Korea)를 이용하여 측정한 후 체질량지수(BMI)를 산출하였으며, 체지방률과 근육량은 체성분 분석기(VENUS-5.5, Jawon Medical, Korea)를 이용하여 생체전기저항 방식으로 측정하였다.
2) 심혈관질환 위험인자
모든 피험자는 채혈 전 최소 9시간 이상 공복상태를 유지하도록 하였으며, 실험 당일 채혈 전 약 30분간의 신체의 안정화 시간을 가진 후 1회용 주사기를 이용하여 전완정맥에서 약 10 mL의 혈액을 채취하였다. 채취된 혈액은 4℃에서 약 30분간 보관 한 후 원심분리기를 이용하여 3,000 rpm에서 혈장을 분리한 후 동결과정을 거치지 않고 분석을 실시하였다. 심혈관질환 위험인자 측정항목은 중성지방, 고밀도 지단백 콜레스테롤, 저밀도 지단백 콜레스테롤, 총콜레스테롤로, 지질성분 진단용 키트와 건식 생화학 분석기(EKTACHEM DT 60 II system, Johnson & Johnson, US)를 이용하여 분석하였다.
3) 골밀도
골밀도분석은 두 개의 에너지를 갖는 X-ray 또는 동위원소를 이용하여 골조직을 투과한 후 검출하는 정도로 골밀도를 측정하는 방법인 DEXA(Technical Insights Co., US)를 이용하여 상완부위, 대퇴부위, 요추부위를 측정하였으며 단위는 g/cm2로 나타내었다.
4. 통계처리
본 연구에서 측정된 자료는 WIN/SPSS Version 22.0 program을 이용하여 모든 자료의 평균과 표준편차를 산출하였으며, 복합운동 프로그램 및 올리브유 섭취에 따른 건강체력, 심혈관질환 위험인자, 그리고 골밀도의 변화차이는 Two-way ANOVA with repeated measures를 사용하였으며 사후검증으로는 Bonferroni를 실시하였다. 분석을 위한 모든 통계적 유의수준은 p<.05로 설정하였다.
연구결과
1. 건강체력의 변화
12주간의 올리브유 섭취수준에 따른 복합운동프로그램 참여를 통한 그룹별 건강체력의 변화는 Table 3에 제시된 바와 같다. 측정시기간의 체중, 체질량지수, 근력, 유연성의 변화는 사전측정과 비교하여 PL 그룹을 제외한 모든 집단에서 유의하게 감소하였지만(p <.001), 각 그룹 간에는 차이가 나타나지 않았다(p>.05). 반면, 사전측정과 비교한 측정시기간 체지방률의 변화는 PL 그룹과 비교하여 모든 그룹에서 유의하게 감소하였으며(p <.05), 특히 HO+CE 그룹은 PL+CE 그룹과 비교하여 유의한 감소 결과를 나타내었다(p<.05). 근육량의 변화에 있어서는 PL 그룹과 비교하여 모든 그룹에서 유의하게 증가하였으며(p<.05), HO+CE 그룹은 PL+CE 그룹과 비교하여 유의한 증가결과를 나타내었다(p <.05). 또한, 근지구력에 있어서도 측정시기간에 PL그룹을 제외한 모든 집단에서 유의한 증가 결과를 가져왔으며(p <.05), 특히 HO+CE 그룹에서 측정시기간 가장 높은 증가율을 나타내었다. 집단 간 차이에서는 HO+CE 그룹은 PL 그룹과 비교하여 유의하게 증가하는 결과를 나타내었다(p <.05). 체지방률에 대한 사후분석 결과 PL 그룹이 PL+CE, LO+CE, HO+CE 그룹 간 유의한 차이가 나타났고(p<.001), HO+CE< LO+CE<PL+CE<PL 순으로 체지방률이 낮게 나타났으며, PL+CE, LO+CE, HO+CE 세 그룹 간에서는 유의한 차이가 나타나지 않았다. 또한, 근육량에 대한 사후분석 결과 PL 그룹이 나머지 세 그룹 간 유의한 차이가 나타났고(p <.001), HO+CE 그룹과 PL+CE그룹 간에서도 유의한 차이가 나타났다(p <.001). 근육량은 HO+CE >LO+CE >PL+CE>PL 순으로 높게 나타났다. 마지막으로 근지구력에 대한 사후분석 결과 PL 그룹이 PL+CE, LO+CE, HO+CE 그룹간 유의한 차이가 나타났고(p <.001), HO+CE =LO+CE>PL+CE>PL 순으로 근지구력이 높게 나타났다. 또한 PL+CE, LO+CE, HO+CE 세 그룹 간에서는 유의한 차이가 나타나지 않았다.
2. 심혈관질환 위험인자의 변화
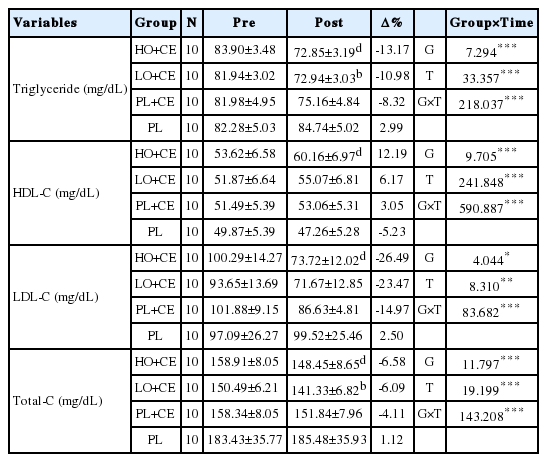
12주간의 올리브유 섭취수준에 따른 복합운동프로그램 참여를 통한 그룹별 심혈관질환 위험인자의 변화는 Table 4에 제시된 바와 같다. 측정시기에 따른 중성지방 및 총콜레스테롤의 변화는 PL 그룹을 제외한 모든 집단에서 유의하게 감소하였음을 알 수 있었고(p <.05), HO+CE 그룹에서 가장 큰 감소율을 나타내었으며, 집단 간 차이에서도 HO+CE 그룹은 PL+CE 그룹 및 PL 그룹과 비교하여 유의하게 감소하였다(p <.001). 고밀도 지단백 콜레스테롤의 변화에 있어서는 PL 그룹과 비교하여 모든 그룹에서 유의하게 증가하였으며(p <.05), HO+CE 그룹은 PL+CE 그룹과 비교하여 유의한 증가결과를 나타내었다(p <.001). 또한, 저밀도 지단백 콜레스테롤에 있어서도 측정시기간에 PL그룹을 제외한 모든 집단에서 유의한 감소결과를 가져왔으며(p<.05), 집단 간 차이에서는 HO+CE 그룹은 PL 그룹과 비교하여 유의하게 감소하는 결과를 나타내었다(p<.05).
중성지방에 대한 사후분석 결과 PL 그룹이 PL+CE, LO+CE, HO+CE 그룹 간 유의한 차이가 나타났고(p<.001), HO+CE<LO+CE<PL+CE<PL 순으로 중성지방이 낮게 나타났다. 또한 PL+CE, LO+CE, HO+CE 세 그룹 간에서는 유의한 차이가 나타나지 않았다. 고밀도 지단백 콜레스테롤에 대한 사후분석 결과 PL 그룹이 PL+CE 그룹과는 유의한 차이가 나타나지 않았고, LO+CE, HO+CE 그룹 간에서는 유의한 차이가 나타났으며(p<.05, p<.001), HO+CE>LO+CE>PL+CE>PL순으로 고밀도 지단백 콜레스테롤이 높게 나타났다. 또한 PL+CE, LO+CE, HO+CE 세 그룹 간에서는 유의한 차이가 나타나지 않았다. 저밀도 지단백 콜레스테롤에 대한 사후분석 결과 PL 그룹이 PL+CE 그룹과는 유의한 차이가 나타나지 않았고, LO+CE, HO+CE 그룹 간에서는 유의한 차이가 나타났으며(p <.01), LO+CE <HO+CE <PL+CE<PL 순으로 저밀도 지단백 콜레스테롤이 낮게 나타났다. 또한 PL+CE, LO+CE, HO+CE 세 그룹 간에서는 유의한 차이가 나타나지 않았다. 총콜레스테롤에 대한 사후분석 결과 PL 그룹이 PL+CE, LO+CE, HO+CE 그룹 간 유의한 차이가 나타났고(p <.01), LO+CE<HO+CE<PL+CE<PL 순으로 총콜레스테롤이 낮게 나타났다. 또한 PL+CE, LO+CE, HO+CE 세 그룹 간에서는 유의한 차이가 나타나지 않았다.
논 의
본 연구에서는 올리브유 섭취 및 복합운동프로그램 수행이 비만초등학생의 체력 및 생활습관병 요인에 미치는 영향을 분석하였으며, 그 결과 비만초등학생에 있어 고올리브유 섭취는 건강체력 및 심혈관질환 위험인자 개선에 긍정적인 효과를 나타냈다.
근육, 뼈, 각종 내장기관, 무기질, 체수분을 포함하는 제지방과 필수지방산, 저장지방으로 분류되는 체지방으로 구분되는데[36,37] 이러한 신체조성에 있어 본 연구에서는 비만초등학생의 올리브유 섭취 및 복합운동에 따라 그룹별 체지방률, 근육량에서 유의한 차이가 나타났다. 고올리브유 섭취와 복합운동을 실시한 초등학생은 위약섭취 및 복합운동을 수행한 집단과 비교하여 체지방률(23.93±1.05% vs. 25.35±1.63%), 근육량(25.81±1.21 kg vs. 22.77±1.81 kg)에 있어 유의하게 긍정적인 변화를 나타내었다. 이러한 결과는 상대적으로 체지방에 비해 근육량이 급격히 증가하는 성장기 초등학생에 있어 유산소성 운동과 저항성 운동이 혼합된 복합운동이 근육량의 증가와 이에 따른 기초대사량 증가에 긍정적인 영향을 가져다 준 것으로 보여진다[38]. 더욱이 Galvao et al. [39]은 41명의 여성을 대상으로 9주간 엑스트라버진 올리브유를 섭취시킨 결과, 통제군과 비교하여 섭취군에서 체지방의 유의한 감소를 가져온 것으로 보고하였고, 비만치료로서 올리브유 섭취가 에너지 제한 다이어트 프로그램에 포함할 것을 강조하여 본 연구의 결과와 일맥상통하였다. 한편 규칙적이고 지속적인 운동은 유리지방산이 에너지원으로 사용되는 비율을 점차 높여 지방조직에서의 지방분해를 증가시킴으로써 혈중 유리지방산이 주된 에너지원으로 이용되는데[40], 신체활동 중 근육 내에 존재하는 당원의 분해를 통해 포도당과 혈중의 포도당을 포착하여 필요한 에너지원으로 이용하게 된다[41]. 더욱이 복합운동과 관련된 선행연구들을 살펴보면, Sousa et al. [42]은 여성을 대상으로 복합운동을 실시한 결과 제지방량의 증가와 더불어 체지방률이 감소한 것으로 보고하였는데, 이는 본 연구에서도 시도한 바와 같이 체지방을 효율적으로 제거하는데 효과적인 유산소성 운동의 적용과 비만도를 감소시키는데 유익한 운동방법인 저항성트레이닝이 가져온 결과라 생각된다. 또한, Jung et al. [43]은 복합운동프로그램에서 체중, 체지방률의 유의한 감소를 나타내었으며, 건강체력에 유의한 변화를 보고하였고, Kim [44]은 초등학생을 대상으로 12주간 유산소운동과 근저항 복합운동을 실시한 결과 체지방률은 감소하였으며, 제지방은 증가되었음을 보고하였다.
건강체력 중 근지구력은 반복적인 근수축이 장시간 요구되어지는 중요한 요인 중의 하나로서 코어운동프로그램과 같은 저항성운동을 통하여 강화되어지는 것으로 보고되어진다[45]. 본 연구에서는 12주간의 복합운동을 수행한 이후에 근지구력은 고올리브유 섭취 및 운동그룹에서 29.1% 증가하였으며, 선행연구에 의하면, 올리브유에 함유된 베타카로틴은 유해산소가 세포를 손상시키는 것을 막는 강력한 항산화 성분으로 혈액 공급과 영양성분 공급이 원활하게 되고 근육도 이완시켜주는 역할을 하여 장시간 운동에 의한 근육경련을 막는 효과가 있고[46], 지속적이고 점진적인 운동부하의 자극은 근육의 수축과 이완을 반복시켜 근위축을 예방하며, 근지구력 증가에 효과를 가져오게 된다[47]. 현재까지의 연구들에서는 아직 올리브유 섭취수준에 따른 근지구력의 변화에 대한 보고가 이루어지지 않았으나, 신체활동과 올리브유 섭취를 실시한 결과 대조군에 비하여 근지구력이 유의하게 증가되는 것으로 보고되고 있다[48]. 초등학생 연령대의 성장기 아동에게 있어 체력은 매우 중요하고, 기본적인 요소이며, 신체활동은 이러한 체력향상을 위한 필수적인 부분이다[49]. Ha & Baek [50]은 초등학생을 대상으로 16주간의 복합운동을 통하여 체력요소 중, 근지구력에서 비만집단의 유의한 증가결과를 보고하였다. 스트레칭 등을 통하여 향상되어지는 체력인 유연성은 관절의 가동범위를 넓혀주고, 근골격계의 손상 위험률을 감소시켜 주며[51], 신체부위별 운동 시 저항무게를 다양하게 증감할 수 있다는 장점과 더불어 운동부위 또한 여러 부위를 이용하여 점진적 저항으로부터 나타나는 손상된 부위의 근육을 강화시켜 줌으로써 유연성을 향상시켜 주는 것으로 알려져 있지만[52], 본 연구는 피험자의 연령대가 낮은 초등학생인 점을 감안하여 부상위험이 적은 웨이트 트레이닝 장비와 탄성밴드운동을 적용시켰으나 유연성 항목에서는 그룹간 유의한 효과가 나타나지 않았다.
한편 심혈관질환의 주요 위험인자인 혈중 콜레스테롤은 혈중지질요소 중 하나이며, 동맥경화증, 관상동맥 질환과 같은 고지혈증을 유발하는데[53], 소아비만의 여부에 따라 혈중지질의 차이가 나타나고, 비만도가 높을수록 정적 상관관계를 보이며, 초등학교 시기의 수준이 성인으로 이어질 확률이 매우 높은 것으로 보고되고 있다[54]. 신체활동은 중성지방, 총콜레스테롤, 저밀도지단백 콜레스테롤 수준은 감소시키고, 고밀도지단백 콜레스테롤 수준을 증가시켜 인체에 긍정적인 변화를 나타내며[55,56], 올레인산이 풍부한 올리브유의 경우에도 고밀도지단백 콜레스테롤을 증가시키고, 저밀도지단백 콜레스테롤은 낮춰주는 효과를 가져온다[57]. 본 실험에서도 고올리브유 섭취 및 복합운동을 실시한 그룹은 중성지방, 총콜레스테롤, 저밀도지단백 콜레스테롤의 감소와 고밀도지단백콜레스테롤의 유의한 증가를 나타냈다. 선행연구를 살펴보면, Ka et al. [58]은 초등학생을 대상으로 12주간의 신체활동 프로그램을 실시하게 한 결과, 중성지방과 저밀도지단백 콜레스테롤에서 유의한 개선효과가 나타났다고 보고하였고, Venäläinen et al. [59] 또한 어린이를 대상으로 장기간의 운동을 통하여 혈중지질에 유익한 효과를 가져온 것으로 보고하였다. 더욱이 Hernaez et al. [60]은 3주간의 올리브유 섭취를 통하여 고밀도지단백 콜레스테롤 수준의 향상 결과를 보고하였고, Maki et al. [61] 역시 엑스트라 버진 올리브유를 3주간 섭취시킨 결과 총 콜레스테롤과 더불어 저밀도지단백 콜레스테롤이 감소하였다. 그러므로, 본 연구에서 실시한 바와 같이 신체활동과 더불어 올리브유 섭취의 이중적 적용은 심혈관질환 위험인자의 긍정적인 변화를 유도하는데 있어서 협력작용을 꾀할 수 있을 것으로 사료된다.
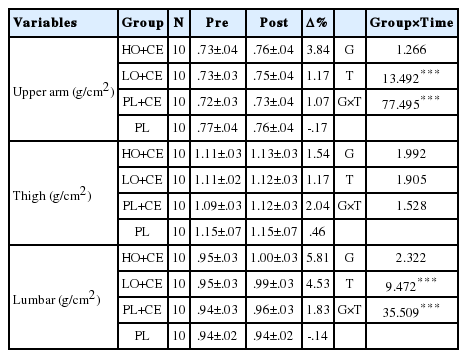
한편 골밀도는 골량을 나타내는 지표로서 무기질로 침착되어지는 성질을 가지고 있으며, 노화에 의해 소실되고, 환경적인 요인, 유전, 영양, 호르몬 등 여러 가지 상호작용의 영향을 받는다[62]. 장기간의 운동 부재는 골밀도를 감소시키고, 골형성은 조락하게 되어 건강상의 문제가 나타나게 된다[63]. 따라서 규칙적인 신체활동은 이러한 문제를 해결할 수 있는 대표적인 방안이라 할 수 있으며, 지속적인 운동은 골격근의 반복적인 수축으로 골의 피질량과 혈류량을 증가시켜 원활하게 혈액순환을 유지시킨다[64]. 운동은 뼈의 재생을 촉진하는 역할을 하지만 이러한 행위가 규칙적으로 수행되어지지 않거나 신체활동량이 적은 경우 뼈조직이 뼈생성 및 분해 간에 불균형이 발생하여 감소하게된다[65]. 유산소성운동과 저항성운동의 수행은 지방조직보다 제지방 조직 중 근육량의 증가현상을 통한 체력상승에 의하여 골밀도 향상에 기여하는 것으로 보고된다[66]. 선행연구에서 살펴보면, Byun & Kim[67]은 12주간의 음악줄넘기 실시를 통하여 요추부위 및 대퇴경부의 골밀도가 증가하였음을 보고하였고, 규칙적인 신체활동을 실시하게 되면 골질량에 긍정적인 효과가 있음을 강조하였으며, Cho & Kim [68]은 저항성 운동은 요부 신전근력 및 균형능력 향상을 통하여 골밀도가 증가되는 것으로 보고하였다. 따라서 체중부하운동은 골밀도를 증가시키기 위한 효과적인 방법으로서 인장력과 압축력의 영향으로 상완 및 요부, 특히 대퇴골두의 골밀도를 높여주는 것으로 알려져 있으나[69], 본 연구에서 실시한 복합운동은 상완, 대퇴, 요추 세 부위에서 골밀도가 증가하는 경향을 나타냈으며 상완과 요추 부위는 그룹과 시기 간에 상호작용 효과를 나타냈지만 사후분석 결과 그룹 간에는 통계적으로 유의한 증가를 나타내지는 못하였다. 이는 본 연구의 복합운동프로그램이 골밀도의 유의한 증가를 가져올 만큼의 고강도 운동 또는 체중부하운동형태에 미치지 않아 복합운동을 실시한 그룹 간의 차이를 보이지 않은 것으로 사료된다.
결론 및 제언
유산소성운동과 저항성운동을 병행한 복합운동과 고올리브유 섭취는 체지방률의 감소와 근육량 및 근지구력 증가, 중성지방, 저밀도지단백 콜레스테롤, 총콜레스테롤 수치 감소, 고밀도지단백 콜레스테롤 증가에 영향을 미치는 것으로 나타났다. 결론적으로, 비만초등학생을 대상으로 실시한 고올리브유섭취 및 복합운동의 시너지적 적용은 신체조성의 긍정적인 변화를 통하여 심혈관질환 위험요인을 개선시키며, 근지구력을 향상시키지만 골밀도에는 영향을 미치지 않는 것으로 보인다.
Notes
이 논문 작성에 있어서 어떠한 조직으로부터 재정을 포함한 일체의 지원을 받지 않았으며, 논문에 영향을 미칠 수 있는 어떠한 관계도 없음을 밝힌다
AUTHOR CONTRIBUTION
Conceptualization: K Kim, Data curation: K Kim and K Lee, Formal analysis: K Kim and K Lee, Funding acquisition: K Kim, Methodology: K Kim, Project administration: K Kim and K Lee, Visualization: K Kim and K Lee, Writing - original draft: K Km, Writing - review & editing: K Lee.