유방암 환자의 인지 손상에 미치는 운동 효과: 메타분석적 접근
Beneficial Effects of Exercise on Cancer-Related Cognitive Impairment with Breast Cancer Patients: A Systematic Review and Meta-Analysis
Article information
Trans Abstract
PURPOSE
Cancer-related cognitive impairment (CRCI) is exposed to cognitive impairments that interfere with their daily lives after a complete recovery. Exercise is one of the effective non-pharmacological treatments to prevent or improve cognitive function decline. This study evaluated the effects of exercise interventions on cognitive function improvement in CRCI breast cancer patients and searched the association of various aspects in which exercise affects cognitive function improvement.
METHODS
PubMed, ScienceDirect, ACS journal, and Google scholar databases from 1 January 2014 to 31 May 2021 were utilized for searching articles related to research purpose. Meta-analysis was conducted with Comprehensive Meta-Analysis 2.0 using the random-effect model.
RESULTS
A meta-analysis of seven studies showed that walking (ES=0.59, p=.000) was the most effective in improving cognitive function, and moderate-intensity (ES=0.60, p=.000) was more effective than moderate-to-high intensity (ES=0.27, p=.007) exercise in CRCI patients with breast cancer. Cognitive function improvement was observed in short-term exercise intervention for four weeks (ES=0.46, p=.038), and after that, it was found that the cognition improvement effect was maintained or improved through long-term (12 or 24 weeks) exercise. Moreover, the cognitive function of CRCI patients with breast cancer improved without supervision during exercise interventions (ES=0.39, p=.001).
CONCLUSIONS
Walking and moderate-intensity exercise can suppress cognitive impairment in CRCI patients with breast cancer. Personalized exercise prescription through short-term and long-term exercise periods can alleviate cognitive decline and improve the cognitive function of CRCI breast cancer patients. Exercise interventions without supervision also show a positive influence on cognitive function improvement.
서 론
항암 화학요법(chemotherapy) 및 호르몬 치료 중, 암환자의 최대 70%가 경험하고, 치료 후 약 60%가 지속적인 인지기능 저하를 호소하는 암 관련 인지기능저하(Cancer-related Cognitive Impairment, CRCI)는 항암치료의 일반적인 부작용이다[1-3]. 인지기능 저하는 암 환자의 삶의 질에도 치명적인 영향을 미치며 연구자들은 암환자와 인지기능 저하의 연관성에 찾기 위한 연구를 진행하고 있다[4-7]. 인지기능 저하 증상이 있는 암환자의 경우, 개인에 따라 6개월에서 최대 20년 이상 증상이 지속되므로 암 완치 후 이전 삶으로 복귀 시 일상생활의 어려움을 겪을 수 있다[8,9]. CRCI는 우리나라 여성암의 2위를 차지하는 유방암 환자에게 자주 발생되며 최대 75%가 인지기능저하를 경험하고, 경험자 중 약 35%가 장기간 지속되는 중증 인지장애를 경험한다[1,9,10]. CRCI의 유발원인에 대한 여러 추측이 있지만 그 치료법은 여전히 명확하게 밝혀지지 않았다[11,12]. National Comprehensive Cancer Network (NCCN)에서는 현재 CRCI 환자의 인지기능개선 치료법으로 비약물적 요법인 운동을 통한 인지기능개선 치료법을 권고하며 지속적인 운동참여를 권장하고 있다[13].
지속적인 운동은 심혈관 기능을 강화하고, 강화된 심혈관 기능을 통해 해마의 부피증가 및 신경세포생성 촉진과 연관되어 인지기능 저하를 완화하는 효과를 보인다[14-16]. 암 환자의 심혈관의 건강 수준이 인지기능개선을 위한 매개 요인이 될 수 있음을 시사한다. 특히 걷기운동은 심혈관 건강 향상과 에너지소비 수준 증가에 밀접한 관련이 있음에도 불구하고, 일반적인 암환자의 운동참여 수준은 치료 중과 후에 꾸준히 감소된다[17]. 항암치료과정에서 암환자가 겪게 되는 피로감, 무력감, 그리고 신체적 통증 등 치료과정 중 발생하는 다양한 요인들에 인해 지속적인 운동참여에 제한을 받기 때문이다[18]. 걷기운동은 단순하고 쉽게 접근할 수 있어 암환자들의 장기적 생활습관에 적용할 수 있는 운동유형으로 노인의 운동중재와 유사한 인지기능개선 효과를 보이며, 인지기능 관련 뇌영역의 용적 및 신경세포생성에 긍정적인 변화를 일으킨다[19-22]. 특히 유방암 환자의 걷기운동은 피로감, 정신건강, 신체건강, 그리고 생존율까지 크게 향상시켜 운동참여에 대한 장벽을 낮추고, 지속적인 운동참여를 통해 인지기능개선의 효과를 기대할 수 있다[23-25].
중강도 수준의 걷기운동이 CRCI 유방암 환자의 인지기능개선에 미치는 긍정적인 영향력이 보고되었고[26], 단기 운동중재의 긍정적 효과가 나타났는데, 중강도 수준의 단기 걷기운동프로그램을 통해 CRCI 유방암 환자의 기억력과 처리속도(processing speed) 능력이 향상되었다[27]. 이러한 연구보고는 건강한 중년과 노인의 인지기능에 미치는 단기 유산소운동효과와 유사한 결과로 CRCI 유방암 환자에게도 건강한 성인과 마찬가지로 짧은 기간의 중강도 걷기운동이 인지기능개선에 효과적인 영향력이 있음을 시사한다[28,29]. 단기운동 프로그램의 효과를 활용해 장기적 운동프로그램을 주저하는 CRCI 유방암 환자의 운동참여를 촉진할 수 있으며, 구체적 운동기간과 기간증가에 따른 인지기능변화를 검증함으로써 달성 가능한 운동프로그램의 뚜렷한 목표를 설정할 수 있을 것으로 예상된다.
운동 목표설정시, 운동감독자(supervisor)의 동반 유무도 CRCI 유방암 환자에게 중요한 요소가 될 수 있다. 고령자, 신체적 통증 또는 장애로 인해 보행이 불편한 경우, 감독하 운동을 통한 보행자세의 교정과 보행거리의 증가 등 신체적 기능 개선[30,31]의 유익함을 확인한 반면, 인지적 기능 측면에서 운동감독자의 동반 유무와 인지기능 변화의 연관성은 검증되지 않았다. 그러나 가정기반(home-based) 중강도 걷기 운동을 통한 CRCI 유방암 환자의 인지기능 개선의 영향력이 보고되면서[26], 인지기능 개선에 미치는 감독하 운동(supervised exercise)의 실효성에 대한 검토가 필요한 상황이다. 감독하 운동에 대한 부담이 암환자의 운동참여율 감소[32]에 기인하는 점을 볼 때, 이는 고용비용 등 경제적인 측면과도 연관되어 운동참여 지속성에 영향을 미칠 수 있으므로 운동 중 인지기능 변화 추이를 통한 감독하 운동효과를 검증할 필요가 있다.
따라서 본 연구는 암유형에 따른 운동유형, 운동강도, 운동기간 및 운동감독 요인이 CRCI 환자의 인지기능 변화에 미치는 영향력을 검증하였고, 유방암 환자에게 가장 효과적인 운동중재 프로그램을 확인하였다. 본 연구의 목적은 CRCI 유방암 환자의 인지기능 개선을 위한 가장 효과적이고, 경제적이며 실행가능성이 높은 운동프로그램 구성요소를 검증하는 것이다.
연구 방법
1. 연구 대상
1) 분석대상 문헌의 선정기준
CRCI 환자의 인지기능 개선을 위한 운동중재의 효과성을 검증하기 위해 2014년 1월부터 2021년 5월까지 해외에서 출간된 관련 학술지를 수집하였고, PICOS 프로세스 기준에 따른 운동실험연구를 선별하였다. 본 메타분석을 위한 연구선정기준은 ⑴ 해외에서 출간된 CRCI 환자 대상연구, ⑵ 운동중재 전과 후의 인지기능 측정연구, ⑶ 무작위 배정 임상시험 연구(Randomized controlled trial, RCT), ⑷ 온라인으로 무료열람이 가능한 문헌, 그리고 ⑸ 영문으로 작성된 문헌이었다. 본 연구를 위한 문헌의 선정과정은 Fig. 1과 같다.
2) 문헌 검색
본 연구 목적에 부합하는 개별문헌의 수집을 위해 PubMed (33개), ScienceDirect (3,161개), ACS journal (50개) 및 Google Scholar (17,000개) 등 네 가지 학술자료 검색 사이트를 활용하여 관련문헌을 검색하였다. 문헌검색에 사용된 주요단어는 ‘Cancer’, ‘Cognitive impairment’, ‘Exercise’, ‘Physical activity’ 및 ‘Randomized controlled trials’ 였으며 관련된 20,244편의 연구 중 선정기준에 만족하는 학술지 총 7편을 분석 대상으로 선정하였다.
2. 연구절차
1) 메타분석 자료수집
수집된 데이터의 코딩 및 분석을 위해 개별연구의 ⑴ 연구자, ⑵ 출간연도, ⑶ 실험집단의 운동중재 실시 전과 후의 인지기능 평균 측정값, ⑷ 표본크기, 그리고 ⑸ p-value를 사용하여 운동이 인지기능 개선에 미치는 전체 평균 효과크기를 암 유형에 따라 운동유형, 운동강도, 운동기간, 그리고 감독하 운동 요인에 따라 산출하였다. 자료코딩은 관련분야 박사 및 박사과정 3인의 검정과 협의를 통해 진행되었다.
2) 자료처리방법
본 연구에서는 Comprehensive Meta-Analysis (CMA version 2.0)프로그램을 사용하여 선정된 연구의 통합적 효과크기를 분석하였고, 표본의 특성 및 중재방법 등 서로 다른 개별연구의 결과를 일반화하기 위한 랜덤효과모형(random-effect model)을 이용하였다. 표준화된 평균차이(Cohen’s d)를 통해 통합된 효과크기를 산출하였으며, 표본수가 작을 경우 효과크기가 과대추정(Hedges & Olkin, 1985)되어 한쪽으로 쏠리는 편향이 발생할 수 있으므로 Hedges’g을 통해 교정된 값으로 변환하였다. 운동유형, 운동강도 운동기간, 암유형 및 운동지도자 동반 유무를 그룹별로 분류하여 그 효과성을 메타 ANOVA를 통해 비교 분석하였으며, 표본의 크기와 효과크기의 관계를 보여주는 펀넬도표(funnel plot)를 통해 본 메타연구에 사용된 연구들에 대한 출판편향 유무를 검증하였다.
연구 결과
1. 출판편향
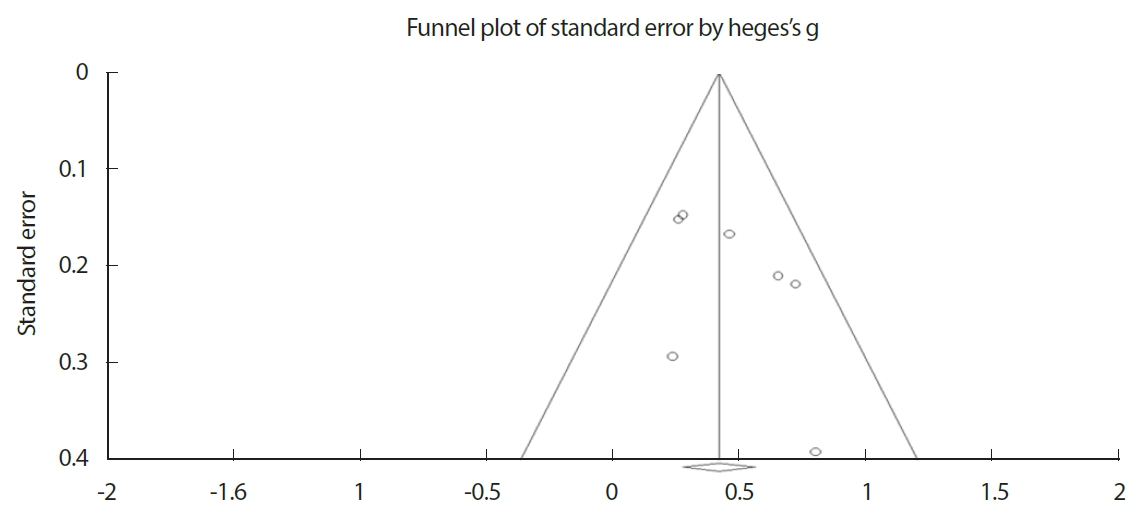
예상에서 벗어난 결과로 인해 의도적으로 출간되지 않은 연구가 존재하면, 출간된 논문들의 결과가 한쪽으로 편향되는 오류가 발생한다(Higgins & Green, 2011). 따라서 본 메타분석연구에서는 펀넬도표(funnel plot)를 사용하여 편향된 결과물로 인해 발생할 수 있는 비대칭 구조의 유무를 시각적으로 확인하였다. 본 연구의 절편(intercept)은 1.86737, 표준오차(standard error)는 1.25826, p=.19791 (2-tailed)로 나타났으며 이는 통계적으로 유의하지 않아서 출판편향이 존재하지 않은 것으로 확인하였다(Fig. 2).
2. 운동중재 프로그램의 전체 평균 효과크기
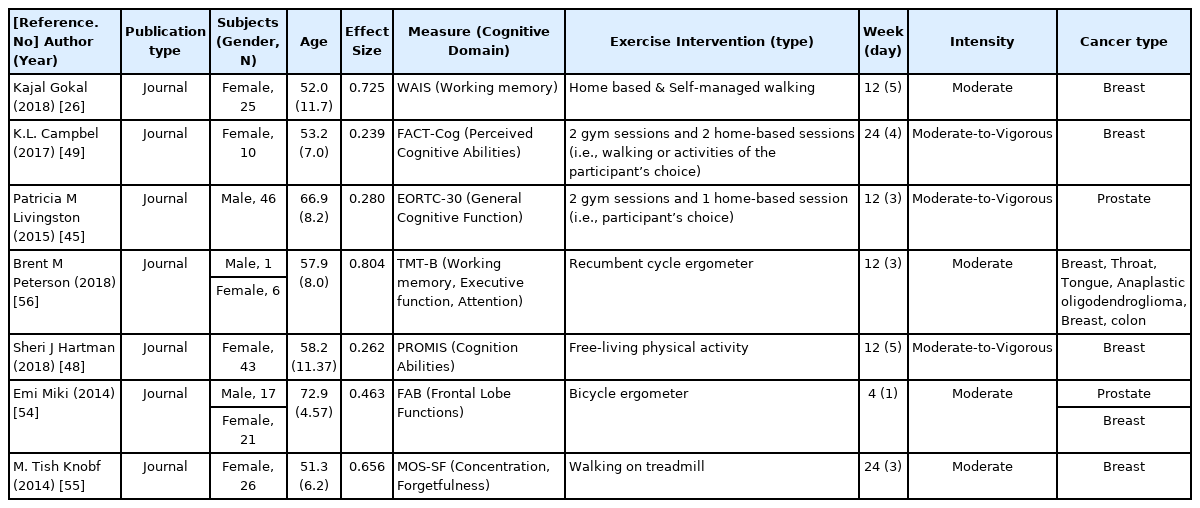
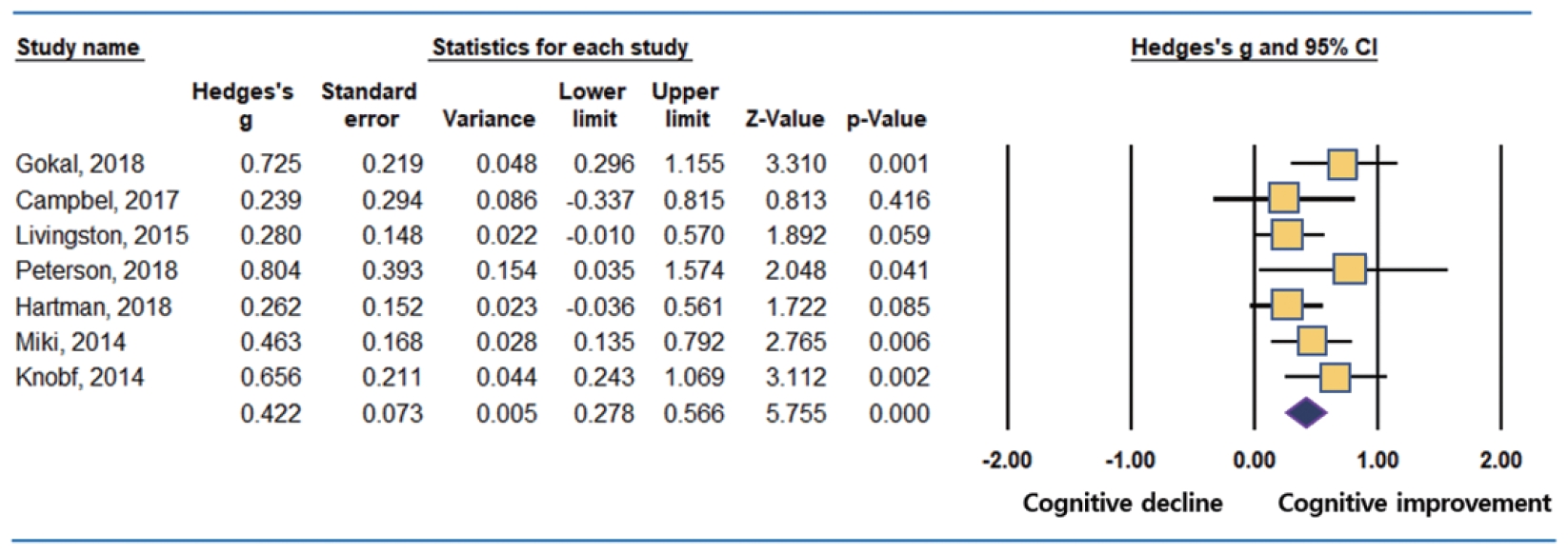
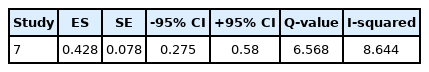
CRCI 환자의 인지기능 개선을 위한 운동기반 프로그램 중재의 효과성을 검증하기 위해 총 7편의 전체 평균 효과크기를 도출했다. 개별 연구의 특성과 효과크기를 제시한 forest plot은 Table 1 및 Figure 3과 같다. 박스의 중간지점은 효과크기를 나타내며, 박스의 크기는 연구의 정밀성(precision)을 나타내는 가중치(weight)를 표시한다. 박스의 크기를 통해 각 연구의 가중치 규모를 확인할 수 있고, 다이아몬드 모양은 연구 전체의 효과크기이다. Forest plot의 0을 기준으로 오른쪽 방향은 인지기능 개선효과가 있음을 나타내고, 왼쪽방향은 인지기능 개선효과가 없음을 나타낸다. 총 7편의 연구에서 랜덤효과 모형을 통해 분석된 운동중재프로그램의 전체 평균 효과크기(ES=0.43, 95% CI: 0.28-0.58, p=.00)는 통계적으로 유의하게 나타났으며, 평균 효과성은 중간 크기에 근접한 수준으로 CRCI 환자 인지기능개선에 긍정적인 영향력이 있는 것으로 확인하였다(Table 2).
3. 운동유형, 운동강도 및 운동기간에 따른 인지기능개선 효과크기의 변화
운동중재 프로그램에 따른 CRCI 환자의 인지기능개선 효과크기의 변화를 운동유형, 운동강도 및 운동기간별로 구분하고, 메타ANOVA를 통해 비교 분석하였다.
1) 운동유형에 따른 CRCI 환자의 인지기능개선
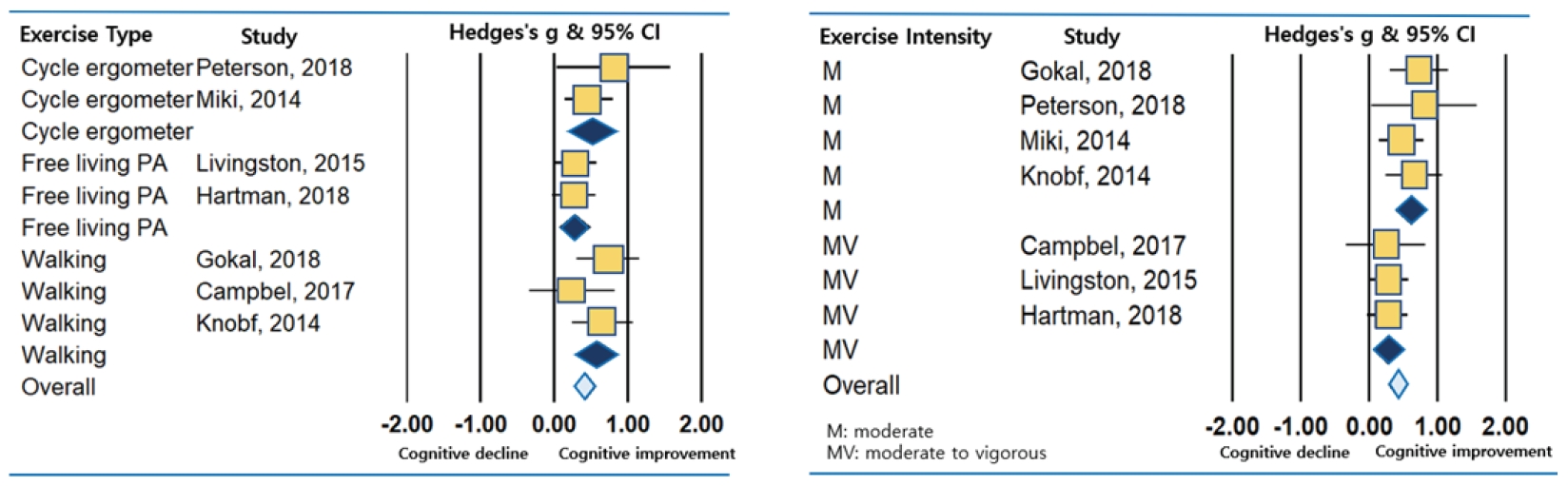
수집된 개별 연구의 CRCI 환자 대상 운동중재 프로그램의 운동유형은 ⑴ 걷기운동(walking), ⑵고정식 실내자전거 운동(indoor cycle ergometer), ⑶ 자율적 신체활동(free-living physical activity)으로 구성되어 있었다. 자율적 신체활동의 경우, 대상자에게 원하는 활동을 자율적으로 선택하도록 한 후 일정 기간 동안 가속도계 또는 자기보고식(self-reported) 방식을 통해 대상자의 신체활동 데이터를 수집하여 분석하였다. 세 가지 운동유형이 CRCI 환자의 인지기능개선에 미치는 영향력을 개별그룹으로 분류하여 메타ANOVA로 분석하였다(Table 3, Fig. 4). 각 운동유형으로부터 나타난 인지기능개선의 효과크기는 다소 차이가 있었지만, 연구가 진행된 운동유형에서 CRCI 환자의 인지기능 개선에 긍정적인 영향력을 나타냈다. CRCI 환자 인지기능개선에 가장 높은 효과크기를 보인 운동유형은 걷기(ES=0.59, p=.000)로 중간수준 이상의 인지기능개선 효과를 보였으며, 그 다음으로는 고정식 실내자전거(ES=0.52, p=.001), 자율적 신체활동(ES=0.28, p=.011)순이었다. 특히, 걷기 그룹은 고정식 실내자전거(d=0.1) 및 자율적 신체활동(d=0.3)그룹과의 평균 인지기능개선 효과차이(difference)를 보이며 CRCI 환자의 인지기능개선에 가장 효율적인 운동유형임을 확인하였다.
2) 운동강도에 따른 CRCI 환자의 인지기능개선
본 연구에서 메타분석한 논문들의 운동중재 프로그램의 참여시간과 운동강도는 American Cancer Society (ACS)에서 제공된 암환자를 위한 운동가이드라인을 기반으로 진행되었고, 암환자를 위한 운동 참여시간 및 운동강도는 주당 최소 150분의 중강도 또는 중·고강도 운동으로 설계되어 있었다. 운동강도에 따른 CRCI 환자의 인지기능개선 효과를 분석했을 때, 각 연구에서 실시한 중강도 운동과 중·고강도 운동 모두 인지기능 개선에 긍정적인 영향을 미치며 통계적으로 유의미한 효과를 보였다. 특히, CRCI 환자 인지기능개선 측면에서 두 운동강도 사이의 효과성은 큰 차이를 보였다. 중강도 운동은 중간 수준(ES=0.60, p=.000) 이상의 인지기능 개선효과를 보였고, 중·고강도 운동(ES=0.27, p=.007)은 낮은 수준의 인지기능 개선효과를 보여 둘 사이의 효과성은 0.3 이상의 차이를 나타냈다. 즉, 개별 운동중재연구에서 설계된 두 가지 수준의 운동강도 모두 인지기능개선에 긍정적인 영향력을 보였지만, 중강도 수준의 운동이 중·고강도 운동에 비해 CRCI 환자의 인지기능 개선에 보다 효율적일 수 있음을 확인하였다.
3) 운동기간에 따른 CRCI 환자의 인지기능개선
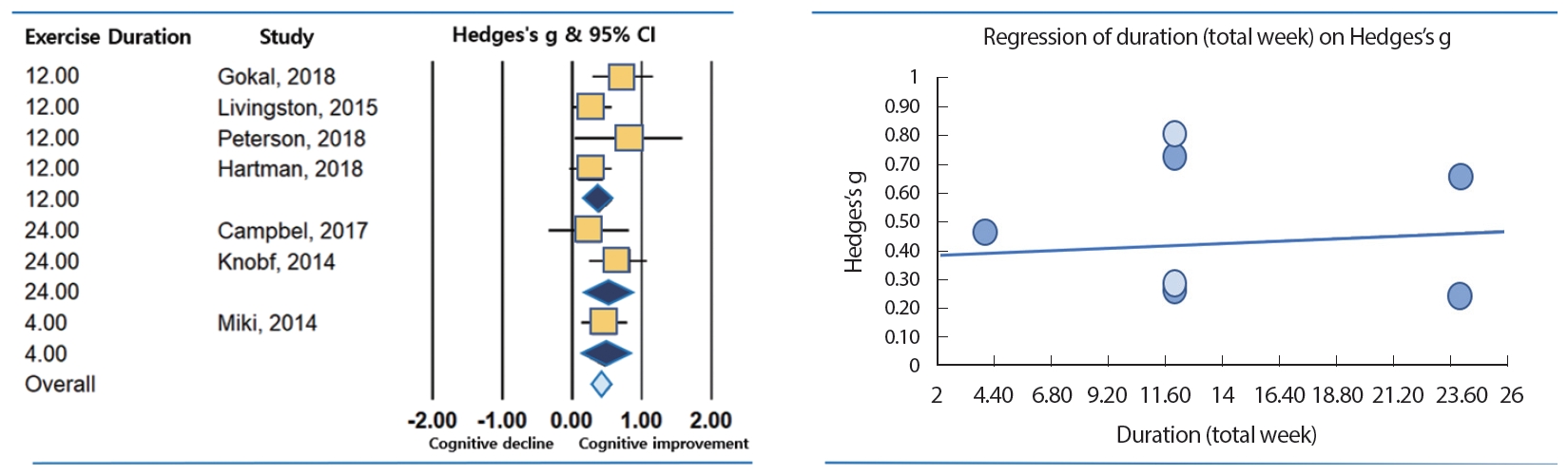
수집된 각 연구의 운동기간은 4주에서 24주로 구성(Table 3)되어 있었다. 운동기간에서 CRCI 환자의 인지기능개선은 중간수준에 미치는 효과성을 보였는데, 운동기간에 따른 메타회귀분석(meta-regression)을 살펴보면 운동기간이 증가할수록 전체평균 CRCI 환자의 인지기능이 개선(slope: 0.00366)되고 있음을 알 수 있다(Table 4, Fig. 5). 메타 ANOVA를 통해 운동기간에 대한 주(week)별 비교(Table 3)를 실시했을 때, 운동기간 24주(ES=0.50, p=.014)동안 운동한 그룹의 경우, 효과 크기가 가장 크게 나타나 CRCI 환자의 인지기능개선에 가장 효율적인 운동기간으로 나타났다. 그다음으로 효과가 높았던 운동기간은 4주(ES=0.46, p=.038)동안 운동중재를 실시한 그룹이었고, 그 뒤로 12주(ES=0.42, p=.001) 운동중재 그룹 순이었다. 이처럼 4주, 12주 및 24주로 설계된 운동중재프로그램에서 기간의 따른 효과성의 차이는 다소 존재했지만 운동을 통한 CRCI 환자의 인지기능개선 효과는 기간과 상관없이 긍정적으로 나타남을 알 수 있다. 특히, 운동기간이 증가할수록 인지기능개선효과는 유지되거나 향상됨을 확인하였다.
4. 암환자 유형에 따른 운동이 CRCI 환자의 인지기능개선에 미치는 효과
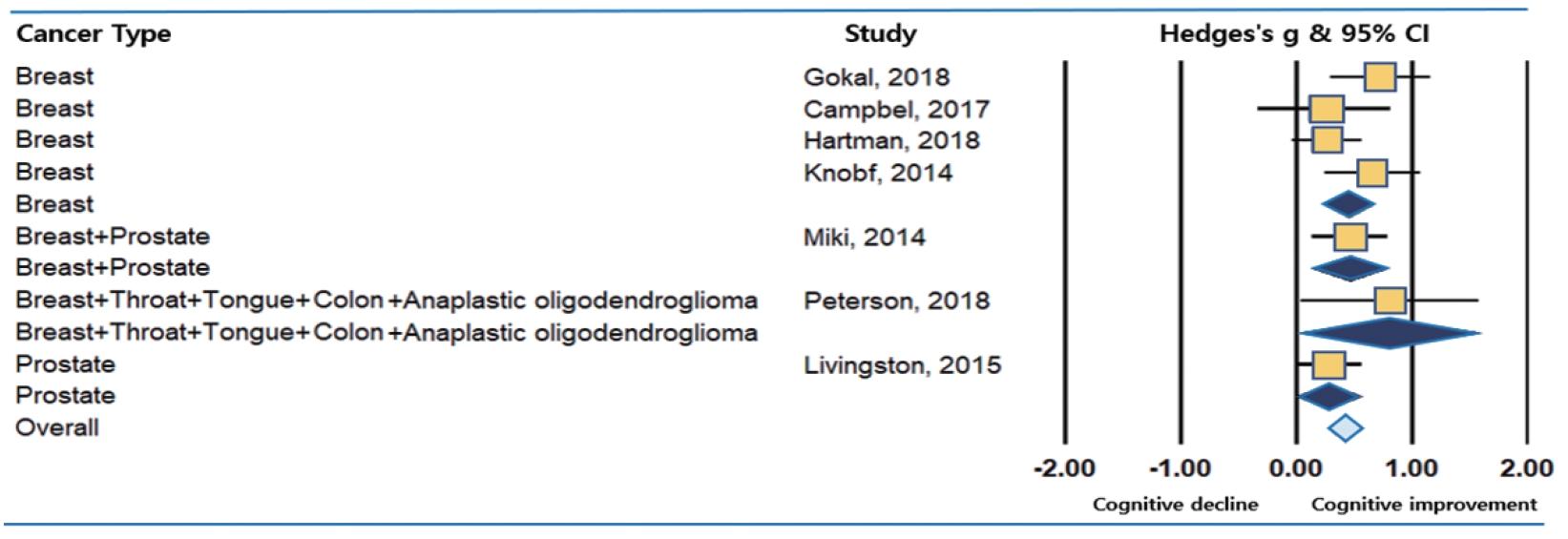
본 메타분석에 사용된 개별 연구의 암유형은 ⑴ 유방암 연구, ⑵ 전립선암 연구, ⑶ 유방암 및 전립선암 통합연구, 그리고 ⑷ 유방암, 인후암, 설암, 대장암 및 악성뇌교종 통합연구로 구성되어 있으며 실험에 참여한 전체 CRCI 환자는 총 195명이었다. 통계적으로 유의미하지 않았지만 암유형에 따른 운동중재효과는 유방암, 인후암, 설암, 대장암 및 악성뇌교종 통합연구(ES=0.80, p=.187)에서 가장 컸다(Table 5, Fig. 6). 운동이 CRCI 인지기능개선에 가장 큰 효과를 보여준 암환자 유형은 유방암이었다. 운동중재가 유방암관련 CRCI 환자의 인지기능개선에 미치는 효과크기는 중간수준(ES=0.47, p=.000)으로 운동을 통한 인지기능개선을 보여주었다. 이와 반대로 전립선암 환자는 유방암 환자에 비해 현격히 낮은 효과크기(ES=0.28, p=.187)를 보였는데 통계적으로 유의미하지는 않았다. 그러나 유방암 환자와 전립선암 환자 대상의 통합연구에서는 중간수준(ES=0.46, p=.040)의 인지기능 개선효과를 보이며 유방암 환자가 포함된 운동중재연구가 CRCI 인지기능개선에 효과가 있음을 보여주었다. 따라서 운동을 통한 인지기능 변화가 유방암 환자에게 쉽게 관찰될 수 있으며, 다른 암 유형에 비해 CRCI 유방암 환자의 인지기능개선에 미치는 운동의 긍정적인 영향력이 크다는 것을 알 수 있다.
5. 운동지도자(supervisor) 유무에 따른 CRCI 환자의 인지기능개선효과
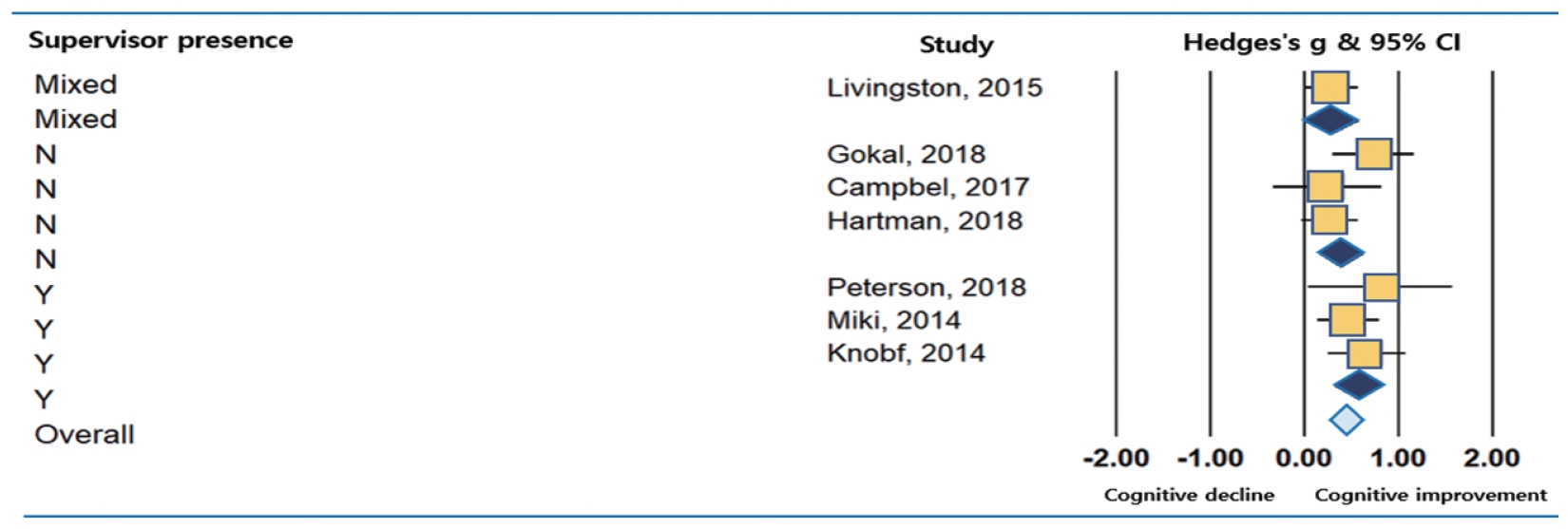
운동 시 운동지도자의 유무에 따른 CRCI 환자의 인지기능개선에 대한 효과성을 알아보았다. 각 연구에서 운동지도자의 유무는 운동중재 프로그램에 따라 ⑴ 동반(Yes)형, ⑵ 비동반(No)형 및 ⑶ 동반과 비동반 혼합(Mixed)형으로 구성되어 있었다. 운동지도자와 동반하여 운동하는 경우, 지도자의 동반없이 운동을 하는 경우 및 혼합하여 운동중재를 실시한 경우 모두 CRCI 환자의 인지기능개선에 긍정적인 효과성을 나타냈다(Table 6). 그러나 운동지도자 유무에 따른 결과 사이의 효과크기는 차이가 있었다. 운동지도자와 동반한 운동중재프로그램에 경우, 인지기능개선에 중간이상(ES=0.57, p=.000)의 효과크기를 보였고, 동반하지 않은 경우는 중간수준(ES=0.39, p=.001)에 준하는 효과성을 나타내며 약 0.2의 효과크기 차이를 확인했다(Fig. 7). 지도자의 동반과 비동반이 혼합된 중재프로그램의 경우는 효과크기가 통계적으로는 유의미하지 않았지만 낮은 수준(ES=0.29, p=.076)의 효과성을 보였다. 이 분석 결과를 통해 운동지도자의 동반 유무와 상관없이 운동이 CRCI 환자의 인지적 개선효과를 보인다는 것을 알 수 있다. 운동지도자가 동반할 경우 CRCI 환자의 인지기능 개선에 미치는 운동효과는 증가하지만, 운동지도자 없이 혼자서 운동을 진행하더라도 인지기능개선 효과를 얻을 수 있음을 확인했다.
논 의
본 연구는 항암치료 중, 유방암 환자에게 높은 확률로 발생되고 있는 인지기능저하(CRCI)에 미치는 운동의 영향력을 메타분석을 통해 검증하였다. 암유형에 따른 운동효과를 검증하기 위해 운동유형, 운동강도, 운동기간 및 운동 중 관리감독의 유무를 기반으로 인지기능개선의 연관성을 정밀하게 분석하며 CRCI 유방암 환자에게 가장 적절한 운동프로그램의 구성요소를 확인했다. 7개 연구의 운동중재 유형을 분류했을 때 유형은 크게 걷기, 고정식 실내자전거, 그리고 자유운동으로 구성되어 있었고, 운동 기간은 4주, 12주, 그리고 24주로 각각 설계되어 있었다. 수집된 연구의 운동강도는 중강도와 중·고강도로 진행되었는데 중강도 운동의 기준은 개별 예비심박수(Heart Rate Ratio, HRR) 55%-65% 수준, 중·고강도 운동의 경우는 HRR 75% 수준을 넘지 않았고, 운동지도자의 동반, 비동반, 또는 동반과 비동반을 혼합한 운동중재로 구성되었다. 메타분석 결과, 전체운동중재프로그램이 암 유형에 관계없이 CRCI 환자의 인지기능개선에 미치는 평균효과크기는 중간수준(ES=0.43)에 준하는 효과를 보이며 운동이 CRCI 환자에게 효과가 있음을 나타냈다. 운동중재프로그램이 암유형에 관계없이 CRCI 환자의 인지기능저하를 완화하는 효과적인 비약물적 중재치료임을 의미하는데, 이는 운동과 인지기능개선에 관한 긍정적인 연구 결과[33-35]를 뒷받침하는 내용으로 CRCI 환자에게도 운동이 인지기능개선에 효과적임을 알 수 있다.
CRCI 환자에게 가장 효과적인 운동중재유형으로는 걷기운동(ES=0.59)이었다. 걷기운동이 인지기능개선에 가장 효과적인 운동유형으로 나타나 경도인지장애(mild cognitive impairment, MCI)노인의 인지기능개선에 걷기운동(ES=0.54)이 효과적이었던 메타분석 보고와 유사한 결과를 보였다[36]. 걷기운동의 특성상 타 운동에 비해 힘은 덜 들지만 신체의 큰 에너지를 사용하기 때문에 항암치료로 인해 저하된 체력 및 신체기능을 가진 암환자에게 노인과 마찬가지로 인지기능개선에 효과적[26,37,38]이며, 큰 에너지를 사용할 때 활성화되는 해마의 신경세포생성과정을 촉진[14]하면서 걷기운동이 CRCI 환자의 인지기능 개선에 효과적인 운동중재로 관찰되는 이유를 설명할 수 있다. 특히, 고령자의 경우, 중등도 강도의 육상 걷기를 통해 동맥내피기능(혈관의 반경 증가 등)이 강화되고 이는 혈류량, 혈류속도 및 선행성 혈류 흐름을 증가시킨다[39]. 본 메타분석에서 관찰된 대상자의 연령분포가 51-76세로 고령임을 감안했을 때, 이러한 중강도 걷기운동을 통한 혈류역학적 효과가 CRCI 환자들의 동맥내피기능 강화에 영향을 미쳤을 것으로 사료된다. 따라서 강화된 동맥내피기능은 뇌유래신경영양인자(Brain-derived neurotrophic factor, BDNF)의 증가 촉진[14-16, 40,41], 심폐운동을 통한 인지기능 관련 뇌영역의 용적증가 및 신경세포생성 [42,43]와 관련되어 인지기능개선에 긍정적인 영향을 미쳤을 것으로 예상할 수 있다. 또한, 중등도 수준의 운동강도를 통해 스토리회상(story memory recall)을 방해하는 백질병변(white matter lesion)의 용적(volume)감소[44]는 중강도 운동이 CRCI 환자 인지기능개선에 효과적(ES= 0.60)이라는 본 연구결과(Table 3)를 뒷받침한다.
본 메타분석에서 수집된 연구들의 CRCI 환자의 수는 총 195명이었고, 표본통합으로 인해 연구 검정력이 증가되고 정확성이 제고되면서 개별 연구의 한계점으로 지적된 표본사이즈에 대한 한계[26]를 완화할 수 있었다. 수집된 연구에서 진단받은 암 유형은 총 6가지로 분류되었는데 유형은 유방암, 전립선암, 인후암, 설암, 대장암 및 악성 뇌교종이었다. 메타 분석된 암유형은 첫째, 한 가지의 암유형(유방암 또는 전립선암)대상자 중재연구, 둘째 두 가지의 암유형(유방암+전립선암) 대상자 중재연구, 그리고 마지막으로 세 가지 이상의 암유형(유방암+인후암+설암+대장암+악성뇌교종) 대상자 중재 연구였다. 본 연구 결과에서 흥미로운 점은 CRCI 유방암 환자의 인지기능개선 효과였다. 수집된 실험연구에서 유방암이 포함된 연구의 효과크기는 중간수준 이상으로 관찰되었고, 개별연구에 활용된 운동중재 프로그램이 유방암 환자에게 특히 효과적임을 확인할 수 있었다. 또한, 전립선암 환자 대상 운동중재[45]에서 인지기능개선의 효과크기는 0.34로 나타났는데 본 메타분석에서 분석된 낮은 효과크기 0.28과 유사한 효과성을 보였다(Table 4). 그러나 또 다른 유방암 환자와 전립선암 통합연구(Table 4)에서 그 효과크기가 중간수준이상(ES=0.46)으로 상향된 것을 보았을 때, 유방암 환자의 높은 효과성이 해당 연구 전체에 영향을 미쳐 높은 효과크기를 나타냈을 것으로 예상할 수 있다. 즉, CRCI 유방암 환자의 인지기능개선에 운동참여의 효율성을 다시 한번 증명함으로써 관련 연구결과[44,46-49]를 지지하는 결론을 도출했다.
CRCI 환자의 운동중재 중, 운동지도자(supervisor)의 유무에 따른 효과크기는 동반(ES=0.57)에 비해 비동반(ES=0.39)인 경우 상대적으로 작은 효과성을 보였지만 운동지도자가 없는 경우일지라도 중간수준에 준하는 CRCI 인지기능개선의 효과성을 내포하고 있음을 시사한다. 이 시사점은 암 환자의 경제적 측면에서 운동참여 장벽을 낮추는 요인으로 활용될 수 있는데, 개인 트레이너(personal trainer) 등 운동지도자를 고용하여 운동을 진행하는 암환자의 경우, 트레이너 없이 운동하는 암환자에 비해 인지기능개선 효과가 더 좋을 수 있다. 그러나 혼자 운동하는 환자의 경우도 이에 준하는 상당한 운동효과를 볼 수 있다는 점에서 운동지도자의 고용은 경제적 측면에 따른 필수가 아닌 선택사항으로 고려될 수 있다. 따라서 인지기능개선 측면에서 CRCI 환자가 정확한 운동가이드라인을 통해 바르게 운동에 참여한다면 혼자서도 충분한 인지기능개선 효과를 얻을 수 있다는 것을 본 분석결과는 내포한다.
메타 분석된 운동중재 기간은 수집된 연구를 기반으로 4주, 12주 및 24주로 분석하였다. CRCI 환자의 인지기능개선효과는 각 기간 내에서 큰 차이를 보이진 않았지만, 운동기간이 길어질수록 인지기능개선효과가 우상향으로 향상(Table 6)되며 운동지속기간에 따라 CRCI 환자의 인지기능개선이 비례하여 향상되는 것을 확인했다. 운동중재프로그램의 지속시간이 길어질수록 인지기능개선에 유익한 효과를 보여주는 메타 분석[50]과 유사한 결과로 운동지속기간과 누적된 시간은 우리 연구에서도 CRCI 환자들의 인지기능개선 효과를 보여주었다(Fig. 7). 특히 이 중 단기간 운동중재에서도 상당한 인지기능개선효과를 확인할 수 있었다. 4주 운동중재 프로그램에 참여한 CRCI 환자의 경우 중간수준(ES=0.46)의 인지기능 개선 효과를 나타냈으며, 24주 운동의 효과크기(ES=0.50)와 유사한 효과성을 보였다. 즉, 단기적인 운동참여가 인지기능개선에 긍정적인 영향을 미칠 수 있음을 보고한 타 연구[46,51]와 유사하게 본 연구에서도 짧은 운동기간이 CRCI 환자의 인지기능개선에 효과가 있었다. 동물실험에서는 기억력 등 인지기능과 연관된 뇌영역인 해마(hippocampus)의 신경세포생성 기간은 약 3주로 보고[52,53]되고 있어 4주 동안의 짧은 운동기간에도 CRCI 환자의 인지기능변화에 미치는 운동효과는 빠르게 나타날 수 있음을 판단할 수 있다. 짧은 기간 동안 발생한 운동효과는 운동을 주저하는 암환자의 심리적 장벽을 낮출 수 있으며, 단기적 운동중재프로그램에 대한 참여를 독려함으로써 추후 지속적이고 자발적인 운동참여의 동기를 부여할 수 있을 것으로 예상된다. 이러한 동기부여를 통한 장기적인 운동 참여는 CRCI 유방암 환자의 인지기능 개선효과를 지속적으로 유지시킬 뿐만 아니라 향상시키는데 기여할 것으로 사료된다.
결 론
본 연구는 CRCI 유방암 환자의 인지기능 개선을 위한 운동중재에서 운동의 유형, 강도, 기간 및 지도자의 동반 유무에 따른 인지기능의 개선에 대한 효과크기를 검증하였다. CRCI 유방암 환자의 인지기능개선에 중등도 수준의 운동강도와 걷기 기반운동이 효과적이었으며 운동지도자 없이 혼자 운동을 하더라도 인지기능개선측면에서 긍정적인 운동효과가 나타났다. 운동을 통한 암 관련 인지 기능 손상에 대한 보상 효과는 4주 동안의 단기간에서 관찰되었으나 4주 이상의 지속적인 운동을 통해 인지기능 개선효과가 유지될 수 있을 것으로 판단된다. 따라서 유방암 관련 인지 손상 환자에게 성취 가능한 단-장기 운동기간의 설정을 포함한 개인별 맞춤 운동처방 프로그램을 제공한다면 인지기능 손상을 완화시키고 인지능력을 향상시킬 수 있을 것이다.
Notes
The authors have no conflicts of interest relevant to this study.
AUTHOR CONTRIBUTION
Conceptualization: HB Eun, SS Baek; Data curation: HB Eun, SS Baek; Formal analysis: HB Eun; Funding acquisition: SS Baek; Methodology: HB Eun; Project administration: HB Eun; Writingoriginal draft: HB Eun, SS Baek; Writing-review & editing: SS Baek.