저항성운동이 난소절제 모델의 PVAT에서 NADPH Oxidase와 Adiponectin에 미치는 영향
Abstracts
PURPOSE
Perivascular adipose tissue (PVAT) is a type of adipose tissue that surrounds vessels to provide anti-contractile effects. This study aimed to investigate the effect of resistance training on NADPH oxidase, adiponectin, and endothelial NOS (eNOS) expression in the abdominal aorta and PVAT of ovariectomized rats.
METHODS
Sprague-Dawley rats at 20 weeks of age were divided into three groups: sham control (Sham, n=10), OVX-control (OVX_Con, n=10), and OVX-resistance exercise (OVX_Rex, n=10). Resistance training was performed by climbing a ladder for 12 weeks. Western blotting was used to analyze target protein expression in the rat abdominal aorta and PVAT.
RESULTS
NADPH oxidase (p67phox) expression was significantly higher in the OVX_Con group than in the sham group, but it was significantly decreased in the OVX_Rex group. The expression of adiponectin, AKT, and eNOS in both abdominal aorta and PVAT was significantly reduced in the OVX_Con group than in the Sham group, but it was improved in the OVX_Rex group.
CONCLUSIONS
The results suggest that regular resistance training inhibits p67phox and increases adiponectin expression and phosphorylation of AKT and eNOS in abdominal aortic PVAT of ovariectomized rats.
Keywords: PVAT, Aorta, Resistance training, Adiponectin, NADPH oxidase
색인어: PVAT, 대동맥, 저항성훈련, 에디포넥틴, NADPH oxidase
서 론
산화 스트레스는 심혈관질환의 시발점에서 중요한 역할을 한다[ 1]. 에스트로겐 결핍은 혈관 활성산소종(Reactive oxygen species, ROS)의 증가와 endothelial nitric oxide synthase (eNOS) 발현 감소를 통해 산화질소(nitric oxide, NO) 생성을 감소시켜 혈관 내피세포 기능의 저하를 유발하는 것으로 잘 알려져 있다[ 2, 3]. 혈관내피세포가 혈관의 장력 조 절에 중요한 역할을 수행하는 것으로 지금껏 알려져 왔으나, 최근 심혈관질환의 합병증을 개선할 수 있는 혈관이완인자인 산화질소의 생성과 항산화 치료에 perivascular adipose tissue (PVAT)가 관련되어 있다고 보고되었다[ 4]. PVAT는 PVRFs (PVAT-derived relaxing factors)과 PVCFs (PVAT-de-rived contracting factors)를 분비해서 내피세포 의존적(endothelium-de-pendent) 혹은 비의존적인(endothelium-independent) 기전을 통해 혈관 장력을 조절한다[ 5– 7]. 특히 Adiponectin는 PVAT에서 분비되는 강력한 혈관 이완인자로써 eNOS 활성을 통해 혈관의 항수축(anti-contractile) 기능을 수행한다[ 8]. 반면에 PVAT에서 NADPH oxidases을 통한 활성산소(Superoxide) 생성에 의해 혈관 수축 반응이 증가된다[ 9]. Fernández-Alfonso et al. [ 10]은 비만에 의한 산화 스트레스 증가가 PVAT 유래-혈관 활성인자들의 불균형을 초래하여 혈관기능저하를 유발한다고 보고하고 있고, 고혈압모델에서도[ 11] ROS가 PVAT 기능을 억제시켜 내피세포 기능저하를 유도하는 것으로 알려져 있다[ 12]. 뿐만 아니라 난소절제 모델(Ovariectomized rat, OVX)의 혈관조직에서 NADPH oxidase Subunit인 p22phox 발현의 증가에 의한 활성산소의 생성으로 혈관 내피세포 기능저하가 유도된다고 보고되었다[ 13, 14]. 그러나 이러한 NADPH oxidase에 의한 내피세포 기능의 저하는 항수축 물질인 adiponectin에 의해 감쇄될 수 있는 바, Antonopoulos et al. [ 15]은 2형 당뇨 인체 동맥의 체외 실험(human arteries ex vivo)에서 재조합 adiponectin이 Rac1의 세포막 이동의 억제와 p22phox발현을 감소시켜 PI3K/AKT/eNOS를 활성화시킨다고 보고하고 있다. 또한 adi-ponectin는 고지혈증 환자에서 p47phox의 세포막 이동을 억제하여 활성산소 생성을 줄여 eNOS를 활성화시킨다[ 16]. 반면에 adiponectin이 제거(knockout)된 고혈압쥐의 심근에서 p22phox 발현의 증가[ 17]와 PVAT-유래 adiponectin 감소가 혈관의 항수축 능력을 감소시키는 것으로 보고 되었다[ 18, 19]. 최근 운동이 비만 쥐에서 adiponectin 발현을 증가시켜 PVAT 기능을 개선할 수 있다는 것이 보고되었고[ 20], 또한 전통적으로 유산소 운동[ 21– 23]과 저항성운동[ 24]이 에스트로겐 결핍 동물과 폐경모델의 혈관조직에서 산화질소 생성의 증가에 의한 혈관기능의 개선을 보고하고 있다. 그러나 이러한 연구들은 PVAT가 제거된 혈관조직에서만 연구가 이루어졌기 때문에, PVAT 조직에서 NADPH oxidase, adiponectin 및 eNOS 단백 운동관련 기전은 불분명하다. 특히 저항성운동은 폐경여성의 근력증가, 지방합성의 억제 및 골다공증 예방효과가 있는 것으로 잘 알려져 있으나 에스트로겐 결핍 모델을 이용한 PVAT관련 저항성운동연구는 아직 보고되어 있지 않다. 이에 본 연구는 난소절제모델을 이용하여 저항성 운동이 PVAT 기능과 관련되어 있는 NADPH oxidase/ adiponectin/eNOS 단백 발현에 미치는 효과를 규명하고자 한다.
연구 방법
1. 실험동물
본 실험에 사용한 동물은 다물 사이언스(Daejeon, Korea)에서 공급받은 Sprague-Dawley (SD) 계열 20주령 암컷 흰쥐 30마리를 대상으로 하였다. 실험동물은 사육케이지(42×28 cm)를 이용해 실험실 온도 22-24°C, 습도 60±5%가 유지되며, 밤낮주기(12시간 light/12시간 dark)가 자동 조절되는 사육실에서 1주간 예비 사육 후 난소 절제 시술을 시행하여 통제집단(Sham, Sham-operated control, n=10), 난소절제 통제집단(OVX_Con, Ovariectomized control, n=10), 난소절제 저항성운동집단(OVX_Rex, Ovariectomized Resistance exercise, n=10)으로 나누어 12주간 실험을 실시하였다. 식이는 고형사료(지방 3.5%, 단백질 22.5%, 저섬유 7.5%, 회분 9.0%, 인 0.5%, 칼슘 0.7%)와 물을 자율적으로 섭취하도록 하였으며, 동물실험 윤리위원회의 승인을 받아 실험을 수행하였다(HNU 2018-1). 실험동물의 특성은 Table 1과 같다.
Table 1.
Characteristics of experimental animals
|
Group |
Number |
Age (wk) |
Weight (g) |
|
Sham |
10 |
20 |
301.51±2.59 |
|
OVX_Con |
10 |
20 |
301.72±2.62 |
|
OVX_Rex |
10 |
20 |
301.53±2.26 |
2. 난소절제술
난소절제술은 Idris [ 25]의 선행연구를 토대로 실시하였다. Ketamine (Korea 100 mg/kg)과 2% Xylazine (Rumpun 0.15 mL/kg)으로 전신 마취하고 제모 및 시술 전 무균 처리(10% povidone-iodine scrub followed by 70% alcohol wipe)를 시행하였다. 실험동물의 배 측 중앙에 1 cm 가량의 절개를 시행한 후 봉합용 실로 난소를 결찰하고 난소절제를 양측으로 시행하였으며 난소절제 후 각 장기를 복강 내로 재위치 시킨 후 봉합용 실로 층별 봉합을 하고 감염 방지를 위해 항생제(cafazolin 50 mg/kg)를 근육에 주사하였다. 시술 후 2주일 동안 회복 과정을 거친 후 실험을 실시하였다.
3. 저항성운동
저항성운동은 An et al. [ 26]의 선행연구를 참고하여 사다리 등반(ladder climbing) 운동을 1일 8회 주 3회로 12주간 실시하였다. 실험의 1주일 동안은 사다리운동 적응기간으로 실험동물은 무부하 상태에서 사다리 오르기를 수행하였으며, 경사면 상부에 사료를 두어 자발적 운동을 유도하였다. 적응기간 종료 후 쥐의 운동량을 동일하게 유지하기 위해 각각의 최대부하강도(repetition maximum, 1RM)를 측정하고 무게부하에 반영하였다. 사다리 오르기에서 1RM은 쥐의 꼬리에 추를 달고 1회에 올라갈 수 있는 최대의 중량이다. 이를 효과적으로 결정하기 위해서 체중의 50% 무게인 추를 꼬리에 달고, 길이 135 cm, 간격 1.5 cm, 경사도 80°의 사다리를 올라가게 하였다. 쥐가 이를 완료하면 그 추의 무게에 25%의 중량을 더하여 다시 올라가게 하였다. 이러한 절차를 반복하여 각 쥐들의 1RM을 평가하였다. 본격적인 저항성운동 방법은 각 개체별로 사전에 결정된 1RM의 50%에 해당되는 무게의 추를 이용하여 꼬리에 달고 사다리를 올라가게 하였다. 만약 이 추를 꼬리에 달고 완전히 올라가면, 2분의 휴식을 제공한 후에 이전에 완료한 무게에 25%의 무게를 증가시켜, 다시 사다리를 올라가게 하였다. 만약 쥐가 1RM 이상의 추를 달고 사다리를 올라가면, 1RM에 20 g의 무게를 추가하여 실시하였다( Table 2).
Table 2.
Resistance training protocols
|
Week |
loading weight (% 1RM) |
|
1 |
50% 1RM |
|
2 |
75% 1RM |
|
3 |
90% 1RM |
|
4 |
100% 1RM |
|
5 |
100% 1RM+20 g |
|
6 |
100% 1RM+40 g |
|
7 |
100% 1RM+60 g |
|
8 |
100% 1RM+80 g |
|
9 |
100% 1RM+100 g |
|
10 |
100% 1RM+120 g |
|
11 |
100% 1RM+140 g |
|
12 |
100% 1RM+160 g |
4. Western blot
혈관과 PVAT의 단백질 발현을 확인하기 위하여 복부 대동맥(Ab-dominal aorta)과 PVAT (Abdominal aortic PVAT)을 적출하여 액체질소에 급랭시키고, −80°에 보관하였다. 적출된 대동맥과 PVAT는 lysis buffer (Sigma, USA)에서 균질화되고, 균질화된 조직은 4°C에서 13,000 rpm으로, 10분간 원심 분리하여 상층액을 분리하고 BCA assay Kit (Bio-rad, USA)를 사용하여 단백질을 정량하였다. 40 μ g의 단백질을 8% SDS-PAGE에서 전기영동한 후 PVDF membrane으로 전이시켰다. Membrane의 비특이적인 반응은 5% nonfat dry milk가 첨가된 TBS-T 용액으로 상온에서 1시간 동안 반응시켜 제거하였다. Adiponectin, p47phox, p67phox, AKT, p-AKT, eNOS, p-eNOS (1:1,000, Cell signaling, USA)와 GAPDH (1:1,000, Sigma, USA)의 일차 항체를 5% skim milk가 첨가된 TBS-T 용액에 희석하여 4°C에서 15시간 동안 반응시켰고, 이차 항체는 horseradish peroxidase conjugated secondary antibodies를 이용하여 실온에서 2시간 반응시켰다. 반응의 확인은 ECL detection system (Thermo, USA)을 이용하여 분석하였다.
3. 자료처리방법
본 실험의 연구결과는 SPSS 통계 프로그램을 이용하여 기술 통계량을 산출하고, 각 단백질 발현량의 변화에 대한 검증은 일원 변량분석(one-way ANOVA)을 이용하였으며, 사후검증은 LSD을 이용하였다. 통계적 유의수준은 .05로 설정하였다.
연구 결과
1. 저항성 운동이 p47 phox 과 p67 phox 단백 발현에 미치는 영향
p47phox와 p67phox 단백발현이 저항성운동에 의해 변화되는지 OVX 모델의 Abdominal Aorta와 PVAT (Perivascular adipose tissue)에서 확인 하였다( Fig. 1). p67phox 단백 발현은 Sham에 비해 OVX_Con에서 대동맥과 PVAT ( Fig. 1B)에서 각각 유의하게 증가되었으나( p <.05, Sham vs. OVX_Con), 저항성운동에 의해 대동맥과 PVAT에서 유의하게 감소되었다( p<.05, OVX_Con vs. OVX_Rex). p47phox 발현은 p67phox와 유사한 경향을 보였으나 그룹 간 유의한 차이가 나타났지 않았다.
Fig. 1.
Fig. 1.Resistance exercise inhibited p47 phox and p67 phox expression in abdominal aorta and perivascular adipose tissue (PVAT) of OVX rats. (A) Results of Western blot and (B) Densitometry analysis for expression of p47 phox and p67 phox. Sham, Sham-control; OVX_Con, OVX-control; OVX_Rex, OVX-Resistance exercise. Each data showed mean±SEM. * p<.05 vs. Sham, # p<.05 vs. OVX_Con. 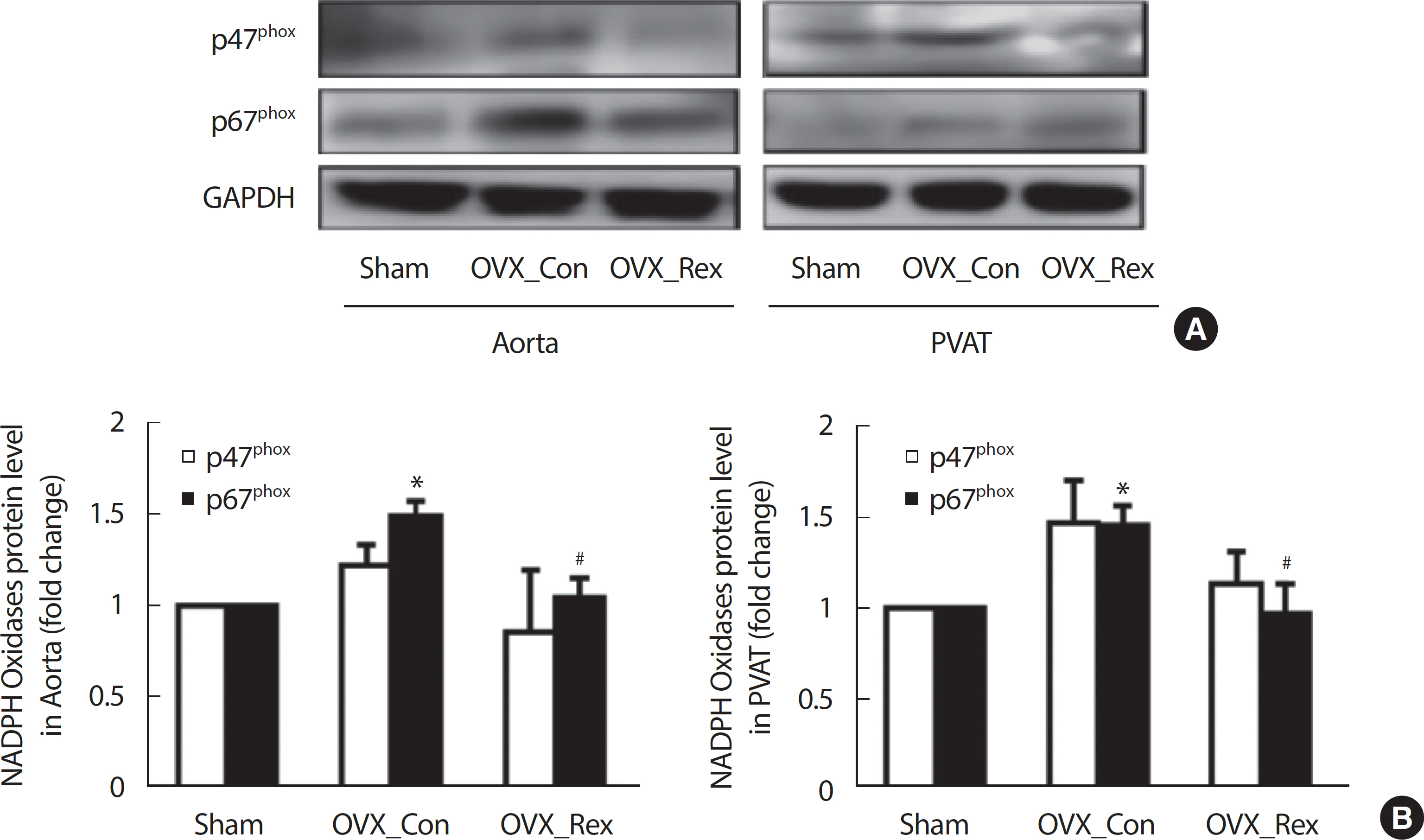
2. 저항성 운동이 Adiponectin 단백 발현에 미치는 영향
저항성운동이 PVAT에서 분비되는 Adiponectin 단백 발현을 OVX 모델의 Abdominal Aorta과 PVAT에서 확인하였다( Fig. 2). Adiponectin 단백발현은 대동맥과 PVAT에서 각각 Sham에 비해 OVX_Con에서 유의하게 감소되었으나( p <.05, Sham vs. OVX_Con), 저항성운동에 의해 대동맥과 PVAT에서 유의하게 증가되었다( p<.05, OVX_Con vs. OVX_ Rex).
Fig. 2.
Fig. 2.Resistance exercise increased Adiponectin expression in abdominal aorta and perivascular adipose tissue (PVAT) of OVX rats. (A) Results of Western blot and (B) Densitometry analysis for expression of adiponectin. Sham, Sham-control; OVX_Con, OVX-control; OVX_Rex, OVX-Resistance exercise. Each data showed mean±SEM. * p<.05 vs. Sham, # p<.05 vs. OVX_Con. 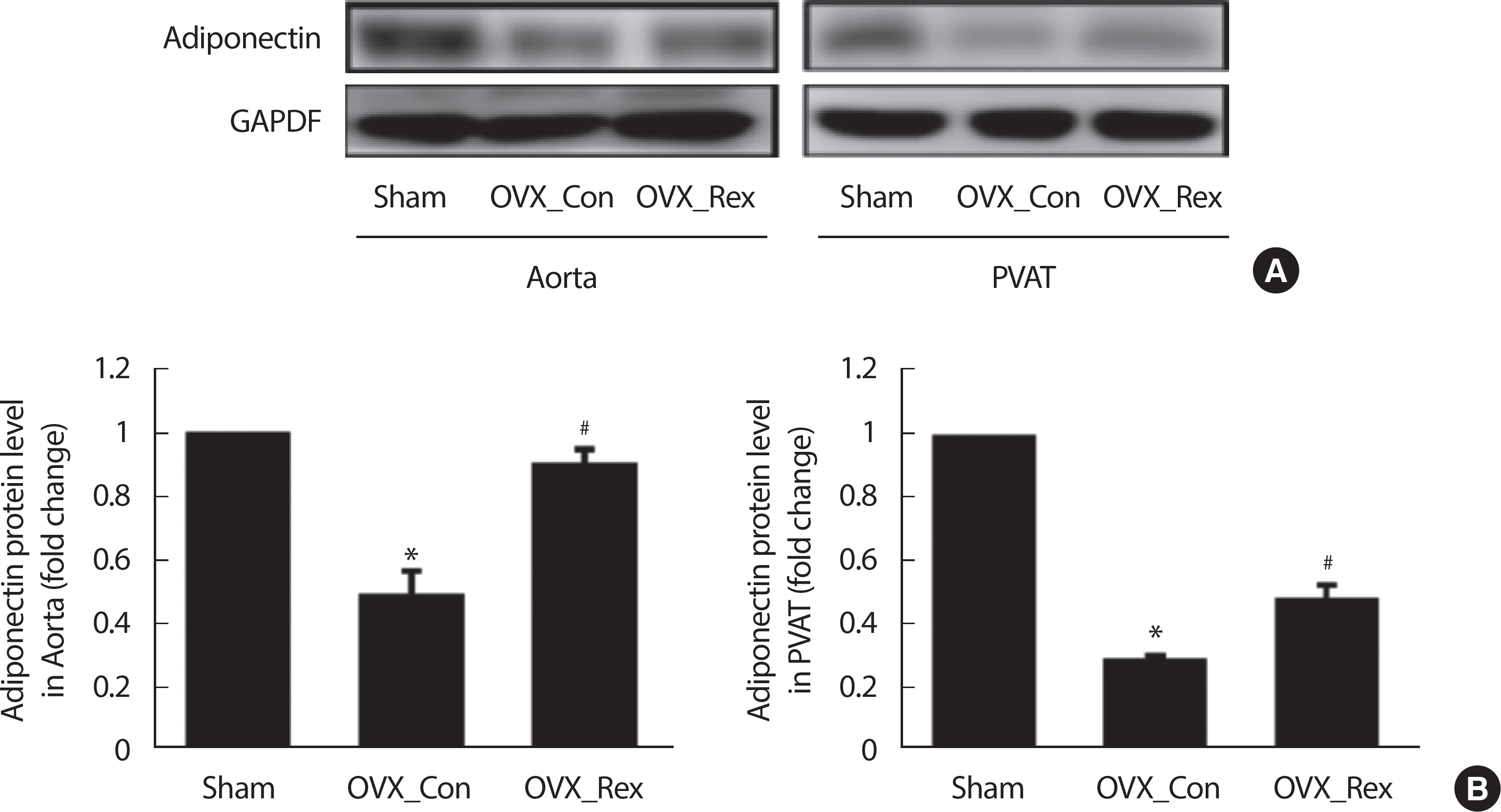
3. 저항성 운동이 AKT 단백 발현에 미치는 영향
저항성운동이 AKT 단백과 인산화 발현의 변화를 OVX 모델의 Ab-dominal Aorta와 PVAT에서 확인하였다( Fig. 3). AKT 인산화(p-AKT) 발현은 대동맥과 PVAT에서 각각 Sham에 비해 OVX_Con에서 유의하게 감소되었으나( p <.05, Sham vs. OVX_Con), 저항성운동에 의해 대동맥과 PVAT에서 유의하게 증가되었다( p <.05, OVX_Con vs. OVX_ Rex). AKT 발현은 대동맥과 PVAT에서 각각 p-AKT와 유사한 경향을 보였으나 지구성운동에 의해 그룹 간 유의한 차이가 나타나지 않았다(OVX_Con vs. OVX_Rex).
Fig. 3.
Fig. 3.Resistance exercise increased p-AKT and AKT expression in abdominal aorta and perivascular adipose tissue (PVAT) of OVX rats. (A) Results of West-ern blot and (B) Densitometry analysis for expression of p-AKT and (C) Densitometry analysis for expression of AKT. Sham, Sham-control; OVX_Con, OVX-control; OVX_Rex, OVX-Resistance exercise. Each data showed mean±SEM. * p<.05 vs. Sham, # p<.05 vs. OVX_Con. 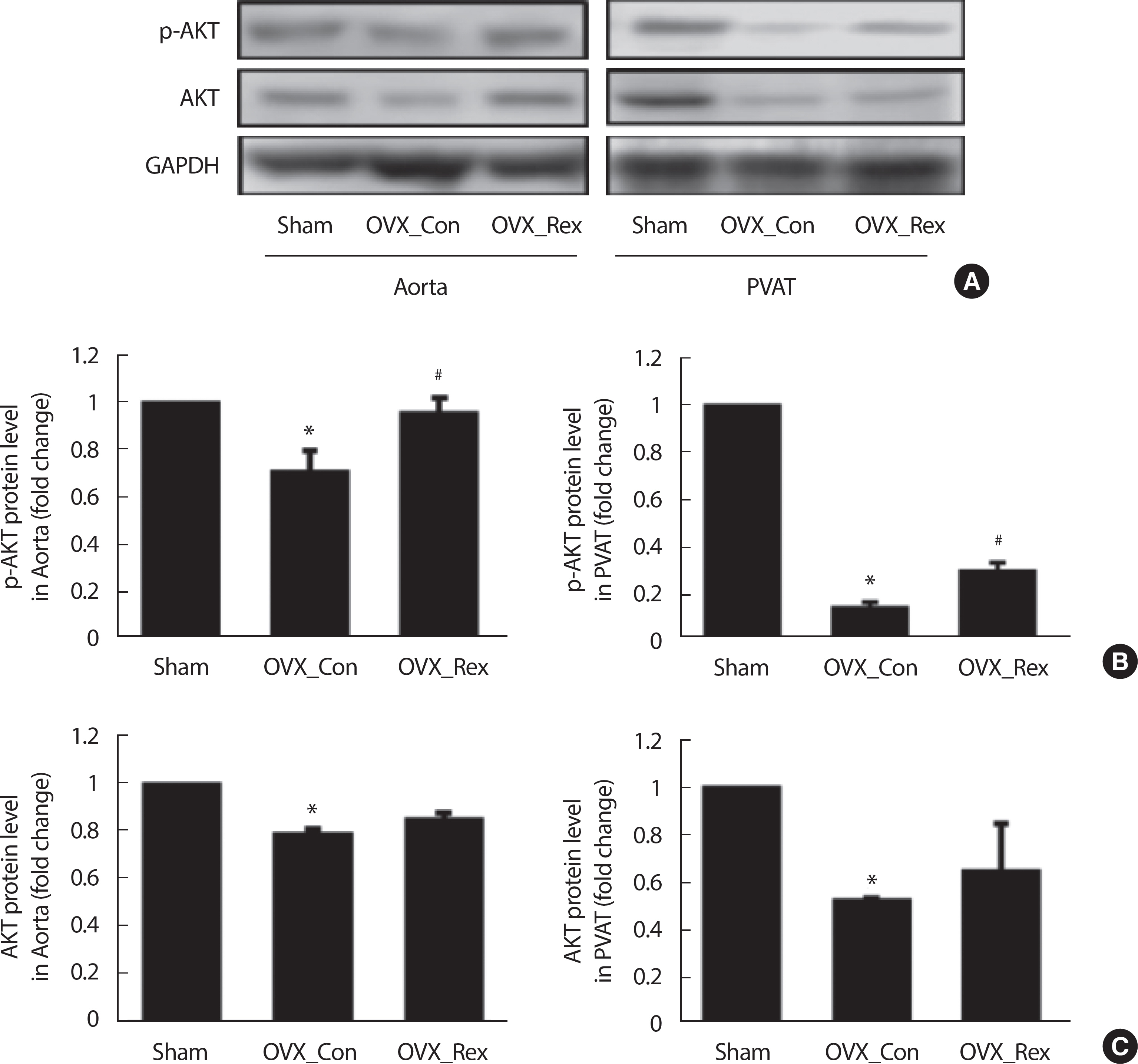
4. 저항성 운동은 eNOS 단백 발현에 미치는 영향
저항성운동이 eNOS 단백과 인산화 발현의 변화를 OVX 모델의 Abdominal Aorta과 PVAT에서 확인하였다( Fig. 4). eNOS와 p-eNOS 발현은 대동맥과 PVAT에서 각각 Sham에 비해 OVX_Con에서 유의하게 감소되었으나( p <.05, Sham vs. OVX_Con), 저항성운동에 의해 대동맥과 PVAT에서 각각 유의하게 증가되었다( p <.05, OVX_Con vs. OVX_ Rex).
Fig. 4.
Fig. 4.Resistance exercise increased p-eNOS and eNOS expression in abdominal aorta and perivascular adipose tissue (PVAT) of OVX rats. (A) Results of Western blot and (B) Densitometry analysis for expression of p-eNOS and (C) Densitometry analysis for expression of eNOS. Sham, Sham-control; OVX_ Con, OVX-control; OVX_Rex, OVX-Resistance exercise. Each data showed mean±SEM. * p<.05 vs. Sham, # p<.05 vs. OVX_Con. 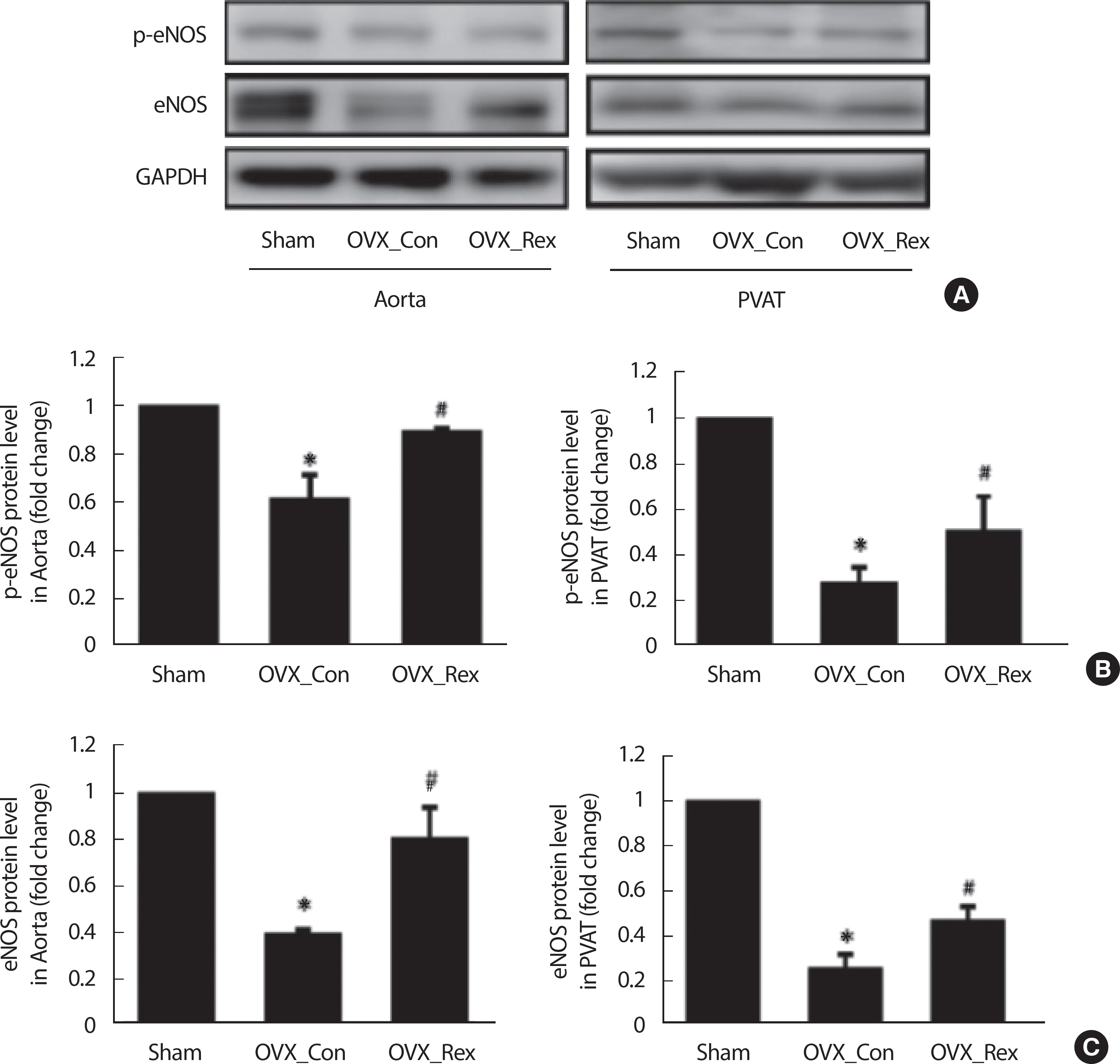
논 의
폐경 후 여성에서 관찰된 에스트로겐 결핍은 혈관 활성산소종(ROS)의 증가와 eNOS 발현 감소를 통해 산화질소의 생성을 감소시켜 혈관 내피세포 기능저하를 유발한다[ 3, 27, 28]. 그러나 유산소 운동은 이러한 내피 기능저하 극복에 중요한 역할을 수행하는 것으로 알려져 있다. 유산소운동이 OVX의 대동맥에서 ROS 생성의 억제 및 eNOS 발현의 증가를 통해 혈관기능을 개선할 수 있다는 것은 일반적으로 잘 알려져 있다[ 2, 29]. Wang et al. [ 2]은 난소절제쥐에서 ROS의 증가로 인해 내피세포의존성 이완반응(Endothelium-dependent relaxation)이 내피세포의존성 수축반응으로 전환되며 이는 PVAT로부터 생성된 ROS 와 관련이 있다고 보고하고 있다. 그러나 폐경여성에게 저항성운동의 효과(근력증가, 지방합성 감소, 골다공증개선 등)가 잘 알려져 있으나 폐경모델에서 혈관조직과 PVAT를 구분해서 NADPH oxidase와 adi-ponectin 및 eNOS에 미치는 저항성운동의 역할에 관한 연구는 매우 제한적이다. 본 연구에서 OVX_Con의 복부대동맥 혈관조직과 PVAT에서 각각 NADPH oxidases의 subunit인 p67phox 단백 발현이 정상 군(Sham)에 비해 증가되었으나 이러한 OVX에 의한 p67phox 단백발현의 증가는 저항성운동에 의해 억제되었다. 이러한 결과는 에스트로겐 부족이 PVAT에서 ROS의 생성을 초래하여 PVAT 기능저하로 인한 혈관 기능저하를 유발하지만 저항성운동에 의해 효과적으로 개선될 가능성이 있다는 것을 의미한다.
산화스트레스에 의한 PVAT-유래 혈관기능 감소는 비만[ 10], 고혈압[ 11], 당뇨[ 15] 등에서 보고되었다. 이는 지방세포에서 분비되는 adipo-nectin과 밀접한 관련이 있다. 흥미로운 것은 PVAT는 혈관을 둘러싸고 있기 때문에 PVAT에서 분비되는 adiponectin이 혈관에 즉시 작용할 가능성이 높다(국소효과). PVAT가 붙어있는 혈관이 제거된 혈관보다 항수축효과가 높게 나타나는 현상은 이를 뒷받침하는 강력한 증거이다[ 2, 6, 9]. 최근 Meziat et al. [ 20]은 운동이 비만 쥐의 PVAT에서 eNOS와 adi-ponectin의 발현을 증가시켜 혈관평활근과 내피세포에서 ROS를 억제하고 eNOS 인산화를 증가시켜 혈관기능을 개선할 수 있다고 보고하 고 있다. 본 연구에서도 저항성 운동이 OVX의 PVAT와 복부대동맥에서 eNOS와 adiponectin의 발현을 유의하게 증가시켰다. 본 연구에서 모든 지방에서 분비되는 혈중 adiponectin 수준을 확인하지 못했지만 PVAT에 의한 혈관의 국소적 역할은 제한적이나마 이해할 수 있다. 저항성 운동도 OVX모델의 PVAT에서 adiponectin의 분비를 촉진하고, 분비된 adiponectin이 혈관으로 유입되어 혈관기능을 개선할 가능성이 있다고 생각된다. Adiponectin은 NADPH oxidase 활성을 억제하고[ 15], AKT-eNOS 축을 활성화시켜[ 8] 혈관기능을 향상시키는 것으로 알려져 있다[ 30]. OVX모델에서 ROS 증가로 인한 eNOS 활성의 감소가 유발되지만[ 31], 유산소 운동은 NADPH oxidase 발현을 감소시켜 AKT-eNOS 활성을 통해 혈관기능을 향상시킨다[ 21– 24]. 본 연구에서도 저항성 운동이 OVX모델의 PVAT와 혈관조직에서 AKT와 eNOS의 인산화를 유의하게 개선시켰다. 이러한 결과는 OVX모델[ 20, 24]의 혈관조직과 2형 당뇨의 PVAT [ 32]에서 지구성운동이 ROS 생성 억제와 eNOS 활성의 증가를 통해 내피세포기능저하를 억제할 수 있다는 연구결과와 일치한다. 이상의 연구결과를 종합하면, 에스트로겐 부족은 복부대동맥조직과 복부대동맥의 PVAT에서 p67phox (NADPH oxidase subunit)을 증가시키고, adiponectin 단백과 AKT와 eNOS 인산화를 억제하지만, 이러한 현상은 규칙적인 저항성운동에 의해 효과적으로 개선될 수 있다. 그러나 PVAT는 혈관부위별 특성이 다르기 때문에 향후 운동이 혈관부위별 PVAT에 미치는 효과에 대한 기전연구가 보다 필요할 것으로 생각된다.
결 론
저항성운동이 난소절제모델의 복부대동맥과 PVAT에서 p67phox 단백질 발현을 유의하게 억제하고, adiponectin 단백질 발현과 AKT-eNOS 단백질의 인산화를 유의하게 증가시켰다.
REFERENCES
1. Violi F, Pignatelli P. Clinical application of NOX activity and other oxidative biomarkers in cardiovascular disease: a critical review. ARS. 2015;23(5):514-32.  2. Wang D, Wang C, Wu X, Zheng W, Sandberg K, et al. Endothelial dysfunction and enhanced contractility in microvessels from ovariectomized rats: roles of oxidative stress and perivascular adipose tissue. Hypertension. 2014;63(5):1063-9.   3. Mendelsohn ME, Karas RH. The protective effects of estrogen on the cardiovascular system. N Engl J Med. 1999;340(23):1801-11.   4. Man AWC, Zhou Y, Xia N, Li H. Perivascular adipose tissue as a target for antioxidant therapy for cardiovascular complications. Antioxidants (Basel). 2020;9(7):574.   6. Kumar RK, Darios ES, Burnett R, Thompson JM, Watts SW. Fenfluramine-induced PVAT-dependent contraction depends on norepinephrine and not serotonin. Pharmacol Res. 2019;140:43-9.   7. Chang L, Milton H, Eitzman D, Chen YE. Paradoxical roles of perivascular adipose tissue in atherosclerosis and hypertension. Circ J. 2013;77(1):11-8.   8. Margaritis M, Antonopoulos AS, Digby J, Lee R, Reilly S, et al. Interactions between vascular wall and perivascular adipose tissue reveal novel roles for adiponectin in the regulation of endothelial nitric oxide synthase function in human vessels. Circulation. 2013;127(22):2209-21.   9. Gao YJ, Takemori K, Su LY, An WS, Lu C, et al. Perivascular adipose tissue promotes vasoconstriction: the role of superoxide anion. Cardiovasc Res. 2006;71(2):363-73.   11. Galvez-Prieto B, Dubrovska G, Cano MV, Delgado M, Aranguez I, et al. A reduction in the amount and anti-contractile effect of periadventitial mesenteric adipose tissue precedes hypertension development in spontaneously hypertensive rats. Hypertens Res. 2008;31(7):1415-23.   12. Greenstein AS, Khavandi K, Withers SB, Sonoyama K, Clancy O, et al. Local inflammation and hypoxia abolish the protective anticontractile properties of perivascular fat in obese patients. Circulation. 2009;119(12):1661-70.   13. Modlinger P, Chabrashvili T, Gill PS, Mendonca M, Harrison DG, et al. RNA silencing in vivo reveals role of p22 phox in rat angiotensin slow pressor response. Hypertension. 2006;47(2):238-44.   15. Antonopoulos AS, Margaritis M, Coutinho P, Shirodaria C, Psarros C, et al. Adiponectin as a link between type 2 diabetes and vascular NADPH oxidase activity in the human arterial wall: the regulatory role of perivascular adipose tissue. Diabetes. 2015;64(6):2207-19.   16. Roberto C, Pasquale P, Simona B, Valerio S, Laura N, et al. Atorvastatin inhibits oxidative stress via adiponectin-mediated NADPH oxidase down-regulation in hypercholesterolemic patients. Atorvastatin inhibits oxidative stress via adiponectin-mediated NADPH oxidase down-regulation in hypercholesterolemic patients. Atherosclerosis. 2010;213(1):225-34.   17. Fujishima Y, Maeda N, Matsuda K, Komura N, Hirata A, et al. Effect of adiponectin on cardiac β-catenin signaling pathway under angiotensin II infusion. Biochem Biophys Res Commun. 2014;444(2):224-9.   19. Withers SB, Bussey CE, Saxton SN, Melrose HM, Watkins AE, et al. Mechanisms of adiponectin-associated perivascular function in vascular disease. Arterioscler Thromb Vasc Biol. 2014;34(8):1637-42.   20. Meziat C, Boulghobra D, Strock E, Battault S, Bornard I, et al. Exercise training restores eNOS activation in the perivascular adipose tissue of obese rats: Impact on vascular function. Nitric Oxide. 2019;86:63-7.   21. Irigoyen MC, Paulini J, Flores LJ, Flues K, Bertagnolli M, et al. Exercise training improves baroreflex sensitivity associated with oxidative stress reduction in ovariectomized rats. Hypertension. 2005;46(4):998-1003.   22. Goto C, Higashi Y, Kimura M, Noma K, Hara K, et al. Effect of different intensities of exercise on endothelium-dependent vasodilation in humans: role of endothelium-dependent nitric oxide and oxidative stress. Circulation. 2003;108(5):530-5.   24. Jun JK, Park HG, Li W, Lee YR, Jung JH, et al. Effects of endurance exercise on estrogen receptors, endothelin-1, and eNOS expression in aorta of OVX rats. Exerc Sci. 2016;25(3):159-65.  25. Idris AI. Ovariectomy/orchidectomy in rodents. Methods Mol Biol. 2012;816:545-51.   27. Wenger NK, Speroff L, Packard B. Cardiovascular health and disease in women. N Engl J Med. 1993;329(4):247-56.   28. Wang D, Luo Z, Wang X, Jose PA, Falck JR, et al. Impaired endothelial function and microvascular asymmetrical dimethylarginine in angiotensin II–infused rats: effects of tempol. Hypertension. 2010;56(5):950-5.   30. Xi W, Satoh H, Kase H, Suzuki K, Hattori Y. Stimulated HSP90 binding to eNOS and activation of the PI3-Akt pathway contribute to globular adiponectin-induced NO production: vasorelaxation in response to globular adiponectin. Biochem Biophys Res Commun. 2005;332(1):200-5.   31. Kuzkaya N, Weissmann N, Harrison DG, Dikalov SJJoBC. Interactions of peroxynitrite, tetrahydrobiopterin, ascorbic acid, and thiols implications for uncoupling endothelial nitric-oxide synthase. J Biol Chem. 2003;278(25):22546-54.  32. Wang J, Polaki V, Chen S, Bihl JC. Bihl. Exercise improves endothelial function associated with alleviated inflammation and oxidative stress of perivascular adipose tissue in type 2 diabetic mice. Oxidative Medicine and Cellular Longevity. 2020;2020:12.
|
|









