서 론
심혈관질환은 사망 원인의 주된 원인 중 하나로 남성에 비해 폐경 후 여성에서 높게 나타나는 것으로 보고되고 있다[1,2]. 이러한 이유는 폐경 후 여성에서 관찰되는 에스트로겐 결핍이 비만[3,4], 혈압[5] 및 동맥경직도의 증가[6]와 같은 여러 심혈관계 변화들의 시발점이 되기 때문이다.
에스트로겐은 심혈관 조직의 세포막, 세포질 및 핵에 존재하는 에스트로겐 수용체(estrogen receptors; ERα, ERβ, orphan G-protein coupled receptor)와 결합하여 세포내로 신호를 전달하는 것으로 알려져 있다[7,8]. 특히 ERα나 ERβ는 에스트로겐과 결합하여 ER-에스트로겐 복합체를 형성하여 핵으로 이동하여 다른 유전인자 발현에 영향을 주기도 하고, 간접적으로 단백질합성 후 변형을 유도하는 것으로 알려져 있다[8].
그러나 혈관조직에서 에스트로겐 부족은 활성산소종(ROS)의 증가와 endothelial nitric oxide synthase (eNOS) 발현 감소를 통해 산화질소(NO, nitric oxide) 생성을 감소시키고[1,2,9], 내피세포에서 분비되는 혈관수축물질인 Endothelin-1 (ET-1)을 증가시켜 내피세포 기능저하를 유발한다[10,11]. 특히 ET-1은 내피세포의 eNOS 단백을 감소시키고, 염증인자인 VCAM-1 단백의 증가를 통해 혈관 내피세포 기능저하를 유발하는바, 이는 extracellular-signal-regulated kinases 1/2 (ERK)단백에 의해 조절되는 것으로 알려져 있다[12].
또한 Guo et al. [13]은 ERα와 ERβ가 제거된 동물모델에서 에스트로겐이 eNOS-NO 증가를 통해 혈관이완반응을 유도하고, 이는 ERK의 활성화 때문이라고 보고하고 있고, Menaza et al. [8]도 총설에서 혈관내피세포의 ERα가 ERK와 eNOS의 활성화를 유발하여 혈관의 보호기능을 수행한다고 보고하고 있다.
규칙적인 신체활동은 이러한 내피세포 기능저하에 대한 보호 및 기능향상에 중요한 역할을 수행하는 것으로 알려져 있다[9,14,15]. 최근 지구성운동이 난소절제술(OVX)의 대동맥에서 ROS 생성의 억제[9], ET-1 발현의 억제 및 eNOS 발현의 증가를 통해 혈관기능을 개선할 수 있다는 것이 보고되었다[6,16].
그러나 이에 대한 기전은 아직 불분명하다. 혈관조직을 이용한 연구에서, ERα와 eNOS는 내피세포막의 Caveolae에 공존(co-localization)하고 있는 것으로 보고되었다[17,18]. 이는 ERα와 eNOS가 밀접한 관련이 있다는 것을 의미한다. 흥미로운 것은 혈관 내피세포에서 ERα에 의해 eNOS가 활성화되지만[19], 심장근에서는 ERβ에 의해 eNOS가 조절된다[20]. 또한 혈관 평활근세포에서 iNOS발현은 ERβ에 의해 증가되고 ERα에 의해 억제되는 것으로 보고되고 있다[21]. 뿐만 아니라 Gorres et al. [22]은 난소절제 모델의 지방세포에서 ERα이 감소되지만 골격근에서는 변화가 없음을 보고하고 있다. 이러한 연구결과들은 ER이 조직에 따라 상이한 반응이 나타나고, 운동에 의한 ER의 발현양상도 다르게 나타날 가능성이 있다.
그러나 에스트로겐 결핍에 따른 혈관조직의 반응에서 ER의 기능 및 이의 신호전달과정의 지구성운동의 효과에 관한 연구는 매우 부족한 실정이다. 이에 본 연구는 난소절제 모델을 이용하여 규칙적인 지구성운동이 혈관의 ER, ET-1, eNOS 및 ERK 단백 발현에 미치는 효과를 규명하고자 한다.
연구 방법
1. 실험동물
본연구는 중앙실험동물(주)에서 6주령의 암컷 쥐(Fischer344, n= 40)를 분양받아 1주간의 실험실 적응기를 거친 후, 통제군(Sham-operated control; SC, n=10), 난소절제통제군(Ovariectomized control; OC, n=10), 난소절제 저강도운동군(Ovariectomized low-intensity exercise; OL, n=10), 난소절제 중강도운동군(Ovariectomized moderate-intensity exercise; OM, n=10)으로 무선배정하였다. 사육실 평균온도는 22±1°C, 습도는 60±5%를 유지하며 주/야 사이클은 12시간 주기가 자동으로 조절되는 실험동물센터에서 사육하였다. 사료와 물은 충분히 공급하였고, C 대학교 동물실험윤리위원회 승인(CNU-00203)을 득한 후 실시하였다.
2. 난소절제술(OVX)
난소를 절제하기 위해, 마취제(Ketamine 80 mg/kg, xylazine 12 mg/kg)를 복강에 투여한 후, 요추1번과 3번의 배부위(dorsal region)를 삭모하고, 요추에서 좌우 1 cm 떨어진 부위를 절개하여 난소를 노출시켜 적출하였다. Sham 통제군은 난소를 노출시킨 후 다시 복원시켜 근육과 피부를 봉합하였다[23].
3. 지구성 운동훈련
난소제거 동물의 운동유형은 트레드밀을 이용한 유산소운동으로 선택하였다. 난소제거 후 일주일간의 실험실 적응기간 동안 트레드밀 운동적응기(8-10 m/min)를 거쳤다. 운동적응기가 끝난 후 저강도 운동 그룹은 준비운동 8-10 m/min로 5-10분간 실시한 후, 본 운동은 10-18 m/min 속도로 실시하였고, 중강도 운동그룹은 준비운동 10-15 m/min로 5-10분간 실시한 후, 본 운동은 15-26 m/min 속도로 실시하였다[23]. 운동 빈도는 1주일에 5일간 실시하였고 운동기간은 16주 동안 수행하였다.
4. 혈액 분석
혈액검사를 위해 마지막 운동이 종료된 후 최소 24시간이 지나고 8시간 이상 공복을 유지한 후 채혈하였다. 전신 마취제(Ketamine 80 mg/kg, xylazine 12 mg/kg)를 복강에 투여한 후, 복부 대동맥에서 10 ml의 혈액을 채혈한 후 원심분리하여 혈장을 추출하여 분석시까지 -70°C에 냉동보관하였다. 중성지방(Triglyceride), 총콜레스테롤(Total cholesterol) 및 고밀도지단백 콜레스테롤(High density lipoprotein)은 Fuji 7000i 자동생화학분석장치(Fujifilm, Japan)를 이용하여 분석하였다.
5. 대동맥 적출 및 Western blot
혈관의 단백질 발현을 확인하기 위하여 대동맥(Thoracic area)을 적출하여 액체질소에 급랭시키고, -80°C에 보관하였다. 적출된 대동맥은 lysis buffer (Sigma, USA)에서 균질화되고, 균질화된 조직은 4°C에서 14,000 rpm으로, 30분간 원심분리하여 상층액을 분리한 후, BCA assay Kit (Bio-rad, USA)를 사용하여 단백질을 정량하였다. 50 μg의 단백질을 9% SDS-PAGE에서 전기영동한 후 PVDF membrane으로 전이시켰다. Membrane의 비특이적인 반응은 5% nonfat dry milk로 1시간 동안 반응시켜 제거하였다. ERα, ERβ, NOS, p-eNOS, ERK, p-ERK (1:1,000, Cell signaling, USA)와 β-actin (1:1,000, Sigma, USA)의 일차 항체는 4°C에서 18시간 동안 반응시켰고, 이차 항체는 HRP가 부착된 rabbit-antimouse IgG (Calbiochem, USA)를 이용하였다. 반응의 확인은 ECL detection system (Thermo, USA)을 이용하여 분석하였다.
연구결과
1. 체중의 변화
규칙적인 지구성운동이 OVX모델에서 체중의 감소를 유발하는지 확인하였다(Table 1). 체중은 SC에 비해 OC에서 유의하게 증가되었다(p<.05, 66.9±14.3 g vs. 127.1±28.6 g). 이러한 체중의 증가는 중강도 지구성운동(OM)에 의해 유의하게 억제되었다(p <.05, 66.9 ±14.3 g vs. 103.1±25.1 g). 그러나 저강도 지구성운동(OL)과는 유의한 차이가 나타나지 않았다.
2. 혈중 혈중지질의 변화
혈중 TG농도는 SC에 비해 OC에서 유의하게 증가되었고(p <.05, 15.7±5.4 vs. 27.8±7.9), 이러한 TG의 증가는 중강도 지구성운동(OM)에 의해 유의하게 억제되었으나(p<.05, 27.8±7.9 vs. 20.2±5.3), 저강도 지구성운동(OL)은 TG의 증가를 억제하지 못하였다. 또한 TC, HDL-C, 혈당은 SC에 비해 OC에서 모두 유의하게 증가되었으나(p<.05, SC vs. OC), 지구성운동과는 유의한 차이가 나타나지 않았다.
3. ER의 변화
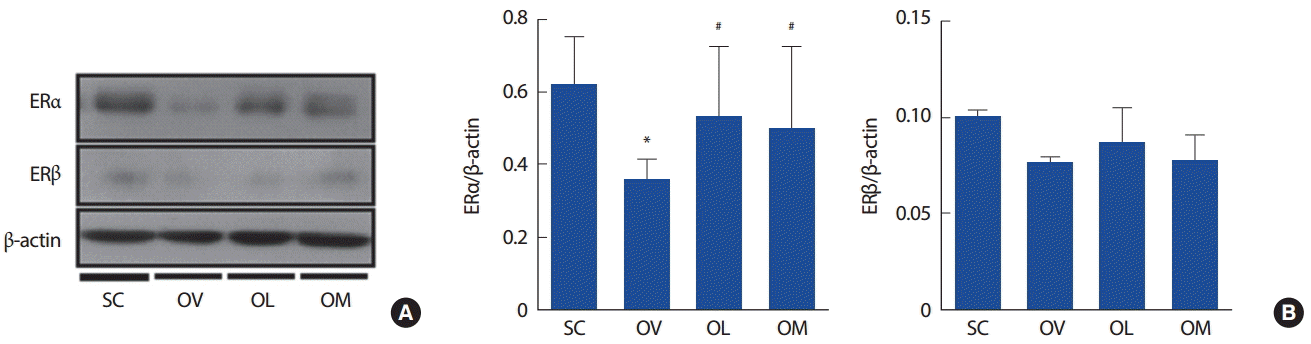
ER단백 발현이 지구성운동에 의해 변화되는지 OVX모델의 대동맥에서 확인하였다(Fig. 1). ERα 단백 발현은 SC에 비해 OC에서 유의하게 감소되었고(p<.05, 0.62±0.13 vs. 0.36±0.06), OC에 비해 OL과 OM에서 유의하게 증가된 것으로 나타났다(p <.05, 0.36 ±0.06 vs. 0.53±0.19, 0.50±0.22). 그러나 OL과 OM은 집단간 차이가 나타나지 않았다. 또한 ERβ 단백 발현은 집단간 차이가 나타나지 않았다.
4. endothelin-1의 변화
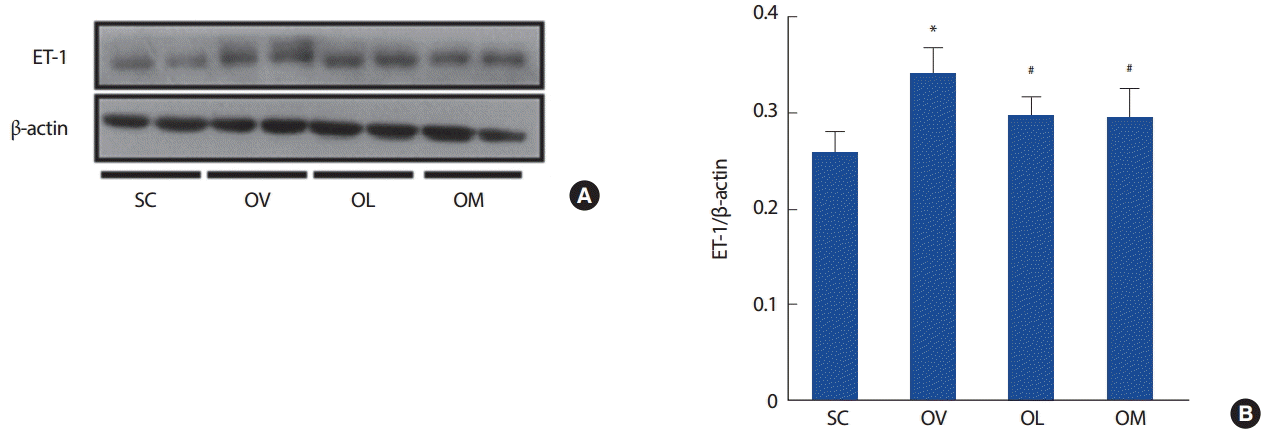
지구성운동이 혈관수축 유발물질로 알려진 ET-1 단백 발현을 OVX모델의 대동맥에서 확인하였다(Fig. 2). ET-1 단백 발현은 SC에 비해 OC에서 유의하게 증가되었고(p<.05, 0.26±0.02 vs. 0.34±0.03), OC에 비해 OL과 OM에서 유의하게 감소되었다(p<.05, 0.34±0.03 vs. 0.30±0.02, 0.29±0.03). 그러나 OL과 OM은 유의한 차이가 나타나지 않았다.
5. eNOS 및 ERK의 변화
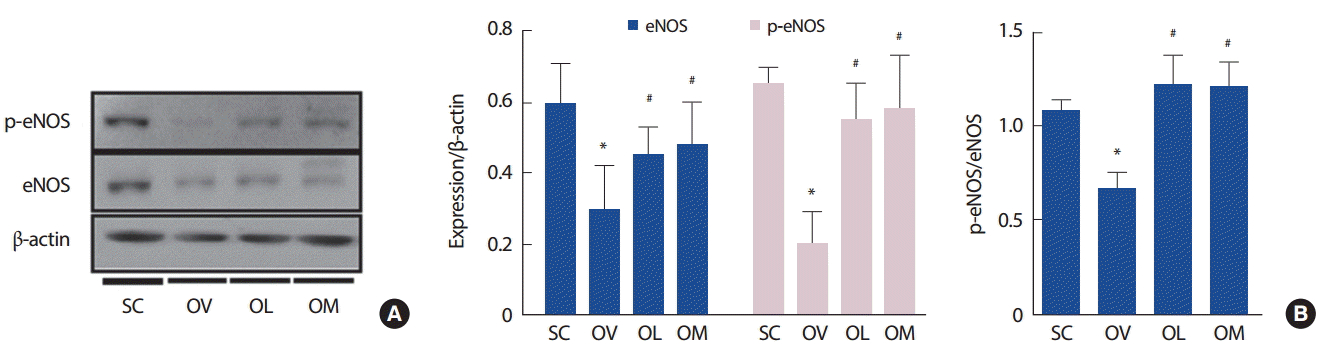
지구성운동이 eNOS와 ERK의 발현과 인산화를 OVX모델의 대동맥에서 확인하였다(Fig. 3, 4). eNOS 단백발현과 인산화는 각각 SC (0.60±0.11, 0.65±0.05)에 비해 OV (0.3±0.12, 0.20±0.09)에서 유의하게 감소되었으나(p<.05), OV에 비해 OL (0.45±0.08, 0.55±0.10)과 OM (0.48±0.12, 0.58±0.15)에서 유의하게 증가되었다(p<.05). 그러나 OL과 OM은 유의한 차이가 나타나지 않았다. p-eNOS/eNOS의 발현비율도 SC에 비해 OV에서 유의하게 감소되었으나(p<.05), OV에 비해 OL과 OM에서 유의하게 증가되었다(p<.05). 그러나 OL과 OM은 유의한 차이가 나타나지 않았다.
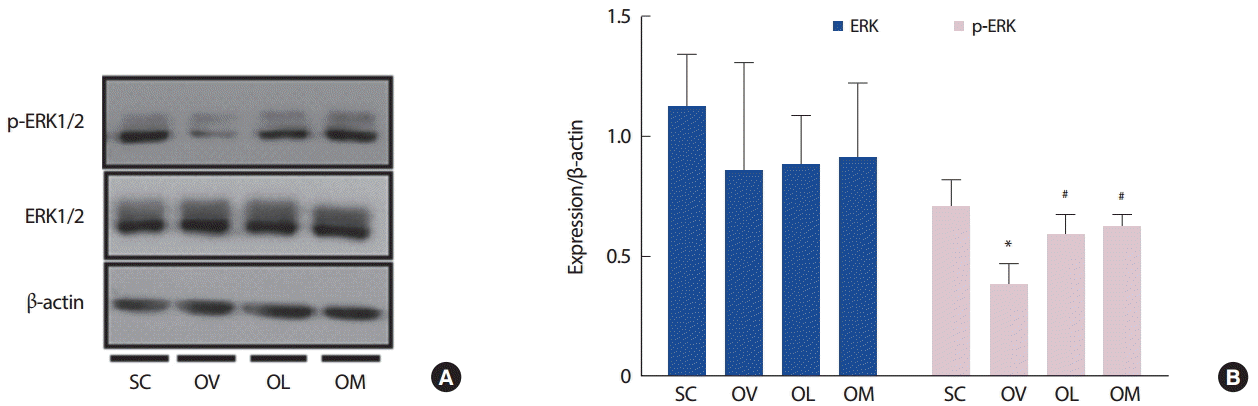
ERK 인산화는 SC (0.71±0.11)에 비해 OV (0.38±0.09)에서 유의하게 감소되었으나(p<.05), OV에 비해 OL (0.58±0.09)과 OM (0.62±0.06)에서 유의하게 증가되었다(p <.05). 그러나 OL과 OM은 유의한 차이가 나타나지 않았다. 또한 ERK 단백발현은 집단간 유의한 차이가 나타나지 않았다.
논 의
페경 후 여성은 폐경전에 비해 비만이나 동맥경화와 같은 심혈관질환의 위험성을 증가시킨다[24]. 이는 에스트로겐이 혈관의 내피세포 및 평활근에 작용하여 혈관이완, 항산화 및 항염증 작용을 하기 때문이다[9,25].
에스트로겐은 ER과 결합하여 세포내로 신호를 전달함에 있어 2가지 경로를 경유하는 것으로 보고되고 있다. 하나는 에스트로겐이 세포내에 존재하는 ER과 결합하여 핵으로 이동한 후 다른 유전인자의 발현에 영향을 미치고, 다른 하나는 세포막에 존재하는 ER과 결합하여 세포내로 신호를 전달한다[8].
OVX모델의 대동맥에서 ERα발현이 감소된다는 보고[22]와 인간을 대상으로 폐경 여성의 내피세포에 존재하는 ERα발현이 폐경 전의 여성에 비해 약 33% 낮다는 보고[26] 등을 볼 때, ER은 에스트로겐에 의해 조절된다는 것을 의미한다. 즉 에스트로겐의 부족이 이러한 에스트로겐-ER의 신호전달을 감소시켜 결국 심혈관질환을 야기할 가능성이 있다.
Gue et al. [13]은 혈압증가에 의한 혈관이완반응이 ERα와 ERβ를 제거한 동물모델(knock-out, KO)에서는 관찰되지 않음을 보고하고 있다. 그러나 ERα와 ERβ는 조직에 따라 그 기능이 다르게 나타나는 것으로 보고되고 있다[19,20]. 또한 Intapad et al. [7]은 OVX모델의 대동맥에서 OVX가 ERα 발현을 감소시키지만 ERβ는 변화되지 않음을 보고하고 있다.
운동은 혈관의 혈류 증가에 의한 shear stress를 유발하여 혈관이완 기능을 향상시킨다. Tarhouni et al. [27]은 ERα와 ERβKO모델을 이용하여 장기간의 혈류(high-flow; shear stress) 반응을 확인하였는데, shear stress가 ERαKO모델의 동맥에서 혈관이완을 증가시키지만 ERβKO모델의 동맥에서는 변화되지 않음을 보고하였다.
본 연구에서도 ERα 단백발현이 OVX의 대동맥(OC)에서 정상군(SC)에 비해 감소되었으나 이러한 OVX에 의한 ERα 단백발현의 감소는 지구성운동에 의해 효율적으로 개선되었다. 그러나 ERβ 단백발현의 변화는 나타나지 않았다(Fig. 1). 이러한 결과는 지구성운동이 혈관의 ERα발현에만 특이적으로 작용한다는 것을 의미한다.
에스트로겐 부족에 따른 혈관 내피세포 기능저하의 원인 중 하나가 Endothelin-1 (ET-1)이다. ET-1은 혈관내피세포에서 분비되는 혈관수축 물질로서 내피세포의 eNOS 단백을 감소시켜 혈관 내피세포의 기능저하를 유발한다[10,11].
최근의 ET-1과 eNOS에 관한 지구성운동의 연구를 살펴보면, 난소 절제 모델(OVX)의 혈관조직에서 지구성운동은 ET-1단백을 감소시키고, eNOS단백을 증가시킨다[6,16]. 또한 이러한 eNOS발현은 저항성운동에 비해 지구성운동이 효율적이며, ET-1 발현의 억제는 지구성운동과 저항성운동이 동일한 효과가 있는 것으로 나타났다[15]. 또한 Braga et al. [9]은 난소절제 모델(OVX)의 혈관에서 지구성운동이 OVX통제군에 비해 ROS생성의 억제와 NO 생성의 증가를 통해 내피세포의 기능저하를 효과적으로 억제하였음을 보고하였다.
본 연구에서도 ET-1 단백발현이 OVX의 대동맥(OC)에서 정상군(SC)에 비해 증가되었다. 또한 eNOS발현과 인산화도 OVX에 의해 감소되었다. 그러나 지구성운동(OL, OM)은 OVX에 의해 유발되는 ET-1의 증가와 eNOS의 감소를 효과적으로 개선하였다(Fig. 2,3). 이러한 결과는 에스트로겐 부족이 ET-1과 NO의 불균형을 초래하여 혈관기능 저하를 유발하지만, 이러한 불균형은 규칙적인 지구성운동(OL, OM)에 의해 효과적으로 개선될 수 있다는 것을 의미한다.
최근에 Lin et al. [12]은 ET-1이 내피세포에서 VCAM-1 단백 발현을 증가시켜 혈관의 염증을 유발하는바, 이는 ERK의 활성에 의해 나타난다고 보고하였다. 뿐만 아니라 ERα에 의한 PI3K-AKT-eNOS의 신호전달과정에도 ERK가 관여하는 것으로 보고 되고 있다[8]. 본 연구에서도 ERK 인산화가 OVX에 의해 감소되었다. 그러나 지구성운동(OL, OM)은 OVX에 의한 ERK의 감소를 효과적으로 개선하였다(Fig. 4). 이러한 결과는 지구성운동이 OVX모델의 혈관조직에서 ERα/PI3K 복합체를 형성하여 ERK-eNOS 활성을 유도한 것으로 생각된다.
그러나 지구성운동의 이러한 긍정적인 효과에도 불구하고, 저강도 지구성운동은 OVX에 의한 체중과 TG의 증가를 억제하지 못했다(Table 1). 비록 저강도 지구성운동이 OVX모델에서 체중이나 TG의 변화에 영향을 주지 못할 지라도, 혈관조직에서 ET-1을 감소시키고, ERα, eNOS 및 ERK를 활성화시키는 것으로 볼 때, 저강도 지구성운동은 에스트로겐의 신호를 세포내로 충분히 전달하여 혈관보호 및 기능의 향상에 도움을 줄 수 있다고 생각한다.
이상의 연구결과를 종합하면, 운동강도에 관계없이 규칙적인 지구성운동은 OVX의 혈관조직에서 ET-1발현을 억제하고, ERα-ERK-eNOS의 활성을 증가시켜 혈관기능을 개선시킬 수 있다고 사료된다. 그러나 중강도 지구성운동은 체중과 TG의 변화에 긍정적인 영향을 미쳤지만 저강도 운동은 효과가 없었다. 따라서 에스트로겐 부족(폐경)에 의한 심혈관질환에서 혈관기능을 개선하기 위해서는 중강도의 규칙적인 지구성운동이 저강도운동보다 효과적일 수 있다고 사료된다.
결 론
본 연구는 난소적제술 모델을 대상으로 16주간의 지구성운동훈련을 실시한 후, 혈관의 ER, ET-1, eNOS 및 ERK 단백 발현에 미치는 변화를 확인하였다. 그 결과, 지구성운동훈련이 난소적제술에 의한 체중의 증가와 대동맥의 ET-1단백 발현의 증가를 효율적으로 억제하고, ER α 및 eNOS와 ERK 단백의 인산화를 증가시켰다. 그러나 운동강도별 차이는 나타나지 않았다. 따라서 지구성운동은 에스트로겐 부족에 의한 혈관의 ET-1 증가를 효율적으로 억제하고, ERα, ERK 및 eNOS 활성의 증가를 통해 혈관기능 개선에 도움을 줄 것으로 사료된다.