서 론
비만한 지방세포는 염증성 사이토카인(cytokine) 분비를 촉진시키기 때문에 오늘날에는 비만을 만성적 염증상황으로(chronic low-grade inflammation) 규정하고 있다[1-3]. 염증은 당뇨병, 심혈관 질환 등과 같은 대사질환 발병과도 관계가 깊어 이를 해결하기 위한 다방면의 연구들이 시도되고 있다[4].
지방조직은 그 위치에 따라 내장지방과 피하지방으로 구별되고, 그 크기나 구조에 따라서 생물학적인 기능에서 차이를 나타낸다. 특히, 내장지방은 제2형 당뇨와 같은 대사질환의 발병과 관계가 깊고[5] 피하지방은 인슐린 저항성 유발과 관련이 깊은 것으로 보고되고 있지만[6] 해부학적으로 위치가 다른 내장지방과 피하지방에서 염증반응을 조절하는 기능차이에 관해서는 명확히 알려져 있지 않은 상태이다.
최근 비만관련 연구들에 의하면 비만동물의 지방조직에서 염증성 사이토카인과 케모카인(chemokine) 생성이 증가되는 원인 중의 하나는 지방조직 내 대식세포의 분화과정에서 대사적 불균형이 염증상황을 더욱 악화시키는 요인임을 제시하였다[7,8]. 대식세포는 환경에 따라 서로 다른 형태(heterogeneity)로 분화하는 것으로 알려져 있다. 일반적으로 대식세포 M1상태는 TNF-α, IL-6 등과 같은 염증성 사이토카인 생성이 증가하고, 대식세포 M2상황에서는 IL-4, IL-13같은 항염증사이토카인 생산이 증가함으로써 지방조직의 대사적 균형을 유지한다[7]. Lumeng et al. [7]은 비만동물의 지방조직에서는 대식세포 분화가 M2에서 M1상황으로 전환되었음을 입증하면서, M1/M2 상황의 불균형은 대사성질환 발병과 관계가 깊다고 하였다. 이에, 지방조직에서 염증반응을 촉진시키는 인자로 알려진 대식세포 침윤을 억제하거나, 세포 내 염증신호 경로를 차단하는 치료방법을 연구하는 것은 비만 개선을 위해 학문적으로도 의미 있는 일이라 할 수 있겠다.
비만 개선을 위해서는 식이조절과 운동요법이 추천되고 있는데, 규칙적인 운동은 비만동물이나 비만인의 혈중에서 염증성 사이토카인 농도를 감소시키고 항염증성 사이토카인 분비를 증가시켜 대사질환 예방을 위한 치료도구로 권장되고 있다[9,10]. 또 다른 방법으로는 폴리페놀(polyphenol)을 식이에 이용한 연구들이 활발하게 시도되고 있는데, 폴리페놀의 항비만 효과는 스트레스에 대한 항산화작용[11], 항염증작용[12] 등이 보고되고 있다. 폴리페놀의 일종인 라스베라트롤은 지방세포에서 분비되는 염증분자의 발현을 감소시킴으로써 지방세포에서 염증반응을 억제하는 기능이 보고되고 있다[13]. 선행연구 결과들을 종합해보면, 저지방식이와 운동 또는 저지방식이와 폴리페놀 복합처치는 비만으로 인해 증가된 대식세포 침윤을 억제하여 지방조직에서의 염증상황을 개선할 수도 있음을 시사하고 있다.
이에 본 연구는 두 가지 가설을 설정하였다. 첫째, 비만개선에 효과적인 방법으로 알려진 저지방식이와 함께 운동 또는 저지방식이와 라스베라트롤 섭취를 병행한다면 대식세포 침윤을 억제하고 염증상황의 조절에 긍정적인 효과를 나타낼 수 있을 것이다. 둘째, 운동과 폴리페놀의 복합처치가 내장지방과 피하지방에서 유전자 발현의 기능적 차이를 나타내는지 규명하고자 시도되었다.
연구 방법
1. 연구 대상 및 식이조성
본 연구는 5주령의 C57BL/6 종으로 총 25마리를 (주)중앙동물에서 분양 받아 1주일간 적응기간을 두었다. 동물의 사육환경은 평균 온도 22±2℃, 습도 50±5%, 주/야 순환은 12시간(06:00-18:00 주간시간)주기로 유지하였다. 비만 유도는 선행연구에 12주간 고지방 식이를 자유롭게 섭취하도록 하였다. 비만유도 후 모든 마우스는 총 칼로리의 10% 지방이 함유된 저지방식이로 전환한 후 8주 동안 처리하였다(LFD, D12450B, Research Diets New Brunswick, NJ). 집단분류는 총 5 집단으로 고지방식이 통제군(high-fat diet: HD, n=5), 저지방식이 통제군(low-fat diet: HLC, n=5), 저지방식이와 라스베라트롤(low-fat diet+resveratrol: HLR, n=5), 저지방식이와 운동군(low-fat diet+exercise: HLE, n=5), 저지방식이와 운동 그리고 라스베라트롤군(low-fat diet+resveratrol+exercise: HLER, n =5)으로 하였다. 실험동물 윤리위원회(Institutional Animal Care and Use Committee, No. 2009-3-29)에 계획서를 제출하고 승인받았으며, C대학교 동물실험 위원회의 취급 규정에 따라 사육하고 실험하였다.
2. 운동 및 라스베라트롤 투여 방법
운동은 트레드밀 운동으로 실시하였고 일주일간의 적응기간(8 m/min의 속도)을 거친 후, 준비운동은 8-15 m/min로 5-10분간 실시하고, 본 운동은 10-22 m/min 속도로, 운동시간은 30-60분간으로 점증적 과부하 원리를 적용하였다. 이 속도는 쥐과 동물의 최대 산소섭취량 60-76% 정도로 중 강도에 해당하는 운동강도로 이용되었다[14]. 운동 빈도는 1주일에 5일 간 8주 동안 수행하였으며, 통제집단도 운동집단과 똑같은 환경적 스트레스에 노출시키고, 사료와 물의 공급도 제한하였다. 라스베라트롤은 건조된 라스베라트롤을 구입하여(Sigma, St. Louis, MO, USA) 50%의 propylene glycon에 충분히 녹인 후 HLR, HLER 그룹에 체중 당 10 mg/kg의 농도로 경구 투여하였다. 나머지 그룹에도 동량의 propylene glycon 용액을 경구 투여하였다.
3. 체중측정 및 지방조직 적출
체중은 미세저울을 이용해 일주일에 1번 측정하여 기록하였다. 마지막 운동이 끝난 24시간 후 모든 동물을 희생시켰으며, 분석을 위해서 백색지방조직(white adipose tissue, WAT)은 해부학적 위치에 따라 부고환 지방(epididymal fat), 신장주변지방(retroperitoneal fat), 장간막지방(mescentric fat) 그리고 피하지방(subcutaneus fat)을 적출하고 생리식염수(0.9% NaCl)에 세척한 후 액체질소에 넣어 분석 시까지 -70℃에 냉동 보관하였다.
4. RNA 추출
Total RNA을 추출하기 위해서 Trizol 1 mL에 비복근 조직 200 mg을 넣고 homogenizer를 이용하여 20초 동안 조직을 간 후 상온에서 5분간 방치하였다. 여기에 chloroform (Sigma, USA) 200 μL를 첨가하고 chloroform이 잘 섞이도록 15초 동안 혼합하며, 상온에서 3분간 방치한 후 원심분리(13,000 rpm, 4℃, 15분) 하였다. 원심분리 후 상층액을 새 튜브에 분리하고 동량의 isopropanol (Sigma, USA)을 첨가하여 상온에서 10분간 방치한 후 원심분리(13,000 rpm, 4℃, 10분) 하였다. 원심분리로 바닥에 형성된 RNA pellet에 70% ethanol 1 mL를 첨가하여 2회 세척(4,500 rpm, 4℃, 5분) 한 후, RNA pellet이 완전히 건조되면 0.01% DEPC로 처리된 증류수를 150 μL 첨가하여 RNA pellet을 용해시켰다. Forward 및 reverse primer의 배열은 Table 1에 나타난 바와 같다.
5. RT-PCR
Reverse transcription-polymerase chain reaction (RT-PCR)을 이용하여 mRNA의 양을 측정하였다. Complementary DNA는 total RNA 2 μg과 reverse primer 0.5 μg을 혼합하여 최종 약 14 μL를 준비하여 75℃에서 15분 동안 열처리(heating)한 후, 5분 동안 얼음 속에 보관하였다. 여기에 5X M-MLV reaction buffer, 10 mM dNTP mixture, 200 units MMLV RT (Promega, Madison, WI, USA)를 첨가하여 최종 양이 25 μL가 되게 한 후, 42℃에서 1시간 동안 반응시킨다. RT reaction 5 μL에 10X reaction buffer (Mg2+포함), 10 mM dNTP, 5 unites Taq polymerase (Solgent, Taeon, South Korea), 그리고 10 μM primer를 첨가하여 최종 50 μL가 되게 한 후, RTC-100TM Programmable Thermal Controller (MJ Research, INC., Waltham, MA, USA)를 이용하여 PCR을 실시하였다.
연구결과
1. 체중 및 지방조직 무게의 변화
8주간의 처치 후 체중과 지방조직 무게의 변화는 Table 2와 같다. 체중은 HD 그룹과 비교해 HLC, HLR, HLE, HLER 그룹 모두 효과적으로 감소하였다. 더욱이 HLE, HLER 그룹의 체중은 HLC 그룹과도 통계적으로 유의한 감소를 나타냈다.
백색지방조직의 부고환지방, 신장주변지방, 장간막지방 그리고 피하지방 무게는 HD 그룹과 비교해 HLC, HLR, HLE, HLER 그룹 모두 효과적으로 감소하였다. 부고환지방 무게는 HLE, HLER 그룹에서 HLC 그룹과 비교해 유의한 감소를 나타냈다.
2. F480, CD11c, CD163 mRNA 변화
고지방식이로 유도된 비만 쥐의 내장지방과 피하지방에서 저지방식이와 운동 그리고 라스베라트롤의 효과를 증명하기 위해 F480, CD11c, and CD163을 분석하였다(Fig. 1).
대식세포 침윤 표시자인 F480 mRNA 발현은 내장지방과 피하지방 모두에서 HD 그룹과 비교해 HLR, HLE, HLER 그룹에서 효과적으로 감소하였다. M1 표시자 CD11c mRNA 발현은 내장지방과 피하지방 모두에서 HD 그룹과 비교해 HLE, HLER 그룹에서만 유의하게 감소되었다. M2 대식세포 표시자 CD163 mRNA 발현은 내장지방에서만 HD 그룹과 비교해 HLE, HLER 그룹에서 유의하게 증가하였다. 피하지방에서는 HLER 그룹에서만 유의하게 증가하였다.
3. MCP-1, ICAM-1, VCAM-1 mRNA 변화
고지방 식이로 유도된 비만 쥐의 내장지방과 피하지방에서 저지방식이와 운동 그리고 라스베라트롤의 효과를 증명하기 위해 MCP-1, ICAM-1, and VCAM-1을 분석하였다(Fig. 2).
내장지방에서 MCP-1 mRNA 발현은 HD 그룹과 비교해 HLR, HLE, HLER 그룹에서 유의하게 감소하였으나 피하지방에서는 그룹 간 유의한 차이를 나타내지 못하였다.
내장지방에서 ICAM-1 mRNA 발현은 HD 그룹과 비교하여 HLE와 HLER 그룹에서만 통계적으로 유의한 감소를 나타냈고, HLE, HLER 그룹은 HLC 그룹과도 ICAM-1 mRNA 발현에 유의한 감소를 나타내었다. 피하지방에서는 그룹 간 차이를 나타내지 못하였다. 내장지방에서 VCAM-1 mRNA 발현은 HD 그룹과 비교하여 HLR, HLE, 그리고 HLER 그룹에서 유의한 감소를 나타내었고, 피하지방에서는 그룹 간 차이를 나타내지 못하였다.
4. TLR4, IL-6, TNF-α mRNA 변화
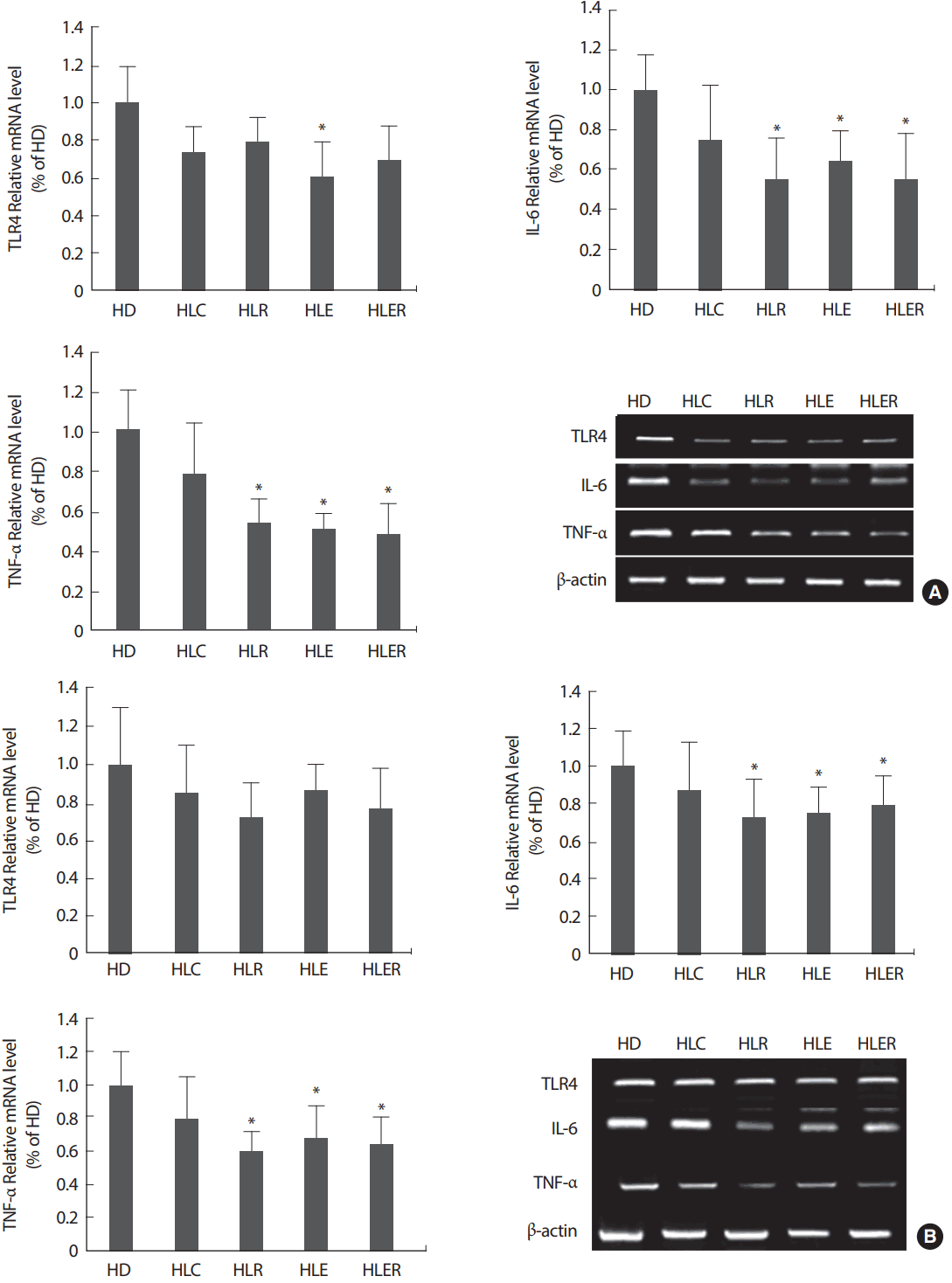
고지방식이로 유도된 염증반응에 관해 저지방식이와 운동 그리고 라스베라트롤의 효과를 증명하기 위해 내장지방과 피하지방에서 TLR4, IL-6, and TNF−α를 분석하였다(Fig. 3).
내장지방에서 염증 신호에 관여하는 TLR4 mRNA 발현은 HD 그룹과 비교하여 HLE 그룹에서만 유의하게 감소하였고, 피하지방에서는 그룹 간 유의한 차이를 나타내지 못하였다. 또한 내장지방과 피하지방에서 염증성 사이토카인 IL-6와 TNF−α mRNA 발현은 각각 HD 그룹과 비교하여 HLR, HLE, 그리고 HLER 그룹에서 효과적으로 감소되었다.
논 의
본 연구는 비만 개선을 위해 저지방식이와 운동 그리고 저지방식이와 라스베라트롤 처치가 내장지방과 피하지방에서 대식세포 침윤과 염증반응 조절기능을 규명하기 위해 시도되었다.
8주 간의 처치 후 체중과 내장지방, 피하지방의 무게는 HD 그룹과 비교하여 HLC, HLR, HLE, HLER 그룹 모두에서 효과적으로 감소되었다. 또한 HLE, HLER 그룹은 HLC 그룹과도 비교해 체중과 지방조직 무게에서 유의한 차이를 나타냈다. 이러한 결과는 비만 치료를 위해서는 운동과 식이를 병행하는 것이 체중과 지방무게 감소에 더욱 효과적이라고 보고한 선행연구들과도 일치하는 결과를 나타냈다[15,16].
HLR 그룹은 HD 그룹과 비교해 체중과 지방조직 무게에서 감소하였지만, 저지방식이만 처치한 HLC 그룹과는 유의한 차이를 나타내지 못하였다. 라스베라트롤과 관련된 선행연구를 고찰해보면 고지방 식이와 라스베라트롤 병행섭취는 체중과 지방조직 무게의 증가를 억제하는 기능이 있는 것으로 보고되고 있으나[17,18] 또 다른 연구에서는 지방간 지수에서만 미비한 개선이 나타났고 체중 변화에는 특별한 효과를 나타내지 못한 것으로 보고되었다[19,20]. 선행연구를 정리해보면, 라스베라트롤은 고지방식이로 인해 발생되는 대사적 불균형을 일부분 억제하는 기능이 있는 것으로 생각된다. 또한 폴리페놀의 처치기간이나 처치농도에 따라서 서로 상반된 결론이 보고되고 있어 폴리페놀의 항비만 효과를 규명하기 위해서는 다양한 후속 연구들이 지속적으로 시도되어야 할 것이다.
비만동물의 지방조직에서 대식세포 분화는 M2에서 M1 상황으로 전환됨을 증명하고 이는 대사성질환 발병과도 관계가 깊은 것으로 알려져 있다[2]. 본 연구에서도 HD 그룹은 다른 그룹들과 비교해 대식세포 마커 F480 mRNA 발현이 현저히 증가되었다. 하지만 8주간의 처치 후, 내장지방과 피하지방에서 F480 mRNA 발현은 HLR, HLE, HLER 그룹에서 효과적으로 감소되었음을 확인하였다. 이는 고지방식이로 유도된 비만동물의 지방조직에서 대식세포 침윤을 차단 후 염증성 사이토카인 발현이 현저하게 감소되었음을 보고[21]한 선행연구와도 일치하는 결과이다. 본 연구에서 사용된 처치방법 HLR, HLE, HLER의 복합처치는 지방조직에서 대식세포 침윤을 효과적으로 감소시킴으로써 염증성 사이토카인의 발현을 조절할 수 있는 항염증기능을 간접적으로 증명한 것으로 사료된다.
Noriaki et al. [22]은 16주간의 유산소운동을 통해 비만동물의 지방조직에서 M1 대식세포 상황을 M2 대식세포 상황으로 전환시켰음을 입증하였다. 본 연구 결과에서도 내장지방과 피하지방에서 M1 대식세포 알려진 CD11c mRNA는 HLE, HLER 그룹에서 효과적으로 감소되었고, M2 마커로 알려진, CD163 mRNA는 내장지방에서만 HLE, HLER 그룹에서 유의하게 증가되었다. 피하지방에서는 단지 HLER 그룹에서만 유의하게 증가되었다. 이러한 결과는 Noriaki et al. [22] 연구결과와도 일치하는 결과를 나타냈으며, 더욱이 본 연구에서는 내장지방, 피하지방 모두에서 HLE, HLER의 병행은 M1 대식세포 표시자로 알려진 CD11c mRNA 발현을 억제시키고, M2 대식세포 표시자로 알려진 CD163 mRNA 발현이 증가되었다. 이러한 결과는 규칙적인 유산소운동은 피하지방과 내장지방 무게를 감소시키고 지방조직의 위치에 관계없이 대식세포 분화과정에도 긍정적인 역할을 수행 할 수 있음을 증명하였다.
현재까지 운동이 대식세포 침윤과 분화과정을 조절하는 분자적 기전에 대해서는 명확하게 밝혀져 있지 않은 상태이나 한 가지 가능성은 지방세포에서 유래된 MCP-1은 지방조직으로의 대식세포 침윤을 유도하여 염증상황을 유발하는데 중요한 역할을 하며[21], 피하지방 보다는 내장지방과 더욱 밀접한 관계가 있는 것으로 보고되고 있다[5]. 하지만 규칙적인 운동은 케모카인이나 협착분자들의 발현을 효과적으로 감소시켜 대사적 불균형을 개선시키는 것으로 보고되고 있다[9,10]. 본 연구에서도 내장지방에서 MCP-1, ICAM-1, 그리고 VCAM-1 mRNA 발현은 HLE, HLER 그룹에서 효과적으로 감소하였고, 피하지방에서는 그룹 간 차이를 나타내지 못하여, 저지방식이와 운동의 병행은 내장지방에서 MCP-1, ICAM-1, 그리고 VCAM-1 mRNA 발현을 억제함으로써 지방조직으로의 대식세포 침윤을 감소시키고 M1 상황에서 M2 상황으로의 긍정적인 분화를 유도하였을 것으로 사료된다.
하지만, 내장지방과 피하지방에서 HLR은 F480 mRNA 발현을 유의하게 억제시켰음에도 불구하고 M1과 M2 상황의 조절과 케모카인 그리고 협착분자 발현에는 어떠한 영향도 미치지 못하였다. 최근에는, 라스베라트롤의 비만개선 효과는 식이조절과 비슷하다는 연구들이 보고되고 있고[18,19], Erlund et al. [11]는 폴리페놀 처치는 낮은 농도 보다는 높은 농도를 처치한 그룹에서 식이제한 그룹과 비슷한 효과를 나타낸 것으로 보고하였다. 따라서 라스베라트롤이 비만을 개선하는 효과는 식이조절과 비슷하거나 처치 농도에(dose-response)에 의존적이라는 것을 확인할 수 있었다.
지방조직에서 염증수용체 TLR4 활성은 하위기전에 있는 TNF-α와 IL-6의 발현을 유도하여 염증상황을 유도하는 인자로 잘 알려져 있다. 본 연구에서도, HD 그룹의 내장지방에서 TLR4 mRNA 발현은 현저히 높게 발현되었다. 하지만 8주간의 복합처치 후 HLE, HLER 그룹은 TLR4 mRNA 발현을 유의하게 감소시켰으나, 피하지방에서는 유의한 차이를 나타내지 못하였다. 또한 HD 그룹의 내장지방과 피하지방에서 높게 발현된 IL-6, TNF−αmRNA 발현은 각각 HLR, HLE, 그리고 HLER에 의해 감소된 것을 확인하였다. 일반적으로 IL-6, TNF−α와 같은 염증성 사이토카인은 내장지방과 깊은 관계가 있는 것으로 보고되고 있다[2]. 그러나 Karla et al. [23]의 연구에서는 내장지방과 피하지방 모두 염증성 사이토카인 IL-6 발현과 깊은 관계가 있음을 보고하였다. 본 연구에서도 비만동물의 내장지방과 피하지방에서 HLR, HLE, 그리고 HLER의 병행은 IL-6, TNF−α 발현을 억제하는데 긍정적인 효과를 나타냈다. 지금까지의 선행연구들에서는 내장비만과 염증상황과의 관계만을 강조한 반면에, 본 연구에서는 내장지방과 피하지방 모두 만성적 염증상황과 관련이 있음을 입증하였다. 또한 HLR, HLE, 그리고 HLER의 병행은 비만으로 유발되는 염증상황을 효과적으로 개선하여 비만개선을 위한 치료도구로 활용될 수 있음을 증명하였다. 따라서 향후 연구에서는 피하지방에서 이루어지는 대사조절과 다양한 내분비 기능을 더욱 면밀히 살펴봐야 할 것으로 사료된다. 본 연구의 결과를 종합해보면, 저지방식이와 운동 또는 저지방식이와 라스베라트롤의 병행은 식이조절의 단독 처치방법과 비교하여 비만으로 유도된 대사적 불균형을 개선하는데 효과적인 것으로 나타났다. 하지만 라스베라트롤 섭취와 운동을 병행한 그룹에서는 단독처치그룹들과 비교해 그 시너지 효과를 나타내지는 못하였다. 이는 결론적으로 식이조절과 운동의 병행만으로도 비만을 예방하고 개선하는데 충분한 효과를 지닌 것으로 판단된다.
결 론
본 연구는 고지방식이를 섭취한 비만동물을 이용하여 8주간의 저지방식이와 운동, 저지방식이와 라스베라트롤 섭취가 내장지방 그리고 피하지방에서 각각 대식세포 침윤과 염증 유전자들의 변화를 살펴보고자 시도되고 다음과 같은 결론을 얻었다.
본 연구 결과 고지방식이 그룹과 비교하여 저지방식이와 운동, 저지방식이와 라스베라트롤 병행처치는 체중과 지방조직 무게를 효과적으로 감소시켰다.
하지만, 고지방식이 그룹과 비교해 저지방식이와 운동, 저지방식이와 라스베라트롤 병행처치는 내장지방과 피하지방 모두에서 대식세포 침윤, M1 대식세포 분화를 효과적으로 억제하였다. M2로의 분화와, 염증관련 분자들의 변화는 내장지방에서 그리고 저지방식이와 운동을 병행한 그룹에서만 효과적인 것으로 나타냈다. 따라서 비만으로 야기되는 대사적 불균형을 예방하고 치료하기 위해서는 저지방식이와 운동의 병행처치가 유익한 치료도구로 보여진다.