AbstractPURPOSEThis study examined blood lactate concentration and removal rate after aerobic and anaerobic maximal exercise test in sedentary middle-age women.
METHODSTen sedentary middle-age women (aged 52.7±3.3 years) were performed after aerobic (Aero group) and anaerobic maximal exercise (Anaero group) test, VO2max test and Wingate test, by cross-over repeated design with biweekly. The blood was collected from cardinal veins at before and immediately after test for measurement of lactate and lactate dehydrogenase (LDH). And it was also collected from fingertip at before, immediately after and then recovery 5, 10, 15, 30 minutes after each maximal test. Lactate removal rate (%) were calculated by bellow formulas: ={1-[(Lactate at 30 minutes. after test-Resting lactate)/Increased lactate]}×100.
RESULTSThe blood lactate concentration from fingertip after both maximal test significantly increased immediately after test (p<.001 respectively), and maintained until recovery of 30 minutes. after test (p<.01, p<.001 respectively) in spite of there were no significant differences between both Aero and Anaero group. There were also no significant differences between both test groups in blood maximum lactate (p=.090) and increased lactate concentration (p=.058). No significant differences were also observed between the two groups in lactate removal rate (p>.05). There are positive correlationship among muscle mass and blood maximum lactate and increased lactate concentration (p<.01).
서 론지금까지 젖산(lactate)은 무산소성 운동 중에 생성되어 근육 수축을 방해하는 피로 물질로 알려져 있다[1]. 국내에서도 Kim et al. [2]의 연구를 통하여 젖산은 운동 피로를 발생시키는 가장 중요한 물질로 보고되면서 많은 연구자들이 피로물질로 오해하고 있는 경우가 많다. 이로 인해 최근까지도 혈중 젖산을 보다 빨리 제거하면 피로회복이 빨리 된다는 생각을 앞세워, 젖산 제거를 보다 빠르게 진행하기 위한 운동강도[3] 또는 마사지 방법[4] 등에 대한 연구가 진행되고 있는 실정이다.
그러나 lactate shuttle theory를 발표한 Brooks et al. [5]의 연구 이래로 젖산은 피로물질이 아니라는 연구들이 다수 보고되면서 기존의 학설이 수정되고 있다. 즉, 젖산은 피로물질이 아니라 세포 내의 산증(acidosis)으로부터 근 섬유를 보호하는 보호물질[6]로, 포도당이 분해되는 과정의 일시적인 상태[7,8]이며, 더 빨리 에너지를 공급할 수 있는 에너지원이라고 보고되고 있다[9]. 더 나아가서 운동에 의한 적응을 조절하는 신호 분자로 정의[10]되고 있으며, 운동 후의 젖산의 섭취가 글리코겐의 농도와 젖산 수송체(monocarboxylate transporters, MCT)를 증가시켜 운동능력을 향상시킨다[11]고까지 보고되고 있다. 따라서 젖산에 대하여 지금까지 알려져 있던 피로물질이라는 인식에서 벗어나 운동 시 운동능력을 향상시킬 수 있는 유용한 물질로서의 접근이 필요하다고 생각된다.
한편, 젖산은 신진 대사 및 운동 중 해당과정에서 생성된 피루브산(pyruvate)이 젖산탈수소효소(lactate dehydrogenase, LDH)의 작용을 통하여 생성된다. 일반적으로 근육에서의 젖산 생성속도가 젖산 제거속도를 초과할 때 농도가 증가하며, 젖산 감소속도는 MCT [12], LDH의 농도[13] 및 조직의 산화 능력[14] 등 많은 요인에 의해 좌우된다. 안정 시 혈중 젖산 농도는 0.5-2 mmol/L 이지만, 격렬한 운동시에는 20 mmol/L 이상으로 상승한다[15]. 안정 시에는 무산소성 에너지 대사는 잘 일어나지 않아 근육에서는 젖산 생성이 안될 것이라 생각되기 쉽지만, 미토콘드리아가 없는 적혈구의 대사와 높은 해당 능력을 갖는 근섬유의 효소 활성에 의해서 젖산이 생성되기 때문에 안정 시에도 혈중에 소량이 생성되고 있다[16]. 또한 강한 무산소성 운동이나 스프린트파워 운동과 같이 짧은 시간에 많은 에너지가 필요할 경우에는 근육에서의 해당과정을 통한 젖산 생성이 증가되고[17], 혈중으로 배출되어 혈중 농도가 급격하게 상승하며[18], 운동 시 혈중 젖산 수치의 증가는 운동강도와 비례하는 것으로 알려져 있다[19]. 또한 유산소성 운동 능력 지표로 젖산역치가 이용되어 왔으며[20,21], 운동 시 또는 회복 시의 혈중 젖산제거 능력은 운동수행능력과 정의 상관관계를 나타낸다고 보고되고 있다[22].
이처럼 혈중 젖산 대사 특성을 이용하여 운동수행능력을 평가하는 방법으로 이용되고 있으며, 트레드밀을 이용한 유산소성 최대운동 부하[23]부터 30초-2분 등의 단시간 고강도의 무산소성 최대운동 부하[4]까지 다양한 운동부하 방법이 적용되고 있다. 그러나 이러한 운동부하 방법 및 운동 시간에 따라서 혈중 젖산 반응은 다르게 나타날 가능성이 있으나 이를 직접 검토한 연구는 미흡한 실정이다. 따라서 본 연구에서는 정기적인 운동 경험이 없는 좌업중년여성을 대상으로 하여 동일 피험자에 의한 반복측정을 실시하였다. 즉, 최대산소섭취량(VO2max) 테스트에 의한 유산소성 최대운동 부하와 Wingate 테스트에 의한 무산소성 최대운동 부하를 실시하고, 운동에 의해 생성된 혈중 젖산생성량 및 젖산제거율을 비교 검토하여 유산소성 최대운동과 무산소성 최대운동에 따른 혈중 젖산 대사에 있어서의 차이를 밝히는 것을 목적으로 하였다.
연구 방법1. 연구대상자 및 실험절차연구대상자는 자율적으로 실험에 참여를 희망하는 좌업 중년여성 중, 48-59세(평균 연령 52.7±3.3세) 10명을 무작위로 선정하였다. 본 실험은 cross-over repeated design에 의하여, 유산소성 최대운동으로 점증부하에 의한 최대산소섭취량(VO2max) 테스트와 무산소성 최대운동으로 Wingate 테스트를 1주일 기간을 두고 총 2회 실시하였다. 실험 시작에 앞서 대상자에게 D대학교의 실험에 대한 규정에 따라, 실험내용 및 피해점, 실험중지의 자유 등에 대하여 자세히 설명한 후 동의를 얻었다. 1차 실험 당일 대상자들은 실험실에 도착하여 신장, 체중 및 신체조성(InBody 620, Biospace, Korea) 등의 신체적 특성을 측정한 후, 5명씩 무작위로 나누어 VO2max 테스트와 무산소성 최대운동으로 Wingate 테스트를 실시하였다. 1주일 후에 1차 시 측정하지 않았던 테스트를 동일한 방법에 의하여 진행하였다. 연구기간 동안 식사와 신체활동을 평소 생활을 유지하도록 하며, 활발한 운동이나 신체활동은 금지하였다. 대상자들의 신체적 특징 및 각 테스트 결과는 Table 1과 같다.
2. 채혈 및 혈액분석대상자들은 8시간 이상의 공복상태에서 실험실에 도착한 후 30분간 안정을 취하고 나서 상완 정맥에서 안정 시(resting) 혈액을 채혈하였다(5 mL). 그 후 각각의 최대운동 테스트를 수행하고 테스트 종료 직후(maximum) 다시 채혈하였다. 정맥에서 채취한 혈액은 전문혈액분석회사에 의뢰하여 젖산 및 젖산탈수소효소(lactate dehydrogenase, LDH)의 농도를 분석하였다. 한편 테스트 종료 후 회복 시의 혈중 젖산(lactate) 변화를 관찰하기 위하여, 정맥혈(vein)과 동일한 안정 시(pre)에 손가락 끝(fingertip)에서 채혈침에 의하여 채혈하였으며, 종료 직후(0 minutes), 5분(5 minutes), 10분(10 minutes), 15분(15 minutes), 30분(30 minutes) 후에 동일한 방법으로 채혈하였다. Fingertip 샘플은 0.1 mL 모세관에 옮겨 젖산 전용 측정기(YSI1500, Instruments, USA)로 젖산을 측정하였다. 젖산증가량 및 젖산 회복률은 다음 식을 이용하여 계산하였다. 젖산증가량(mmol/L) =최대젖산 농도–안정 시 젖산 농도; 젖산제거율(%) ={1-[(회복 30 minute 젖산 농도-안정 시 젖산 농도)/젖산증가량]}×100.
3. VO2max 테스트최대 유산소성 운동을 부하하고, 유산소성 관련 지표를 측정하기 위하여 점증부하에 의한 VO2max 테스트를 실시하였다. 점증부하 방법은 운동 경험이 없는 중년 여성인 점을 감안하여 한국스포츠개발원에서 개발한 KISS 프로토콜을 토대로 변경하여 실시하였다. 프로토콜은 0:00-1:00까지 경사도 0%, 3.0 km/hr로 시작하여, -3:00까지 경사도 2%, 4.8 km/hr로 하였으며 그 이후부터는 2분 간격으로 경사도는 2%, 속도는 1.2 km/hr를 증가시켜 측정하였다. VO2max의 결정은 대상자 스스로가 더 이상 운동을 지속하지 못하거나, 운동 강도가 증가하더라도 심박수 또는 산소섭취량이 유의하게 증가하지 않을 때, 호흡교환률 1.10 이상, 운동자각도(RPE) 17 이상 중 2가지 이상이 충족된 경우로 하였다[24]. 트레드밀(Technogym run race 10, Technogym, Italy)과 호흡가스분석기(Cosmed, Quark b2, USA)를 사용하였다.
4. Wingate 테스트Wingate 테스트는 전용 측정기(Excaliber Sport, Sweden)를 이용하여 2분 이상 사전 운동 후 30초간 최대 운동부하를 실시하였다[25]. 페달의 상대적 부하는 피험자 체중의 약 0.05% (kp)로 하였다. 측정 시에는 대상자들이 자의적으로 최대 무산소성 능력을 발휘하도록 격려하였으며, 측정 결과로부터 fatigue index 및 total work, peak power, mean power를 환산하였다.
5. 자료분석 및 통계방법모든 자료는 SPSS 22.0 통계 프로그램을 이용하여 요인별 평균과 표준편차, 표준오차를 산출하였다. 두 가지 최대 운동부하 후 30분간의 회복 시의 변화를 비교하기 위하여 이원변량반복측정분산분석(2-way repeated measure ANOVA)을 실시하여 2가지 최대 운동 방법(VO2max 테스트와 Wingate 테스트)에 따른 시기간(6시기: 운동 전, 운동직후 및 회복 0, 5, 10, 15, 30분 후)의 차이(2 by 6)를 분석하였다. ANOVA 검사 후 주 효과에 유의한 차이가 있을 경우 시기 간의 사후 검증은 일원변량분산분석(one way ANOVA)를 이용하였다. 기타 변인의 집단 간에 차이의 검토는 paired t-test를 실시하였다. 통계적 유의 수준은 p<.05로 설정하였다.
연구 결과1. 최대 운동부하 전후의 혈청 젖산 변화
Table 2에는 두 집단 간의 최대 운동부하 전후의 손가락 끝(fingertip) 혈액의 평균 젖산 변화를 각 측정 시기별로 나타냈다. 이원변량반복측정분산분석 결과 시기 간에 유의한 차이가 나타났다(p <.001). 사후 검증 결과 유산소성 최대 운동부하 집단(Aero)에서는 운동 전(pre)과 비교하여 운동 직후(0 minute)에 최대치를 나타냈으며(p<.01), 회복 10분 이후에 최대치에 비교하여 유의하게 감소하였다(p<.001). 무산소성 최대 운동부하 집단(Anaero)에서는 운동 전(pre)과 비교하여 운동직후에 증가하였으나(p <.001), 회복 5분 후에 운동 직후보다 더 증가(p<.05)하여 최대치를 나타냈다(p <.01). 회복 15분 이후에는 최대치에 비교하여 유의하게 감소하였다(p <.01). Fig. 1에는 두 집단의 운동 전(pre)을 기준으로 한 상대적 변화율을 나타냈다. Aero 집단의 최대치는 0 minute에 나타나 안정 시(mean±SD)의 6.50±2.79배까지 증가하였으며, Anaero 집단의 최대치는 5 minutes에 나타나 안정 시의 5.98±2.44배까지 증가하였다.
2. 최대 운동부하 전후의 정맥과 fingertip 혈액에서의 젖산 변화
Table 3에는 두 집단 간의 최대 운동부하 전후의 정맥과 fingertip 혈액에서의 젖산 변화를 나타냈다. 최대젖산 농도(Maximum lactate)는 Aero 집단에서는 대부분 0 minute에 나타났으나, 2명은 5 minutes에 나타났다. Anaero 집단의 최대젖산 농도는 각각 2명은 0 minute에, 4명은 5 minutes에, 4명은 10 minutes에 나타났다. 정맥에서의 안정 시 젖산 농도는 Anaero 집단이 높았으나(p <.05), 최대젖산 농도에서는 두 집단 간의 유의한 차이는 나타나지 않았다. 정맥의 젖산 증가량에서는 Aero 집단이 Anaero 집단에 비교하여 약 1.3배 높은 경향을 나타냈으나 통계적 유의차는 나타나지 않았다(p =.058). 한편, fingertip에서의 안정 시 및 최대치, 증가량, 회복 30 minutes의 젖산 농도, 젖산제거율은 두 집단 간의 유의한 차이는 나타나지 않았다. 젖산탈수소효소(LDH)에 있어서도 두 집단 간의 유의한 차이는 나타나지 않았으며, 두 집단 내의 안정 시와 최대치의 비교에 있어서도 유의한 차이는 나타나지 않았다.
3. 정맥과 fingertip 혈액 간의 젖산 농도 비교
Table 4에는 정맥과 fingertip 혈액 간의 젖산 농도 비교를 나타냈다. 정맥과 fingertip 혈액의 젖산 농도를 비교하기 위하여 Aero 집단과 Anaero 집단을 더하여 산출하였다(n=20). 안정 시에는 두 집단 간의 유의한 차이는 나타나지 않았으나, 최대젖산 농도에서는 정맥이 fingertip에 비교하여 약 1.14배 유의하게 높았다(p<.01).
4. 젖산 관련 지표와 신체조성, 유산소성 지표, 무산소성 지표와의 상관관계
Table 5에는 정맥과 fingertip 혈액에 있어서의 젖산 관련 지표와 신체조성, 유산소성 지표, 무산소성 지표와의 상관관계를 나타냈다. 신체조성과의 관계에 있어서는 체중은 젖산제거율과 정적 상관관계를 나타냈으며(p <.05), 총근육량 및 골격근량, 제지방량은 fingertip의 최대 젖산 농도와 정적 상관관계(p <.05)를, 골격근량과 fingertip의 젖산 증가량과 정적 상관관계를 나타냈다(p <.05). 유산소성 지표와의 관계에 있어서는 VO2max와 HRmax, Running time, METs는 정맥의 최대 젖산 농도 및 젖산 증가량과 정적 상관관계를 나타냈다(p<.05, p<.01). 또한, HRmax와 Running time은 fingertip의 최대 젖산 농도 및 젖산 증가량과 정적 상관관계를 나타냈다(p<.05, p <.01). 무산소성 지표와의 관계에 있어서는 Mean power/BW은 정맥의 최대 젖산 농도 및 젖산 증가량과 정적 상관관계를 나타냈다(p <.05). 또한, Mean power/BW은 fingertip의 젖산 증가량과 정적 상관관계를 나타냈다(p<.05).
논 의본 연구에서는 유산소성 최대운동 후와 무산소성 최대운동 후에 생성된 혈중 젖산생성량 및 젖산제거율을 비교 검토하였다. 그 결과 유산소성(Aero) 최대 운동 후의 정맥 혈중 젖산 농도는 6.88 ±1.96 mmol/L로 무산소성(Anaero) 최대 운동 후의 5.73±1.24 mmol/L와 통계적인 유의한 차이는 없는 것으로 나타났다. 6-7분 지속되는 VO2max 테스트와 30초로 끝나는 Wingate 테스트에 의한 젖산생성량에는 큰 차이가 없는 것으로 나타났다. VO2max 테스트 시, 운동강도가 낮을 때에는 유산소성 대사에 의해 에너지 생산이 진행되므로 젖산의 생성은 거의 일어나지 않지만 운동 강도가 높아지면서 에너지 수요가 증가하게 되고 이에 따라 포도당 분해가 증가하면서 혈중 젖산 농도도 증가한다. 일반적으로 무산소성 경로를 통한 근육의 ATP 공급능력은 동적 운동의 마지막 약 3분 동안에 최대로 나타나며, 건조 근육 중량(dm)당 약 370 mmol/kg을 생산하는 것으로 알려져 있다. 또한 무산소성 해당과정을 통하여 약 80%, 포스포크레아틴(PC) 분해를 통하여 약 16%, 저장 ATP를 통하여 약 4% 공급되는 것으로 알려져 있다[26]. VO2max 테스트의 초·중반에는 운동강도가 그다지 높지 않지만 운동 후반부에 급격히 증가하게 되고 피험자는 더 이상 그 운동부하를 유지하지 못하는 운동피로가 유발된다. 이러한 테스트의 특성이 반영되기 때문에 VO2max 테스트와 Wingate 테스트 사이의 젖산 생성량에는 큰 차이가 없었던 것으로 판단된다.
또한, 최대혈중 젖산 농도는 운동 강도는 물론이고 대상자나 운동방법에 따라 다르게 나타나며 최대 25 mmol/L까지 증가하는 것으로 알려져 있다[15]. Smith et al. [27]의 연구에서는 평균연령 22.5세의 건강한 남성을 대상으로 점증부하 자전거 에르고미터 최대 운동 후의 혈중 젖산 농도가 약 9 mmol/L이었다고 보고되고 있으며, 우리나라 마라톤 선수의 경우 본 연구와 유사한 VO2max 테스트를 실시한 결과 12.7±2.7 mmol/L까지 증가하는 것이 보고되고 있다[23]. 본 연구에서 최대 약 6.9 mmol/L이었던 점을 감안하면 일반 젊은 남성의 약 77%, 남자 마라톤 선수의 약 50%의 젖산밖에 생성하지 못하는 것으로 나타났다.
한편, Simon et al. [28]은 운동 능력이 좋을수록 젖산 확산율이 높아 운동 종료 후 혈중 젖산 농도가 빠르게 증가한다고 보고하고 있고, 이러한 혈중 젖산의 빠른 증가는 트레이닝으로 인한 모세혈관의 밀도 증가에 따라서 교환 면적이 증가하기 때문이라고 알려져 있으며, 이러한 모세혈관의 밀도 증가는 젖산 생성 위치로부터 혈관으로의 확산거리를 단축시켜 젖산 교환 능력이 향상되기 때문으로 알려져 있다[29]. 즉 트레이닝에 의해 체력이 좋아질수록 혈중으로의 젖산이 빠르게 증가하는 것을 의미한다. 본 연구에서의 피험자들의 VO2max는 약 34.3±4.1 mL/kg/min 정도로, 위의 Smith et al. [27]의 연구의 피험자들 42.8±2.0 mL/kg/min, 마라톤 선수 약 70.9±1.0 mL/kg/min 이었던 점을 고려해 보면, 각각 80.1%와 48.4%의 체력수준에 불과하고, 젖산 생성비율과 유사한 비율이라는 것을 알 수 있다. 즉, 심폐체력 수준에 따라 젖산 생성량이 달라질 가능성이 있으며 추가 연구를 통하여 검토할 사항이라 생각된다.
또한, 두 집단의 최대 운동 후의 혈중 젖산 농도를 살펴보면, 두 집단 사이의 통계적인 유의차는 없었지만 Aero가 Anaero에 비교하여 약 1, 2배 높은 경향을 나타내고 있으며(p =.090), 젖산 증가량 또한 약 1.3배 높은 경향을 나타내고 있다(p =.058). 통계적으로 유의차는 없으나 대상자 수에 의해 영향을 받으므로 0.1 이하의 유의 수준은 주의 깊게 검토할 필요가 있다고 판단된다. 즉, Aero와 Anaero의 최대 운동 시 모든 대상자들은 자신의 최대 노력으로 운동을 수행하였기 때문에, 두 집단의 최대 젖산 농도의 차이는 무산소성으로 실시한 운동 시간, 즉 최대로 노력한 시간에 의한 차이라고 판단된다. 본 연구에서 Aero의 경우 운동 시간은 평균 419.0±48.6초이었으며, Anaero는 30초이었다. Aero의 경우 운동 시작 60초 이후부터는 120초 간격으로 부하강도를 높였으므로 평균적으로 4번째 스테이지 이후부터 최대 운동을 수행하였을 것이다. 최대로 노력한 시간을 정확하게 알 수는 없지만, 평균 약 7분 정도의 운동 시간을 고려할 때 적어도 1분 이상은 최선의 노력으로 고강도의 운동을 수행하고 있는 것으로 판단되었다. 반면 Anaero는 테스트 초반에 가장 높은 파워가 도출되는 특성을 반영하여 테스트를 시작하여 10-15초 내외까지 최대 운동을 수행하고 나머지 시간까지 그것을 유지하는 운동을 수행하였을 것이라고 판단된다. 이러한 운동 특성은 fingertip 젖산 농도에 반영되어, Aero에서는 운동 직후(0 minute)에 최대치를 나타내는 것에 반하여 Anaero에서는 회복 5분 후에 최대치를 나타내는 것으로 판단된다. 즉, Aero에서는 운동 시간이 긴 만큼 운동에 따른 근육에서의 젖산 생성이 혈액에 그대로 반영되어, 운동 종료 직후 나타나는 것에 반하여, Anaero에서는 운동 시간이 짧은 만큼 근육에서 생성된 젖산이 혈액에 반영되기까지 시간적으로 지연되는 것을 의미하는 것이라 판단된다. Withers et al. [30]의 연구에서도 30-90초 정도의 단시간 고강도 ‘all out’ 운동 시의 혈중 최대 젖산 수치는 운동 종료 후 몇 분 정도 뒤에 나타난다고 보고하고 있으며, Goodwin et al. [15]도 30초에서 120초 정도 지속하는 ‘all out’ 최대 운동 시에는 혈중 최대 젖산 수치가 운동 종료 후 3분에서 8분 사이에 나타난다고 보고하고 있다.
한편, 지금까지 운동 후의 젖산 생성은 운동강도에 비례한다고 알려져 있다. Kelleher et al. [31]의 연구에서도 전통적인 근력 트레이닝(TRAD)과 여러 세트를 번갈아 가며 고강도로 작용-길항 근육의 근력 트레이닝을 수행하는 상호적 슈퍼세트(SUPERs)를 부하한 후 검토한 결과, SUPERs 집단의 운동 후 초과산소섭취량(excess postexercise oxygen consumption, EPOC) 증가와 함께 혈중 젖산도 TRAD 집단(3.8±0.6 mmol/L)에 비교하여 SUPER 집단(5.1±0.9 mmol/L)에서 유의하게 증가하게 증가하는 것을 보고하고 있다. 최근의 Jones et al. [32]과 Park et al. [33]의 연구에서도 근력 트레이닝 집단(ST)과 근력 트레이닝 후에 지구력 트레이닝(ST-END), 지구력 트레이닝 후에 근력 트레이닝 집단(END-ST), 트레이닝 없는 대조 집단(CON)으로 나누어 검토한 결과, 운동 후 1시간 뒤의 END-ST와 ST의 혈중 젖산 농도는 ST-END에 비교하여 유의하게 높은 것으로 나타나 마지막에 수행한 운동강도가 젖산 농도에 영향을 미치는 것을 제안하고 있다. 그러나 Thornton et al. [34]의 연구에서는 저항성 운동강도를 저강도와 고강도로 나누고 운동량을 일정하게 하여 운동 후의 혈중 젖산 농도를 검토한 결과, 두 집단간의 유의한 차이가 없음을 밝히면서, 혈중 젖산의 생성은 운동강도보다는 운동량(work volume)에 비례한다는 것을 보고하고 있다. 본 연구에서도 단순히 운동 강도로만 비교할 때에는 Anaero가 Aero에 비교하여 운동강도는 더 높았다. 그러나 혈중 젖산 농도는 운동 강도가 낮았던 Aero 후에 더 높은 경향을 나타냈으며, 젖산 농도는 어느 수준을 넘는 운동강도에서는 최대로 발휘한 운동시간과 같이 운동량에 영향을 받을 가능성이 시사하는 것이라 생각된다.
혈중 젖산 농도는 fingertip에 비교하여 정맥에서 더 높게 나타날 가능성이 시사되었다(Table 4). 젖산의 생성은 사용되는 근육의 세포질에서 생성되어 혈류를 타고 혈중으로 배출된다. 정맥혈은 다양한 조직으로부터 생성된 물질들이 포함되기 때문에 채혈 부위에 따라서 혈중 젖산농도는 달라질 수 있고, 가능한 동맥혈에서 젖산 농도를 측정하는 것이 바람직하다[35]. 그러나 동맥혈의 경우, 운동 시에 빠르게 채혈하는 것이 힘들기 때문에 보통 정맥혈이나 fingertip에서 채혈하고 있다. 그러나 Foxdal et al. [36]은 10명의 남성을 20-25분간 최대하 운동 수행전후의 혈장 및 정맥혈, fingertip 혈액에서 각각 젖산 농도를 비교한 결과, 각각 유의한 차이가 있기 때문에 직접 비교해서는 안 된다고 보고하였다. 또한 혈중 젖산 농도가 4.0 mmol/L이 되는 운동강도를 비교한 다른 연구[37]에서는 유의하게 혈장<fingertip <정맥혈 혈액 순으로 나타나는 것을 보고하고 있다. 즉, 운동강도가 같다고 가정할 때 정맥혈에 비교하여 fingertip의 젖산농도가 더 높다는 것을 의미하는 것으로, 본 연구 결과와 같이 최대 강도의 운동 후의 젖산 농도는 정맥혈이 fingertip 혈액보다 더 높게 나타날 수 있다는 것을 의미한다. 따라서, 운동 후의 젖산 농도의 비교는 채혈 부위별로 나누어 검토해야 할 것이라 판단되었다.
혈중 젖산탈수소효소(LDH)은 운동 종료 후 Aero와 Anaero는 각각 약 5.0%와 11.4% 정도 증가하는 경향을 보였으나 유의한 차이는 나타나지 않았다(Table 3). 젖산 농도는 두 집단 모두 운동 전에 비교하여 운동 후에 6.1-10.6배 증가한 것에 비교해서는 LDH의 변화는 미비한편이라 할 수 있다. LDH는 근조직 내에서 피루브산을 젖산으로 변화시킬 때 작용하는 효소로서 젖산증가와 동반하여 LDH도 증가할 것이라 생각했지만 유의한 변화는 나타나지 않았다. 한편, LDH는 일반 혈액 검사에서는 근손상 지표로 사용된다. Koch et al. [38]은 저항 운동과 혈중 근손상 지표와 관련한 리뷰 논문에서 저항성 운동이 근육조직에 있어 세포 골격 및 수축 미세 섬유, 기저 판 등에서 국소적인 손상을 초래하며, 이때 젖산탈수소효소 및 크레아틴키나제(CK), 미오글로빈 등이 혈액으로 방출된다고 제안하고 있다. 또한 Neto et al. [39]은 남성 군인을 대상으로 저강도의 저항운동과 혈류 제한 조건에 따른 근손상과 산화적 스트레스를 검토한 연구에서도 LDH의 증가를 근손상 지표로 사용하고 있다. 추후 운동 방법이나 인원 수 등을 조정하여 추가적으로 검토할 필요가 있을 것이라 생각된다.
한편, 두 집단의 회복 30 minutes의 젖산농도에서는 유의한 차이는 나타나지 않았다. 젖산제거율에 있어서도 Aero와 Anaero는 각각 약 63%와 약 56%까지 회복되는 것으로 나타났으나 두 집단 간의 유의한 차이는 나타나지 않았다. 이로써 평소에 운동을 수행하지 않은 중년 여성이라 할지라도 최대 운동 후 약 30분 정도 안정을 취하면 약 60%까지 젖산이 제거되는 것으로 나타났다. 서론에서도 언급한 바와 같이 지금까지 젖산 회복에 대한 연구는 운동에 의하여 빨리 젖산을 제거하는 것이 피로회복에 효과적이라고 보고하고 있다[3,4]. Neric et al. [40]의 단시간 최대 운동 후 생성된 젖산제거에 미치는 운동 효과를 검토한 연구에서도 운동 종료 후 20분에 수동적인 안정 상태는 약 4.1 mmol/L이었지만, 최대하 수영 회복은 약 1.6 mmol/L까지 감소하여 능동적으로 운동을 수행하는 것이 젖산 제거에 효과적이라고 보고하고 있다. 즉, 운동 후 혈중 젖산이 높은 상태에서 회복처치로써 유산소 운동을 수행하면 젖산의 간에서의 포도당 신생(일부분)과 피루브산으로의 전환을 통한 크렙스 사이클의 에너지원으로 이용(대부분) 모두가 높아지기 때문이다[9]. 일반적으로 젖산 제거 능력은 지구성 운동수행능력이나 상대적으로 더 고강도로 운동을 지속할 수 있는 능력과 관련이 있다[41]. 같은 조건에서 젖산제거 능력이 좋다고 한다면, 운동 막바지의 고강도 운동 시의 근육 내의 젖산 축적을 줄일 수 있고, 더 높은 강도에서의 내성이 증가하는 것이므로 운동수행력의 예측 인자로 활용할 수 있을 것이다. 이를 평가하기 위한 전제 조건은 회복 시의 운동 강도는 일정해야 한다. 본 연구에서는 회복기에 운동을 수행하지 않고 안정 상태에서 제거율을 비교하였다. 동일인에 의한 실험이었던 만큼 거의 비슷한 회복률을 보였다고 판단된다.
한편, 체중과 젖산제거율은 정적 상관관계가 있는 것으로 나타나, 체중이 많을 수록 젖산제거가 빠를 가능성이 있는 것으로 나타났다. 그러나 근육량 및 골격근량과 젖산제거율 간 관련성이 없는 것으로 나타나, 이에 대해서는 추가적인 검토가 필요할 것으로 판단된다. 총근육량 및 골격근량, 제지방량은 fingertip의 최대 젖산 농도와, 골격근량은 fingertip의 젖산 증가량과 정적 관련성이 있는 것으로 나타나 근육량이 많을수록 젖산 축적량이 많을 것으로 생각되었다. Beneke et al. [42]의 연구에 의하면 Wingate 테스트 후의 젖산농도는 평균 연령 약 12세 소년, 약 16세 청소년, 약 27세 성인에서 각각 약 10.2, 12.7, 13,7 mmol/L를 나타낸다는 보고와 같이, 연령 증가와 함께 전신의 근육량이 증가하고 이에 따라서 최대 젖산치도 증가하는 것이라고 판단된다. 또한, VO2max와 HRmax, Running time, METs 등의 유산소성 지표는 정맥 또는 fingertip의 최대 젖산 농도 및 젖산 증가량과 정적 상관관계를 나타냈다. 즉 유산소 운동 중 막바지에는 무산소성 에너지 대사 비율이 증가하게되어 젖산생성량이 증가하고, 축적되는 젖산에 대한 내성이 높을수록 유산소성 운동수행력도 높다는 것을 반증하는 것이라고 생각된다. McLellan & Jacobs [43]의 운동강도와 근육 글리코겐 이용률을 외측광근(m. vastus lateralis)의 생검으로 검토한 연구에 의하면 근육 글리코겐 이용은 %VO2max와 %OBLA와 높은 정상관이 있는 것으로 알려져 있다. 이는 유산소성 운동수행력이 높을수록 글리코겐 이용율이 높고, 근육 중의 젖산 농도도 높을 가능성을 시사하는 것이다. 무산소성 지표인 Mean power/BW은 정맥 또는 fingertip의 최대 젖산 농도 및 젖산 증가량과 정상관을 나타내, 평균 파워의 경우도 젖산 내성과 관련성이 높다는 것을 의미하는 것이라고 판단되었다.
결 론정기적인 운동 경험이 없는 좌업 중년여성을 대상으로 VO2max 테스트와 Wingate 테스트에 의한 유산소성 최대운동과 무산소성 최대 운동 후의 혈중 젖산생성량 및 젖산 제거율을 비교 검토하였다. 그 결과 젖산생성량에는 유의한 차이가 없었고, 회복 30 minutes의 젖산제거율에 있어서도 두 집단 간의 유의한 차이는 없는 것으로 나타났다. 또한, 근육량 및 골격근량 등은 최대 젖산 농도 또는 젖산 증가량과 정적 관련성이 있는 것으로 나타나, 근육량이 많을수록 젖산생성량이 증가하고 이로 인해 젖산 내성이 증가할 가능성이 시사되었다.
Fig. 1.Fig. 1.The comparison of change rate of fingertip lactate concentration at recovery period between aerobic and anaerobic maximal test. Values are mean±SE. An aerobic maximal test was performed by VO2max test and anaerobic maximal test was performed by Wingate test. aaap<.001, aap<.01 vs. pre VO2max test; bbbp<.001, bbp<.01 vs. pre Wingate test; cccp<.001 vs. 0 minute after VO2max test; dp<.05 vs. 0 minute after Wingate test, eeep<.001, eep<.01 vs. 5 minutes after Wingate test. 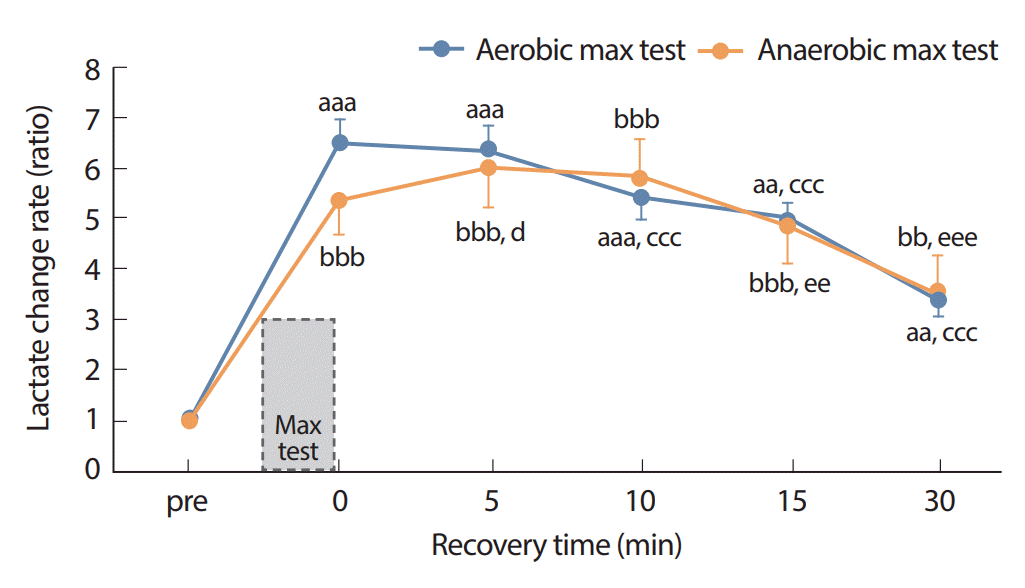
Table 1.The characteristics of the subjects Table 2.The comparison of fingertip lactate concentration after each maximal test between aerobic and anaerobic group
Table 3.The comparisons of vein and fingertip lactate index between aerobic and anaerobic group Values are mean±SD. Aero, aerobic maximal test group; Anaero, anaerobic maximal test group; LDH, Lactate dehydrogenase. Increased lactate volume and lactate removal rate (%) were calculated by bellow formulas: Increased lactate volume (mmol/L)=Maximum lactate - Resting lactate Lactate removal rate (%)={1-[(Lactate at 30 minutes after test-Resting lactate)/Increased lactate]}×100. Table 4.The comparison of lactate index in draw point between vein and fingertip (n=20)
Table 5.The relationship among lactate index from both vein and fingertip, body composition, aerobic and anaerobic capacity index
Max. lactate, maximal lactate concentration; Inc. lactate, increased lactate concentration; BW, Body weight; TMM, total muscle mass; SMM, skeletal muscle mass; FFM, fat free mass; TFM, total fat mass; %FM, % fat mass; BMI, body mass index; VO2max, maximal oxygen consumption; HRmax, maximum heart rate; VE, minute ventilation; METs, metabolic equivalents. REFERENCES1. Karlsson J, Saltin B. Lactate, ATP, and CP in working muscles during exhaustive exercise in man. Journal of Applied Physiology. 1970;29(5):596-602.
2. Kim SS, Lee GY, Kim YP, Lee SJ, Byun JJ, et al. Effect of long term dance training on the maximal oxygen uptake (VO2max) and blood lactate concentration in dance major. The Korean Journal of Sports Medicine. 1997;15(2):262-273.
3. Park EJ, Koo HJ, Lee JK. Setting of proper recovery exercise intensity to recover from lactate fatigue. Journal of Korean Association of Physical Education and Sport for Girls and Women. 2004;18(1):67-75.
4. Shin W, Lee KS. The effect of foot massage on blood lactate concentration after exercise. Journal of Sport and Leisure Studies. 2009;37(2):1231-1239.
5. Brooks GA. The lactate shuttle during exercise and recovery. Medicine and Science in Sports and Exercise. 1986;18(3):360-368.
6. Messonnier L, Kristensen M, Juel C, Denis C. Importance of pH regulation and lactate/H+ transport capacity for work production during supramaximal exercise in humans. Journal of Applied Physiology. 2007;102(5):1936-1944.
7. Eto D, Hada T, Kusano K, Kai M, Kusunose R. Effect of three kinds of severe repeated exercises on blood lactate concentrations in thoroughbred horses on a treadmill. Journal of Equine Science. 2004;15(3):61-65.
8. Kitaoka Y, Endo Y, Mukai K, Aida H, Hiraga A, et al. Muscle glycogen breakdown and lactate metabolism during intensive exercise in Thoroughbred horses. The Journal of Physical Fitness and Sports Medicine. 2014;3(4):451-456.
9. Stevenson RW, Mitchell DR, Hendrick GK, Rainey R, Cherrington AD, et al. Lactate as substrate for glycogen resynthesis after exercise. Journal of Applied Physiology. 1987;62(6):2237-2240.
10. Nalbandian M, Takeda M. Lactate as a signaling molecule that regulates exercise-induced adaptations. Biology (Basel). 2016;5(4):1-12 doi:10.3390/biology5040038.
11. Hoshino D, Hanawa T, Takahashi Y, Masuda H, Hatta H. Chronic post-exercise lactate administration with endurance training increases glycogen concentration and monocarboxylate transporter 1 protein in mouse white muscle. Journal of Nutritional Science and Vitaminology. 2014;60(6):413-419.
12. Cupeiro R, Pérez-Prieto R, Amigo T, Gortázar P, Redondo C, et al. Role of the monocarboxylate transporter MCT1 in the uptake of lactate during active recovery. European Journal of Applied Physiology. 2016;116(5):1005-1010.
13. Bird SR, Linden M, Hawley JA. Acute changes to biomarkers as a consequence of prolonged strenuous running. Annals of Clinical Biochemistry. 2014;51(Pt 2):137-150 doi:10.1177/0004563213492147.
14. Ceci R, Duranti G, Sgrò P, Sansone M, Guidetti L, et al. Effects of tadalafil administration on plasma markers of exercise-induced muscle damage, IL6 and antioxidant status capacity. European Journal of Applied Physiology. 2015;115(3):531-539 doi:10.1007/s00421-014-3040-5.
15. Goodwin ML, Harris JE, Hernández A, Gladden LB. Blood lactate measurements and analysis during exercise: a guide for clinicians. Journal of Diabetes Science and Technology. 2007;1(4):558-569 doi:10.1177/193229680700100414.
16. McArdle MD, Katch FI, Katch VL. Exercise physiology: nutrition, energy, and human performance. Wolters Kluwer/Lippincott Williams & Wilkins Health. 2010; ISBN 978-0-683-05731-7.
17. Péronnet F, Aguilaniu B. Physiological significance and interpretation of plasma lactate concentration and pH in clinical exercise testing. Revue des Maladies Respiratoires. 2014;31(6):525-551.
18. Barstow TJ. Characterization of VO2 kinetics during heavy exercise. Medicine and Science in Sports and Exercise. 1994;26(11):1327-1334.
19. Lagally KM, Robertson RJ, Gallagher KI, Goss FL, Jakicic JM, et al. Perceived exertion, electromyography, and blood lactate during acute bouts of resistance exercise. Medicine and Science in Sports and Exercise. 2002;34(3):552-559.
20. Takeshima N, Kobayashi F, Watanabe T, Tanaka K, Tomita M, et al. Cardiorespiratory responses to cycling exercise in trained and untrained healthy elderly: with special reference to the lactate threshold. Applied Human Science. 1996;15(6):267-273.
21. Fernandes TL, Nunes Rdos S, Abad CC, Silva AC, Souza LS, et al. Postanalysis methods for lactate threshold depend on training intensity and aerobic capacity in runners. An experimental laboratory study. Sao Paulo Medical Journal. 2015;13;134(3):193-198 doi:10.1590/1516-3180.2014.8921512.
22. Messonnier L, Freund H, Féasson L, Prieur F, Castells J, et al. Blood lactate exchange and removal abilities after relative high-intensity exercise: effects of training in normoxia and hypoxia. European Journal of Applied Physiology. 2001;84(5):403-412.
23. Cho SY, Oh CS, Lee JH. The recovery rate of heart rate and blood lactate after maximal exercise test in korean and kenyan male elite marathon runners. The Korean Journal of Physical Education. 2012;51(1):273-281.
24. American College of Sports Medicine (ACSM). Guidelines for exercise testing and prescription. 9th Edition, Lippincott Williams & Wilkins: Baltimore, MD 2013;pp. 114-141).
25. Bar-Or O. The Wingate anaerobic test an update on methodology, reliability and validity. Sports Medicine. 1987;4(6):381-394.
26. Spriet LL. Anaerobic metabolism in human skeletal muscle during short-term, intense activity. Canadian Journal of Physiology and Pharmacology. 1992;70(1):157-165.
27. Smith EW, Skelton MS, Kremer DE, Pascoe DD, Gladden LB. Lactate distribution in the blood during progressive exercise. Medicine and Science in Sports and Exercise. 1997;29(5):654-660.
28. Simon J, Young J, Blood D, Segal K, Case R, et al. Plasma lactate and ventilation thresholds in trained and untrained cyclists. Journal of Applied Physiology. 1986;60(3):777-781.
29. Messonnier L, Freund H, Féasson L, Prieur F, Castells J, et al. Blood lactate exchange and removal abilities after relative high-intensity exercise: effects of training in normoxia and hypoxia. European Journal of Applied Physiology. 2001;84(5):403-412.
30. Withers RT, Sherman WM, Clark DG, Esselbach PC, Nolan SR, et al. Muscle metabolism during 30, 60 and 90 s of maximal cycling on airbraked ergometer. European Journal of Applied Physiology and Occupational Physiology. 1991;63(5):354-62.
31. Kelleher AR, Hackney KJ, Fairchild TJ, Keslacy S, Ploutz-Snyder LL. The metabolic costs of reciprocal supersets vs. traditional resistance exercise in young recreationally active adults. The Journal of Strength & Conditioning Research. 2010;24(4):1043-1051 doi:10.1519/JSC.0b013e3181d3e993.
32. Jones TW, Howatson G, Russell M, French DN. Effects of strength and endurance exercise order on endocrine responses to concurrent training. European Journal of Sport Science. 2017;17(3):326-334 doi:10.1080/17461391.2016.1236148.
33. Park JS, Park DH, Kim YJ. The effect of aerobic and resistance exercise sequence on RPE, EPOC and fat oxidation in college aged male. The Korean Journal of Exercise Nutrition. 2010;14(3):127-135.
34. Thornton MK, Rossi SJ, McMillan JL. Comparison of two different resistance training intensities on excess post-exercise oxygen consumption in African American women who are overweight. The Journal of Strength & Conditioning Research. 2011;25(2):489-496 doi:10.1519/JSC.0b013e3181bf0350.
35. Forster HV, Dempsey JA, Thomson J, Vidruk E, DoPico GA. Estimation of arterial PO2, PCO2, pH, and lactate from arterialized venous blood. Journal of Applied Physiology. 1972;32(1):134-137.
36. Foxdal P, Sjödin A, Ostman C, Ostman B, et al. Lactate concentration differences in plasma, whole blood, capillary finger blood and erythrocytes during submaximal graded exercise in humans. European Journal of Applied Physiology and Occupational Physiology. 1990;61(3-4):218-222.
37. Foxdal P, Sjödin A, Ostman B, Sjödin B. The effect of different blood sampling sites and analyses on the relationship between exercise intensity and 4.0 mmol.l-1 blood lactate concentration. European Journal of Applied Physiology and Occupational Physiology. 1991;63(1):52-54.
38. Koch AJ, Pereira R, Machado M. The creatine kinase response to resistance exercise. Journal of Musculoskeletal and Neuronal Interactions. 2014;14(1):68-77.
39. Neto GR, Novaes JS, Salerno VP, Gonçalves MM, Batista GR, et al. Does a resistance exercise session with continuous or intermittent blood flow restriction promote muscle damage and increase oxidative stress? Journal of Sports Sciences. 2017;31:1-7 doi:10.1080/02640414.2017.1283430.
40. Neric FB, Beam WC, Brown LE, Wiersma LD. Comparison of swim recovery and muscle stimulation on lactate removal after sprint swimming. The Journal of Strength & Conditioning Research. 2009;23(9):2560-2567 doi:10.1519/JSC.0b013e3181bc1b7a.
41. Messonnier L, Freund H, Bourdin M, Belli A, Lacour J. Lactate exchange and removal abilities in rowing performance. Medicine and Science in Sports and Exercise. 1997;29(3):396-401.
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||