서 론
인체의 혈관 조직은 해부학적 횡단면으로 관찰하였을 때, 가장 내부에 위치한 내피세포(endothelial cells)로 구성된 내막층(intimal layer)과 내피세포를 감싸고 있는 평활근 세포(smooth muscle cells)로 구성되어 있다. 평활근 세포는 위치에 따라 중막(media) 및 외막(adventitia)으로 구분된다[1]. 따라서 혈관 내피세포는 구조적으로 순환하는 혈액과 끊임없이 접촉하게 된다. 이 과정에서 혈관 내피세포는 혈류의 증감 및 속도변화로 야기되는 물리적 신호와 혈액과의 물질 교환을 통해 발생되는 화학적 신호들을 흡수한다. 이러한 신호는 평활근 세포층에 전달되어 혈관조직의 수축 및 이완 기능을 담당하게 된다[2]. 내피세포는 혈관 조직 내에서 다양한 역할을 하는 것으로 알려져 있는데, 해부학적으로 혈관 내벽을 구성할 뿐만 아니라, 생리학적으로는 투과성(vessel wall permeability maintenance), 혈관 운동(vasomotor control), 혈전 thrombosis regulation), 염증반응(inflammation reaction)을 종합적으로 조절한다[1].
안정 시, 혈관 내피세포는 조약돌 모양의 고유한 형태학적 특성을 가지는 것으로 알려져 있다[3]. 유산소성 운동 등을 통해 증가하는 혈류속도의 변화는 혈류역학적 마찰력(Hemodynamic friction force)을 의미하는 혈관 내 전단응력(shear stress)을 증가시키는데, 이러한 과정 중에 혈관 내피세포의 형태가 혈류방향을 따라 길어지며 세포해부학적으로 안정화된 구조가 만들어진다[3,4]. 또한 운동에 의해 유발되는 혈관 내 전단응력의 향상은 전체 혈관의 기능 개선과 항상성 유지에 필수적인 산화질소 합성효소(endothelial nitric oxide synthase, eNOS)를 활성화시켜 산화질소의 생성을 증가시킨다[5].
세포 내 자가소화작용을 의미하는 오토파지(autophagy)는 외부의 스트레스 또는 자극에 반응하여 세포질(Cytoplasm) 내에서 정상적인 기능을 하지 못하는 손상된 세포소기관(organelle)을 분해한다[6]. 이 중 거대자가포식(macroautophagy)은 차후 재활용 또는 소멸 과정으로의 진입을 유도함으로써 세포의 에너지 대사 및 산화 ·환원 반응을 정상적으로 유지하게 한다[7,8]. 이 과정에서 세포 내외적인 스트레스에 의해 손상된 소기관들은 자가포식소포체(autophagosome)라고 하는 이중막 소낭에 에워싸이게 되는데, 오토파지 관련 유전자(Atg5, 6, 12, autophagy-related gene)가 소낭의 초기 막형성에 관여하는 것으로 알려져 있다[9]. 용해성의 유비퀴틴 단백질인 LC3 (microtubule- associated protein 1A/1B-light chain 3)은 단백질 분해효소인 Atg4에 의해 변형되어 LC3I이 되고, LC3I은 포스파티딜에탄올라민(phosphatidylethanolamine)에 의해 LC3II로 변형되는데, 이 과정에 Atg3, 7 등과 같은 오토파지 단백질이 관여하게 된다[10]. 오토파지의 최종 생체지표 역할을 하는 LC3II는 자가포식소포체의 성장과 최종 형성에 직접적인 역할을 하며, p62 단백질은 손상된 소기관을 자가포식소포체에 연결하고 차후 과정에서 리소좀(lysosome)과 자가포식소포체의 결합체인 자가포식용해소체(autophagolysosome)의 형성을 통한 세포 소기관의 최종 소멸을 유도하면서 자가포식소포체와 함께 분해된다[11]. 따라서 오토파지의 기능은 시작 단계에 관여하는 Atg3, 4, 5, 6, 7, 12 등과 같은 Atg family의 발현량 증가와 p62 단백질의 소멸, LC3II 단백질의 축적과 상대적인 LC3I의 감소 등을 통해 정량화할 수 있다[12,13].
관련 연구들에 따르면, 장기간의 영양결핍 및 유전적 결함으로 유래된 극단적인 오토파지의 지속은 근질환 및 선암(adenocarcinoma) 등을 유발하는 등 부정적인 병리학적 현상을 야기시키는 것으로 알려져 있으나[14,15], 이와 반대로, 일반적인 상황에서의 오토파지의 감소는 혈관 기능의 저하를 유발하고 염증반응을 촉진하여 혈관 및 다양한 조직의 항상성에 부정적인 결과를 초래하는 것으로 보고되고 있다[16-18]. 또한 오토파지의 기능 저하는 내피세포 신호를 조절하는 단백질 및 미토콘드리아의 기능 장애를 유발하여, 산화 스트레스를 유발하는 것으로 알려져 있다[19,20]. 최근 연구에서는 오토파지 기능이 혈관 기능 향상에 기여하는 산화질소 생성의 기전에도 관여하는 것으로 보고되고 있어[21], 혈관 내 전단응력 증가와 오토파지 관련 단백질 발현에 대한 연구가 필요하다. 또한, 혈관기능의 필수적인 요소로 받아들여지는 오토파지가 유산소성 운동에 의해 혈관 내피세포에서 특이적으로 증가하는지 여부에 대한 논의는 명확히 검증되지 않은 상태에 있다. 따라서 본 연구에서 (1) 건강한 마우스에게 자발적인 유산소성 운동환경을 조성하여 혈관 오토파지 단백질의 발현이 증가하는 것을 확인하고, (2) 혈관 내피세포의 대표적인 세포주인 human aortic endothelial cells (HAEC)와 human umbilical vein endothelial cells (HUVEC)을 배양하여 전단응력과 관련 단백질 발현의 직접적인 인과관계가 있는지 추가 검증함으로써, 차후 혈관기능의 개선이 필요한 심혈관 환자에게 유산소성 운동의 심층적 기전을 제공하는 데 그 목적이 있다.
연구 방법
1. 실험세포 배양 및 전단응력 처치
본 연구의 실험에 사용된 HAEC 세포와 HUVEC 세포는 20%의 fetal bovine serum (FBS)이 함유된 EGM-2와 M199 배양액에서 각각 배양되었으며[22], 세포배양을 위한 인큐베이터의 내부 환경은 37℃ 온도와 5% CO2로 유지되었다. 배양된 세포를 이용한 모든 실험과정은 반복된 계대배양으로 유도되는 세포노화의 영향을 극소화하기 위해 패시지 3-5에서 실시되었다. 배양된 세포의 전단응력(laminar shear stress) 처치는 배양 세포가 6웰 플레이트(6-well plate)에서 약 90-100%의 밀도로 증식되었을 때, 오비탈 셰이커(orbital shaker)를 이용하여 20 dyne/cm2의 강도로 24시간 실시하였다. 전단응력의 처치 강도는 τmax=α√ (p ×η (2πf)3)로 계산되었다(α=orbital radius, p =medium density, η=viscosity of the medium, f=frequency of rotation) [17,23].
2. 실험동물 및 운동처치
본 연구의 실험동물은 10주령의 수컷 C57BL/6 마우스 20마리로 하였다. 동물의 사육환경은 평균온도 21±2℃, 습도 50 ±5%, 주간 및 야간의 순환은 각각 12시간(주간시간 07:00-19:00)으로 유지되었으며, 물과 사료는 제한 없이 섭취하도록 공급되었다. 실험동물 20마리 중, 무작위로 선발된 10마리의 운동군(VWR group)은 직경 11.5 cm의 금속 휠이 설치된 케이지에서 개별적으로 사육되었으며, 1주일간의 적응기간을 거친 후, 12주간의 자발적 휠 달리기 운동(voluntary wheel running)을 실시하였다. 나머지 10마리의 비운동군(SED group)은 케이지당 5마리씩 사육되었다. 본 연구를 위한 실험동물은 국제 association for assessment and accreditation of laboratory animal care (AAALAC) 인증기관인 U대학교의 동물실험윤리위원회(IACUC)의 승인(Protocol#15-05003)을 거쳐, 실험동물 관리 지침에 따라 사육되었다. 실험동물의 체중은 매주 수요일 13:00에 주 1회 측정하였으며, 운동군의 일일 주행거리는 휠의 회전 수와 거리를 측정하는 디지털 카운터에 의해 자동 측정되었으며, 매일 오후 13:00에 확인 및 기록하였다.
3. 조직처리
본 연구에서 사용된 모든 실험 동물은 12주간의 자발적 휠 달리기 운동 후, 100%의 산소와 혼합된 2-4%의 이소플루레인(isoflurane)의 흡입을 통해 마취 후, 흉강을 열고 대동맥(aorta)를 샘플링하였다. 전체 대동맥은 단백질 발현량 측정에 필요한 면역 블랏(immunoblotting)을 위해 샘플링 후, 액화질소(liquid nitrogen)에 급속 냉동 후, -80℃ 냉동고에 저장되었다.
4. Immunoblot
-80℃에 저장된 대동맥 샘플은 4℃로 냉장 보관된 RIPA 용액(10 mM Tris-HCl, 5 mM EDTA, 150 mM에 NaCl, 1% triton X-100, 0.1% SDS, 1% deoxycholate, pH 7.5)에서 균질화(homogenization)하여 용해하였다. 배양된 실험세포는 전단응력 처치 종료 후, 차가운 DPBS 버퍼에 워싱과정을 거쳐 RIPA 용액에 용해하였다. RIPA 용액에 용해된 샘플들은 4℃에서 16,000 g로 15분간 원심분리 후, 상층액을 수집하였다. 브래드포드 단백질 에세이(bradford protein assay)를 통해 단백질의 농도를 측정 후, sodium dedocyl sulfate (SDS)를 혼합하고, polyacrylamide gel electrophoresis (PAGE) 전기영동을 실시하였다. 젤상의 SDS-단백질 혼합물은 Immobilon-P 멤브레인으로 이동시킨 후, 화학발광(chemiluminescence) 기법을 이용하여 단백질 발현량을 관찰하였다. Atg3 (cell signaling, product no. 3415), Atg7 (cell signaling, product no. 8558), LC3II (sigma, product no. L7543), p62 (novus, product no. H00008878-M01) 등과 같은 오토파지 관련 유전자의 1차 항체(primary Antibody)를 이용하여 오토파지 발현량을 측정하였고, GAPDH (cell signaling, product no. 2118)를 내부 대조 유전자로 활용하였다. 각각의 단백질 발현량의 수치화된 객관적 측정을 위해 Image J (NIH) 소프트웨어를 활용하였다.
연구 결과
1. 자발적 휠 달리기 운동에 따른 마우스 체중의 변화
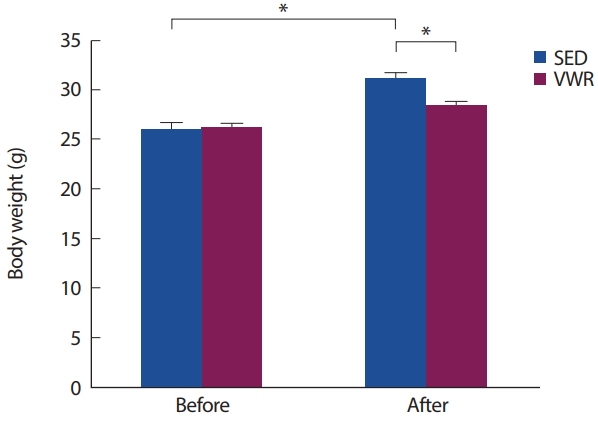
12주간 자발적 휠 달리기 운동에 따른 비운동군(SED)과 운동군(VWR) 간 마우스 체중 변화는 Fig. 1과 같다. 자발적 휠 달리기를 통해 수행된 운동군의 일일 평균 운동량은 6.1 km/day였으며, 비운동군은 사전에 비해 사후 체중이 유의하게 증가하였으나, 운동군의 체중은 다소 증가하는 경향성을 나타내었을 뿐, 사전·사후 간 통계적 유의차는 나타나지 않았다. 그룹 간 체중 비교 결과, 운동군의 12주간 체중 증가량은 비운동군에 비해 유의하게 낮았다.
2. 운동에 따른 마우스 대동맥의 오토파지 변화
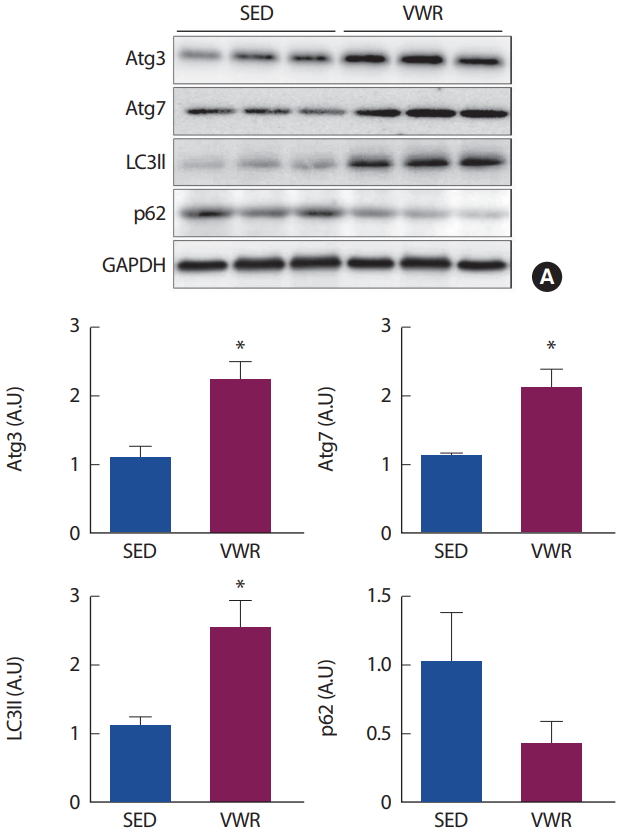
12주간 자발적 휠 달리기 운동에 따른 Atg3, Atg7, LC3II, p62 등과 같은 오토파지 관련 단백질 발현량의 변화는 Fig. 2와 같다. 먼저, 오토파지의 시작 단계에 관여하는 Atg3와 Atg7 단백질은 12주간의 자발적 달리기 운동을 통해 그 발현량이 유의하게 증가하였다. 오토파지 기능의 최종 산물인 LC3II 발현 역시 운동군에서 유의한 증가를 나타내었다. 오토파지가 정상적으로 기능함에 따라 자가포식소포체와 함께 최종적으로 소멸됨으로써 그 최종 발현량이 감소하게 되는 p62의 발현량은 운동군에서 대조군에 비해 낮은 경향성을 나타내었으나, 통계적인 유의차는 발견되지 않았다.
3. 전단응력 처치에 따른 HAEC 세포에서의 오토파지 변화
실험 환경에서 배양된 HAEC 세포에 20 dyne/cm2의 강도로 24시간 실시한 전단응력 처치에 따른 Atg3, Atg7 단백질 발현량 및 LC3II/I의 상대적 발현량 분석 결과는 Fig. 3과 같다. Atg3 단백질은 전단응력 처치에 따라 유의한 증가를 보였으며, Atg7은 그 발현량의 증가 경향을 나타내었지만, 통계적인 유의차는 발견되지 않았다. LC3I에 대한 LC3II 변화량 또한 증가하였으나, 유의차는 나타나지 않았다.
4. 전단응력 처치에 따른 HUVEC 세포에서의 오토파지 변화
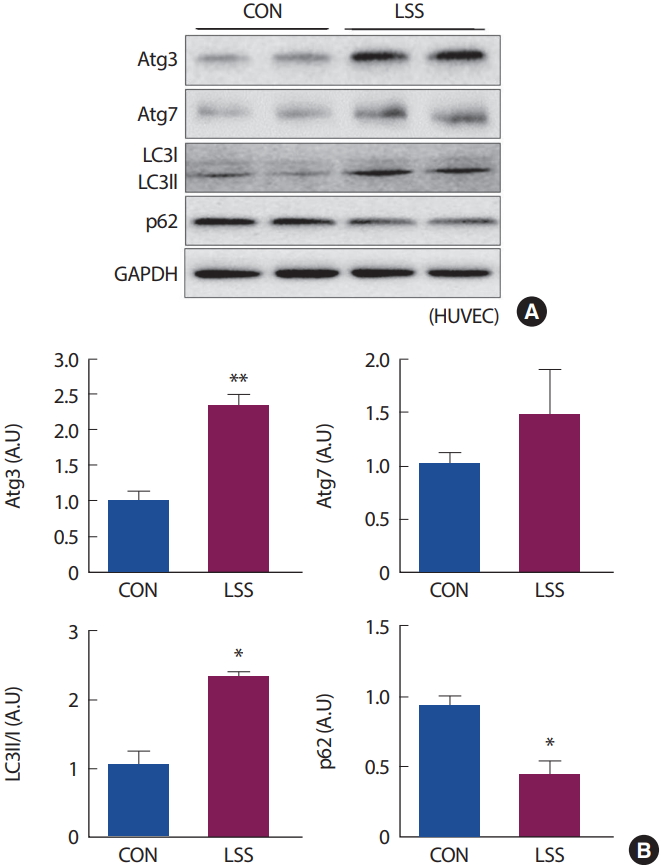
실험 환경에서 배양된 HUVEC 세포에 20 dyne/cm2의 강도로 24시간 실시한 전단응력 처치에 따른 Atg3, Atg7, p62 단백질 발현량 및 LC3II/I의 상대적 발현량 분석 결과는 Fig. 4와 같다. Atg3 단백질은 전단응력 처치에 따라 유의한 증가를 보였으며, Atg7은 그 발현량의 증가 경향을 나타내었지만, 통계적인 유의차는 발견되지 않았다. 오토파지 기능의 직접적 지표인 LC3II 단백질은 전단응력 처치에 따라 유의한 증가를 나타내었으며, 오토파지 기능 활성에 따라 그 발현량이 감소하는 p62 단백질은 전단응력 처치 그룹에서 유의한 감소를 나타내었다.
논 의
본 연구는 혈관기능 항상성 유지에 필수적 요소로 받아들여지는 오토파지가 유산소성 운동에 의해 유발되는 혈관 내 전단응력 증가를 통해 내피세포에서 그 발현이 증가하는지를 검증함으로써, 심혈관 기능 향상을 위한 유산소 운동의 효과를 다시 한 번 확인하고, 그 분자생물학적 기전을 파악하는 데 그 목적이 있다. 연구의 목적을 달성하기 위해 본 연구에서는 12주간 건강한 마우스에게 자발적 휠 달리기 운동을 실시하여 대동맥의 오토파지 관련 단백질 발현량을 비운동군과 비교·분석하였다. 아울러, 혈관 조직에서 나타난 오토파지의 변화가 유산소성 운동을 통해 증가하는 전단응력과 이에 직접적으로 노출되는 혈관 내피세포에서 나타나는 생리학적 현상인지를 검증하기 위해 배양된 HAEC 및 HUVEC 세포에 전단응력을 처치하여 오토파지 발현량을 측정하였다.
본 연구의 12주간 자발적 휠 달리기 운동을 실시한 운동군의 일일 평균 달린 거리는 약 6.1 km/day로 나타났다. 비운동군이 12주 동안 평균 체중이 유의하게 증가한 반면, 운동군은 체중 변화가 나타나지 않았으며, 12주 후 그룹 간 체중 비교 결과, 운동군의 12주간 체중 증가량은 비운동군에 비해 유의하게 낮았다(Fig. 1). 이는 본 연구에서 처치된 12주간의 자발적 휠 달리기 운동이 충분한 유산소성 운동 효과를 나타내는 강도와 기간이었음을 의미한다[24]. 이러한 12주간의 유산소성 운동은 추출된 대동맥 조직의 단백질 발현량 측정 결과, 오토파지의 관련 단백질인 Atg3, Atg7와 오토파지 지표인 LC3II의 발현량을 증가시켰다. 반면, 오토파지가 기능함에 따라 자가포식소포체와 함께 최종 소멸됨으로써 그 발현이 자연적으로 감소하는 p62의 발현량은 유산소성 운동을 통해 감소하는 경향을 보였다(Fig. 2). 이러한 결과는 뇌 또는 골격근 조직에서 규칙적인 운동을 통해 오토파지 발현의 증가가 나타났다는 선행연구들의 결과와 일치하였으며[25-27], 본 연구에서는 지속적인 유산소성 운동이 혈관 조직에 있어서도 오토파지 관련 단백질 발현의 증가를 유발한다는 사실을 발견하였다. 즉, 규칙적인 운동은 뇌, 골격근 뿐만 아니라, 혈관 조직에 있어서도 오토파지 기능 향상 기전을 통해 항상성 유지에 기여한다는 사실을 발견할 수 있었다.
최근의 연구에 따르면, 혈관의 오토파지 기능 손상은 미토콘드리아의 생합성과 재건에 치명적인 결함을 유도하여 활성산소종(ROS)의 증가를 유도하는 것으로 알려져 있다[19,20]. 만성적인 활성산소종은 염증반응을 유도하고, 혈관 내피세포의 산화질소 합성기전을 감소시켜 항상성 불균형을 초래한다[16-18]. 따라서 유산소성 운동으로 유도된 Atg3, Atg7 및 LCII의 발현은 오토파지의 촉진을 통한 혈관 기능향상에 매우 중요한 요소라고 할 수 있다.
하지만 운동은 전단응력을 높일 뿐 아니라 다수의 생리학적 자극들을 생성시킴으로써, 동물실험만으로 전단응력과 혈관 내피세포 오토파지 단백질 발현의 직접적인 인과관계를 밝히기에는 부족함이 있다. 또한 동물실험기법의 한계로 인하여, 실험용 쥐의 대동맥적출 시 내피와 평활근 세포의 완벽한 분리가 기술적으로 한계가 존재한다. 따라서 유산소 운동에 의해 유발된 혈관 조직의 오토파지 기능 향상이 혈관내피세포에 의한 것인지 명확히 단정을 내리기 어려운 점이 있다.
동물실험기법을 극복하고 전단응력과 혈관내피세포 오토파지의 직접적인 인과관계를 밝히기 위해, 본 연구에서는 배양된 HAEC 세포와 HUVEC 세포에 운동시 유도되는 전단응력의 물리학적 수준인 20 dyne/cm2 강도로 직접 처치를 하였다.
오비탈 셰이커를 통해 전단응력 처치 결과 HAEC 세포와 HUVEC 세포에서는 오토파지 시작단계에 자가포식소포체의 생성과 성장에 관여하는 Atg3 단백질의 발현이 유의하게 증가하였으며, 오토파지 지표 단백질인 LC3II의 발현량 또한 증가하였다. 이는 동일한 강도와 실험 방법으로 3시간 동안 Bovine Aortic Endothelial Cells (BAEC) 세포에 전단응력을 처치한 선행연구의 실험 결과와 일치하였다[17,21]. 유산소성 운동을 처치받은 동물과 전단응력을 처치한 세포연구 결과를 종합해보면, 운동을 통한 혈관 조직의 오토파지 향상과 혈관 기능의 개선은 운동성 전단응력의 증가에 기인하는 것임을 알 수 있었다.
차후 연구에서는 혈관 내막을 구성하는 내피세포층과 중·외막을 구성하는 평활근 세포층을 구분하여 연구를 진행함으로써, 혈관 조직 중 운동을 통한 오토파지 기능의 향상이 실제적으로 어느 층에서 일어나는지를 명확히 검증할 필요가 있겠다. 또한 영양상태와 오토파지 기능변화의 연관성이 보고되어 있는 상황이므로 운동, 식이, 그리고 오토파지의 인과관계를 밝히는 복합적인 연구가 필요할 것으로 사료된다[28]. 이는 혈관 기능 개선을 위한 운동처방의 과학적인 지침을 만드는 데 도움이 될 것이라 사료된다.
결 론
본 연구에서는 12주간 자발적 휠 달리기 운동은 건강한 마우스의 대동맥 오토파지 기능을 향상시키는 효과를 나타내는 것으로 나타났다. 또한 이러한 혈관 조직에서의 오토파지 기능 향상이 혈관 내피세포에서의 오토파지와 직접적 관련이 있는지를 파악하기 위해 배양된 HAEC 및 HUVEC 세포에 고강도 전단응력을 처치한 결과, 혈관 내피세포의 오토파지 관련 단백질 발현량이 대조군에 비해 유의하게 증가하는 결과를 나타내었다. 따라서 본 연구의 결과는 지속적인 유산소성 운동은 혈관 내피세포에 가해지는 혈류 전단응력의 향상을 통해 내피세포 및 혈관 조직 전체의 오토파지 기능을 증진하며, 이를 통해 혈관 기능 항상성에 기여하는 것으로 판단된다.